-
1
-
2
-
3
-
4
-
5
-
6
-
7
-
8
-
9
-
10
-
11
-
12
-
13
-
14
-
15
-
16
-
17
-
18
-
19
-
20
-
21
-
22
-
23
-
24
-
25
-
26
-
27
-
28
-
29
-
30
-
31
-
32
-
33
-
34
-
35
-
36
-
37
-
38
-
39
-
40
-
41
-
42
-
43
-
44
-
45
-
46
-
47
-
48
-
49


본문내용
362
1.344
50ml
90ml
84.5
1.362
1.341
50ml
100ml
84.8
1.361
1.340
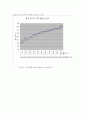
그림4-2. 물의 증가에 따른 끓는점 변화 그래프
※ 물이 증가함에 따라 끓는점이 높아진다.
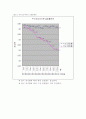
그림4-3. 부피조성에따른 굴절률변화
※ 물이 증가함에 따라 액상 굴절률이 감소한다.
※ 물이 증가함에 따라 기상 굴절률은 거의 일정하다.
②-3 순수한 물질의 굴절률(물, 에탄올)
표6. 순수한 물질의 측정된 굴절률
물
에탄올
측정 굴절률
1.332
1.363
표7. 순수한 물질의 굴절률(문헌치)
물(20℃)
에탄올
굴절률(문헌치)
1.33
1.36
그림4-4. 문헌상의 굴절률
③ 몰 굴절성(Rx)의 계산
③-1 Lorents-Lorez 식
n = 진공에 대한 시료의 굴절률
M = 시료의 분자량
ρ = 시료의 밀도
NA = 아보가드로 수
③-2 물의 몰 굴절성 계산
③-3 에탄올의 몰 굴절성 계산
④ 도표화된 결합굴절률을 조화시킨 분자구조 예측
④-1 결합굴절률 도표
표8. 결합굴절률 도표
그 룹 R(cm³/mol)
그 룹 R(cm³/mol)
C - O 1.51
O - H 1.73
H - H 2.08
C - H 1.70
C - C 1.21
C = C 4.15
C = C 6.03
C = O 3.42
C = H 3.38
C-O-C 2.85
C-O-H 3.23
Cl- 5.967
Br- 8.865
I- 13.90
④-2 물의 분자구조 예측
* 실험을 통해 얻어낸 물의 몰굴절성(R)=3.69
RH2O = 3.69
* 표8에서의 O-H의 결합굴절률=1.73
RO-H = 1.73
* RH2O = RO-H + RO-H = 2RO-H
3.69 ≒ 2*1.73 = 3.43
※ 문헌치와 다소 차이가 보임
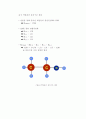
그림4-5 물의 분자구조 예측
④-3 에탄올의 분자구조 예측
* 실험을 통해 얻어낸 에탄올의 몰굴절성(R)=12.95
RC2H5OH = 12.95
* 표8를 통한 결합굴절률
RC-H = 1.70
RC-C = 1.21
RC-O = 1.51
RO-H = 1.73
* RC2H5OH = 5RC-H + RC-C + RC-O + RO-H
12.95 ≒ 5*1.70 + 1.21 + 1.51 + 1.73 = 12.95
※ 문헌치와 거의 정확히 맞음
그림4-6 에탄올의 분자구조 예측
4.2 결과 데이터 검증
* Rth와 Rex의 편차
※ Rth = 방정식에 의해서 계산된 R의 값
※ Rex = 추정된 심료에 대하여 표8로부터 얻어진 R의 이론적인 값
① Rth와 Rex의 값
표9. Rth와 Rex의 값
시료
몰굴절성
얻는 과정
얻어진 값
물
Rth
3.69
Rex
RH2O = RO-H + RO-H = 2RO-H
2*1.73 = 3.43
3.43
에탄올
Rth
12.95
Rex
RC2H5OH = 5RC-H + RC-C + RC-O + RO-H
5*1.70 + 1.21 + 1.51 + 1.73 = 12.95
12.95
② Rth와 Rex의 편차
* 물의 Rth와 Rex의 편차
* 에탄올의 Rth와 Rex의 편차
5. 결론
이번 실험을 통해 우리는 굴절률 측정법을 알게 되었으며, 반복적인 실습으로 Abbe굴절계를 보다 익숙하게 다룰 수 있게 되었다. 뿐만 아니라 굴절계의 원리를 알게 되었고, 굴절률을 통한 많은 인접 지식을 연결할 수 있는 계기가 되었다.
또한 측정한 굴절률을 바탕으로 Lorents-Lorez 식을 통해 몰 굴절성을 알 수 있었다. 몰 굴절성은 분자배열에 대한 특성값이며 그 값은 굴절률과 분자량, 밀도만 알고 있으면 쉽게 구할 수 있었다. 몰 굴절성은 화합물 안에서 각 원자와 그들의 결합형태가 나타내는 각 특성값들의 합으로 표현 할 수 있었다. 그래서 결합 굴절률을 통해 그 분자의 구조를 예측할 수 있었다.
굴절률 측정결과 문헌치와 거의 일치하게 측정되었으며, 계산된 몰 굴절성 값과 표를 통해 얻어진 이론적 값을 비교한 결과 물은 7.05%차이를 보였고, 에탄올은 0%차이를 보여 비교적 정확한 데이터를 얻었다.
6. 토의사항
이번실험은 비교적 정확한 데이터를 얻을 수 있었다. 우선 Abbe굴절계를 통한 시료의 굴절률이 문헌치와 거의 일치하게 측정되었다. 그 이유는 굴절계의 프리즘 표면을 약솜으로 깨끗이 닦아준 후 건조를 잘 시켜줘서 그런 것 같다. 만약 아세톤이나 벤젠을 가지고 프리즘을 닦아주고 채 마르기도 전에 측정할 시료를 넣었으면 굴절률이 다소 오차가 생겼을 것이다.
비교적 정확한 데이터를 얻었음에도 불구하고 다소 오차가 생긴 이유는 다음과 같다.
항온조의 온도가 일정하지 않았다. 굴절계는 온도에 아주 민감한 장치이기에 온도를 일정하게 유지시켜주는 항온조의 온도를 일정하게 해주는 것이 생명이다. 그러나 이번 실험은 항온조의 온도가 약간씩 변함에도 불구하고 굴절률을 측정한 결과 다소 오차가 생겼다.
또한 미세한 먼지 때문에 생긴 오차도 무시를 못할 것이다. 굴절계는 온도는 물론 미세먼지에 직접적인 영향을 받아 결과 값이 확연히 다르게 나올 수 있어 먼지에 대해 각별한 조심을 해야 하는데 이번 실험에서는 약간의 미세먼지가 들어가 측정값에 미소의 오차를 낸 것 같다.
한편 시료 자체가 약간은 불순했다. 시료를 채취해야 할 피펫 속에 약간의 이물질이 들어가 있는 상태에서 시료를 채취하여 시료 자체에서 약간의 오차가 시작된 걸로 보인다.
7. 사용부호
M : 시료의 분자량 [ g /mole ]
m : 몰랄농도 [mol/kg]
N : 아보가드로 수
n : 진공에 대한 시료의 굴절율
P : 압력 [torr]
p : 시료의 밀도 [ g / cm ]
R : 몰 굴절성 [ cm / mol ]
T : 온도 [°K]
8. 참고문헌
1. P.W. Atkins, 물리화학, 청문사, 6, 717-734
2. 대한화학회, 물리화학실험, 청문사, 1, 42-47(1999)
3. 김정림, "물리화학실험" 자유아카데미, 1, 349-371, 1999
4. 이공교재편찬회 저자, “물리화학과 연습”, 탑출판사, 74-79, 1982
5. 네이버 백과사전
6. 두산 동아세계백과사전
7. http://www.buylab.co.kr
8. 이영만, 김득호 “High Top 화학2” 두산동아
1.344
50ml
90ml
84.5
1.362
1.341
50ml
100ml
84.8
1.361
1.340
그림4-2. 물의 증가에 따른 끓는점 변화 그래프
※ 물이 증가함에 따라 끓는점이 높아진다.
그림4-3. 부피조성에따른 굴절률변화
※ 물이 증가함에 따라 액상 굴절률이 감소한다.
※ 물이 증가함에 따라 기상 굴절률은 거의 일정하다.
②-3 순수한 물질의 굴절률(물, 에탄올)
표6. 순수한 물질의 측정된 굴절률
물
에탄올
측정 굴절률
1.332
1.363
표7. 순수한 물질의 굴절률(문헌치)
물(20℃)
에탄올
굴절률(문헌치)
1.33
1.36
그림4-4. 문헌상의 굴절률
③ 몰 굴절성(Rx)의 계산
③-1 Lorents-Lorez 식
n = 진공에 대한 시료의 굴절률
M = 시료의 분자량
ρ = 시료의 밀도
NA = 아보가드로 수
③-2 물의 몰 굴절성 계산
③-3 에탄올의 몰 굴절성 계산
④ 도표화된 결합굴절률을 조화시킨 분자구조 예측
④-1 결합굴절률 도표
표8. 결합굴절률 도표
그 룹 R(cm³/mol)
그 룹 R(cm³/mol)
C - O 1.51
O - H 1.73
H - H 2.08
C - H 1.70
C - C 1.21
C = C 4.15
C = C 6.03
C = O 3.42
C = H 3.38
C-O-C 2.85
C-O-H 3.23
Cl- 5.967
Br- 8.865
I- 13.90
④-2 물의 분자구조 예측
* 실험을 통해 얻어낸 물의 몰굴절성(R)=3.69
RH2O = 3.69
* 표8에서의 O-H의 결합굴절률=1.73
RO-H = 1.73
* RH2O = RO-H + RO-H = 2RO-H
3.69 ≒ 2*1.73 = 3.43
※ 문헌치와 다소 차이가 보임
그림4-5 물의 분자구조 예측
④-3 에탄올의 분자구조 예측
* 실험을 통해 얻어낸 에탄올의 몰굴절성(R)=12.95
RC2H5OH = 12.95
* 표8를 통한 결합굴절률
RC-H = 1.70
RC-C = 1.21
RC-O = 1.51
RO-H = 1.73
* RC2H5OH = 5RC-H + RC-C + RC-O + RO-H
12.95 ≒ 5*1.70 + 1.21 + 1.51 + 1.73 = 12.95
※ 문헌치와 거의 정확히 맞음
그림4-6 에탄올의 분자구조 예측
4.2 결과 데이터 검증
* Rth와 Rex의 편차
※ Rth = 방정식에 의해서 계산된 R의 값
※ Rex = 추정된 심료에 대하여 표8로부터 얻어진 R의 이론적인 값
① Rth와 Rex의 값
표9. Rth와 Rex의 값
시료
몰굴절성
얻는 과정
얻어진 값
물
Rth
3.69
Rex
RH2O = RO-H + RO-H = 2RO-H
2*1.73 = 3.43
3.43
에탄올
Rth
12.95
Rex
RC2H5OH = 5RC-H + RC-C + RC-O + RO-H
5*1.70 + 1.21 + 1.51 + 1.73 = 12.95
12.95
② Rth와 Rex의 편차
* 물의 Rth와 Rex의 편차
* 에탄올의 Rth와 Rex의 편차
5. 결론
이번 실험을 통해 우리는 굴절률 측정법을 알게 되었으며, 반복적인 실습으로 Abbe굴절계를 보다 익숙하게 다룰 수 있게 되었다. 뿐만 아니라 굴절계의 원리를 알게 되었고, 굴절률을 통한 많은 인접 지식을 연결할 수 있는 계기가 되었다.
또한 측정한 굴절률을 바탕으로 Lorents-Lorez 식을 통해 몰 굴절성을 알 수 있었다. 몰 굴절성은 분자배열에 대한 특성값이며 그 값은 굴절률과 분자량, 밀도만 알고 있으면 쉽게 구할 수 있었다. 몰 굴절성은 화합물 안에서 각 원자와 그들의 결합형태가 나타내는 각 특성값들의 합으로 표현 할 수 있었다. 그래서 결합 굴절률을 통해 그 분자의 구조를 예측할 수 있었다.
굴절률 측정결과 문헌치와 거의 일치하게 측정되었으며, 계산된 몰 굴절성 값과 표를 통해 얻어진 이론적 값을 비교한 결과 물은 7.05%차이를 보였고, 에탄올은 0%차이를 보여 비교적 정확한 데이터를 얻었다.
6. 토의사항
이번실험은 비교적 정확한 데이터를 얻을 수 있었다. 우선 Abbe굴절계를 통한 시료의 굴절률이 문헌치와 거의 일치하게 측정되었다. 그 이유는 굴절계의 프리즘 표면을 약솜으로 깨끗이 닦아준 후 건조를 잘 시켜줘서 그런 것 같다. 만약 아세톤이나 벤젠을 가지고 프리즘을 닦아주고 채 마르기도 전에 측정할 시료를 넣었으면 굴절률이 다소 오차가 생겼을 것이다.
비교적 정확한 데이터를 얻었음에도 불구하고 다소 오차가 생긴 이유는 다음과 같다.
항온조의 온도가 일정하지 않았다. 굴절계는 온도에 아주 민감한 장치이기에 온도를 일정하게 유지시켜주는 항온조의 온도를 일정하게 해주는 것이 생명이다. 그러나 이번 실험은 항온조의 온도가 약간씩 변함에도 불구하고 굴절률을 측정한 결과 다소 오차가 생겼다.
또한 미세한 먼지 때문에 생긴 오차도 무시를 못할 것이다. 굴절계는 온도는 물론 미세먼지에 직접적인 영향을 받아 결과 값이 확연히 다르게 나올 수 있어 먼지에 대해 각별한 조심을 해야 하는데 이번 실험에서는 약간의 미세먼지가 들어가 측정값에 미소의 오차를 낸 것 같다.
한편 시료 자체가 약간은 불순했다. 시료를 채취해야 할 피펫 속에 약간의 이물질이 들어가 있는 상태에서 시료를 채취하여 시료 자체에서 약간의 오차가 시작된 걸로 보인다.
7. 사용부호
M : 시료의 분자량 [ g /mole ]
m : 몰랄농도 [mol/kg]
N : 아보가드로 수
n : 진공에 대한 시료의 굴절율
P : 압력 [torr]
p : 시료의 밀도 [ g / cm ]
R : 몰 굴절성 [ cm / mol ]
T : 온도 [°K]
8. 참고문헌
1. P.W. Atkins, 물리화학, 청문사, 6, 717-734
2. 대한화학회, 물리화학실험, 청문사, 1, 42-47(1999)
3. 김정림, "물리화학실험" 자유아카데미, 1, 349-371, 1999
4. 이공교재편찬회 저자, “물리화학과 연습”, 탑출판사, 74-79, 1982
5. 네이버 백과사전
6. 두산 동아세계백과사전
7. http://www.buylab.co.kr
8. 이영만, 김득호 “High Top 화학2” 두산동아