목차
1. 목적(Objective)
2. 요지(Summary)
3. 이론(Theory)
4. 시약, 기구, 장치(Reagents, Instruments, Apparatus)
5. 실험 방법 및 과정(Experimental Procedure)
6. 계산(Calculation)
7. 결과 및 고찰(Results and Discussion)
8. 기호(Nomenclature)
9. 인용문헌(References)
2. 요지(Summary)
3. 이론(Theory)
4. 시약, 기구, 장치(Reagents, Instruments, Apparatus)
5. 실험 방법 및 과정(Experimental Procedure)
6. 계산(Calculation)
7. 결과 및 고찰(Results and Discussion)
8. 기호(Nomenclature)
9. 인용문헌(References)
본문내용
N
= 60.05g * 1000
= 30.025g * 500
0.5N
= 15.0125g * 500
0.25N
= 7.50625g * 500
0.125N
= 3.753125g * 500
0.0625N
= 1.8765625g * 500
6.1 Toluene - 물 계
Toluene 50ml와 각각 다른 농도를 가진 식초산 50ml를 넣어 4개의 혼합 용액을 만든다.
실험값
식초산 농도(N)
0.5
0.25
0.125
0.0625
분취량()
10
20
20
20
적정량()
7.92
3.88
1.63
0.75
0.492
0.248
0.124
0.0621
0.489
0.246
0.123
0.0610
64.9
140.6
177.2
208.2
62.121
127.84
152.15
165.60
65.251
141.71
178.67
211.95
[표 3] Toluene-식초산 혼합용액의 식초산 농도에 따른 결과값
계산 관련식
( : 적정염기의 농도, : 적정량, : 취해준 부피)
( : 에서의 초기농도, : 전체 평형 농도)
()
( : 산의 해리상수)
계산
① 0.5 식초산
② 0.25 식초산
③ 0.125 식초산
④ 0.0625 식초산
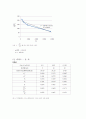
∴ 절편 = 195.33
= 195.33
6.2 에테르 - 물 계
실험값
식초산 농도()
0.5
0.25
0.125
분취량()
5
10
10
적정량()
39.60
34.25
17.00
0.396
0.171
0.085
0.104
0.079
0.040
0.393
0.169
0.084
0.104
0.079
0.040
0.263
0.467
0.476
0.263
0.462
0.471
0.265
0.467
0.476
[표 4] 디메틸에테르-식초산 혼합용액의 식초산 농도에 따른 결과값
계산 관련식
(N : 적정염기의 농도, V : 적정량, V' : 취해준 부피)
( : 상 1에서의 초기농도, : 전체 평형 농도)
()
※ 가 와 같은 것은 에테르 안에서는 산의 이온화 또는 회합이 일어나지 않기 때문이다.
※ 용매를 매번 써서 번 추출하면 추출되지 않고 남는 용질의 몰 수이다.
계산
① 0.5 식초산
② 0.25 식초산
③ 0.125 식초산
6.3 단일 추출, 되풀이 추출
실험값
단일 추출
되풀이 추출
적정량()
9.4
10.6
추출분율(%)
53.0
79.6
덜어낸 물의 양 : 20, 차이 : 1.2
계산 관련식
① 단일추출
② 되풀이추출
(: 에테르 용액의 부피, : 물의 부피)
계산
※ 추출 된 몰수
※아세트산과 수산화나트륨은 1=1이다. 그러므로 →이다
① 단일추출
② 되풀이추출
7. 결과 및 고찰(Results and Discussion)
7.1 결과
Toluene - 물 계에서 식초산 농도에 따른 , , , , .
식초산 농도(N)
0.5
0.25
0.125
0.0625
분취량()
10
20
20
20
적정량()
7.92
3.88
1.63
0.75
0.492
0.248
0.124
0.0621
0.489
0.246
0.123
0.0610
62.121
127.84
152.15
165.60
7.2 고찰
이 실험은 서로 섞이지 않는 두 용매 사이에서 일어나는 용질의 평형분배를 알아보는 것으로 이 실험에서는 식초산을 톨루엔 - 물 계, 에테르 - 물 계의 용질로 사용한다. 실험을 세가지로 나누어서 결과값을 얻었다.
이 실험의 원리는 각 물질이 비중(톨루엔<물, 디메틸에테르<물)에 따라 층을 생성하는 것을 이용한 것이다. 아세트산은 톨루엔과 에테르, 그리고 물에 모두 녹으므로 톨루엔과 물, 에테르와 물이 층을 만들 때 물에 녹아있던 아세트산이 톨루엔과 에테르에 각각 녹아들어가게 된다. 그리고 어느 정도 시간이 되면 아세트산의 농도(각 용액에서)가 일정하게 되는데, 이 때가 평형 상태이다. 이 상태에서의 톨루엔과 에테르를 수산화나트륨 수용액으로 적정한다. 그에 따른 결과값으로 분배계수를 결정할 수 있다.
실험 결과 톨루엔 - 물 계 실험에서 분배계수는 0.5, 0.25, 0.125, 0.0625 식초산농도에 따라 각각 64.9, 140.6, 177.2, 208.2로 측정되었으며 에테르 - 물 계 실험에서의 분배계수는 0.5, 0.25, 0.125 식초산 농도에 따라 0.263, 0.467, 0.476으로 측정되었다.
분배계수는 온도에 따른 함수이므로 모두 같은 값이 나와야하지만 실제로는 그렇지 않음을 보이고 있다. 분배계수에 대한 오차의 원인에는 여러 가지가 있을 수 있다. 첫 번째, 평형 상태에 있는 용액이 온도의 변화나 흔들림에 의하여 그 평형 상태가 깨져버려서 오차가 생겼을 수 있다. 두 번째, 정확한 기계가 아닌 피펫으로 용액을 옮겼기 때문에 시료의 정확한 양의 측정이 이루어지지 않아 이러한 오차가 생겼을 것이다. 세 번째, 용액으로 적정하는 과정에서 오차가 발생하였다. 적정을 할 때는 용액의 한 방울로도 변화가 크게 일어날 수 있으므로 정확하게 해야한다. 각 용액을 적정할 때마다 색깔의 진하기 정도가 달라서 이에 따른 오차도 있을 것으로 생각된다.
물로 에테르를 단일 추출한 결과 0.235(=0.235), 되풀이 추출한 결과는 0.102(=0.1
02)로 각각의 추출분율은 각각 53.0%, 79.6%로 단일 추출보다 되풀이 추출이 더 효율적이라는 것을 알 수 있다.
8. 기호(Nomenclature)
노르말 농도() : 용액 1 속에 녹아 있는 용질의 g당량수를 나타낸 농도를 말한다.
몰 농도() : 용액 1 속에 포함된 용질의 몰수를 용액의 부피로 나눈 값이다. 으로 표시한다.
: 산의 해리상수. 산의 세기를 나타내는 척도로 값이 클수록 이온화 경향이 크다.
: 에서의 초기농도.
: 전체 평형 농도.
: 두 용매 사이에서 분배되는 용질 분자의 농도.
: 의 용매 에테르 용액에서의 용질의 농도.
: 의 용매 물을 써서 단일추출 한 후 용매 에테르 용액에서 추출되지 않고 남은 용질의 농도.
9. 인용문헌(References)
이문득, 물리화학실험, 자유아카데미, 1997.
H.D. Crockford 외 3명, “물리화학실험”, 탐구당, 1997.
http://mbel.kaist.ac.kr/lecture/che201/2002-4.ppt.
= 60.05g * 1000
= 30.025g * 500
0.5N
= 15.0125g * 500
0.25N
= 7.50625g * 500
0.125N
= 3.753125g * 500
0.0625N
= 1.8765625g * 500
6.1 Toluene - 물 계
Toluene 50ml와 각각 다른 농도를 가진 식초산 50ml를 넣어 4개의 혼합 용액을 만든다.
실험값
식초산 농도(N)
0.5
0.25
0.125
0.0625
분취량()
10
20
20
20
적정량()
7.92
3.88
1.63
0.75
0.492
0.248
0.124
0.0621
0.489
0.246
0.123
0.0610
64.9
140.6
177.2
208.2
62.121
127.84
152.15
165.60
65.251
141.71
178.67
211.95
[표 3] Toluene-식초산 혼합용액의 식초산 농도에 따른 결과값
계산 관련식
( : 적정염기의 농도, : 적정량, : 취해준 부피)
( : 에서의 초기농도, : 전체 평형 농도)
()
( : 산의 해리상수)
계산
① 0.5 식초산
② 0.25 식초산
③ 0.125 식초산
④ 0.0625 식초산
∴ 절편 = 195.33
= 195.33
6.2 에테르 - 물 계
실험값
식초산 농도()
0.5
0.25
0.125
분취량()
5
10
10
적정량()
39.60
34.25
17.00
0.396
0.171
0.085
0.104
0.079
0.040
0.393
0.169
0.084
0.104
0.079
0.040
0.263
0.467
0.476
0.263
0.462
0.471
0.265
0.467
0.476
[표 4] 디메틸에테르-식초산 혼합용액의 식초산 농도에 따른 결과값
계산 관련식
(N : 적정염기의 농도, V : 적정량, V' : 취해준 부피)
( : 상 1에서의 초기농도, : 전체 평형 농도)
()
※ 가 와 같은 것은 에테르 안에서는 산의 이온화 또는 회합이 일어나지 않기 때문이다.
※ 용매를 매번 써서 번 추출하면 추출되지 않고 남는 용질의 몰 수이다.
계산
① 0.5 식초산
② 0.25 식초산
③ 0.125 식초산
6.3 단일 추출, 되풀이 추출
실험값
단일 추출
되풀이 추출
적정량()
9.4
10.6
추출분율(%)
53.0
79.6
덜어낸 물의 양 : 20, 차이 : 1.2
계산 관련식
① 단일추출
② 되풀이추출
(: 에테르 용액의 부피, : 물의 부피)
계산
※ 추출 된 몰수
※아세트산과 수산화나트륨은 1=1이다. 그러므로 →이다
① 단일추출
② 되풀이추출
7. 결과 및 고찰(Results and Discussion)
7.1 결과
Toluene - 물 계에서 식초산 농도에 따른 , , , , .
식초산 농도(N)
0.5
0.25
0.125
0.0625
분취량()
10
20
20
20
적정량()
7.92
3.88
1.63
0.75
0.492
0.248
0.124
0.0621
0.489
0.246
0.123
0.0610
62.121
127.84
152.15
165.60
7.2 고찰
이 실험은 서로 섞이지 않는 두 용매 사이에서 일어나는 용질의 평형분배를 알아보는 것으로 이 실험에서는 식초산을 톨루엔 - 물 계, 에테르 - 물 계의 용질로 사용한다. 실험을 세가지로 나누어서 결과값을 얻었다.
이 실험의 원리는 각 물질이 비중(톨루엔<물, 디메틸에테르<물)에 따라 층을 생성하는 것을 이용한 것이다. 아세트산은 톨루엔과 에테르, 그리고 물에 모두 녹으므로 톨루엔과 물, 에테르와 물이 층을 만들 때 물에 녹아있던 아세트산이 톨루엔과 에테르에 각각 녹아들어가게 된다. 그리고 어느 정도 시간이 되면 아세트산의 농도(각 용액에서)가 일정하게 되는데, 이 때가 평형 상태이다. 이 상태에서의 톨루엔과 에테르를 수산화나트륨 수용액으로 적정한다. 그에 따른 결과값으로 분배계수를 결정할 수 있다.
실험 결과 톨루엔 - 물 계 실험에서 분배계수는 0.5, 0.25, 0.125, 0.0625 식초산농도에 따라 각각 64.9, 140.6, 177.2, 208.2로 측정되었으며 에테르 - 물 계 실험에서의 분배계수는 0.5, 0.25, 0.125 식초산 농도에 따라 0.263, 0.467, 0.476으로 측정되었다.
분배계수는 온도에 따른 함수이므로 모두 같은 값이 나와야하지만 실제로는 그렇지 않음을 보이고 있다. 분배계수에 대한 오차의 원인에는 여러 가지가 있을 수 있다. 첫 번째, 평형 상태에 있는 용액이 온도의 변화나 흔들림에 의하여 그 평형 상태가 깨져버려서 오차가 생겼을 수 있다. 두 번째, 정확한 기계가 아닌 피펫으로 용액을 옮겼기 때문에 시료의 정확한 양의 측정이 이루어지지 않아 이러한 오차가 생겼을 것이다. 세 번째, 용액으로 적정하는 과정에서 오차가 발생하였다. 적정을 할 때는 용액의 한 방울로도 변화가 크게 일어날 수 있으므로 정확하게 해야한다. 각 용액을 적정할 때마다 색깔의 진하기 정도가 달라서 이에 따른 오차도 있을 것으로 생각된다.
물로 에테르를 단일 추출한 결과 0.235(=0.235), 되풀이 추출한 결과는 0.102(=0.1
02)로 각각의 추출분율은 각각 53.0%, 79.6%로 단일 추출보다 되풀이 추출이 더 효율적이라는 것을 알 수 있다.
8. 기호(Nomenclature)
노르말 농도() : 용액 1 속에 녹아 있는 용질의 g당량수를 나타낸 농도를 말한다.
몰 농도() : 용액 1 속에 포함된 용질의 몰수를 용액의 부피로 나눈 값이다. 으로 표시한다.
: 산의 해리상수. 산의 세기를 나타내는 척도로 값이 클수록 이온화 경향이 크다.
: 에서의 초기농도.
: 전체 평형 농도.
: 두 용매 사이에서 분배되는 용질 분자의 농도.
: 의 용매 에테르 용액에서의 용질의 농도.
: 의 용매 물을 써서 단일추출 한 후 용매 에테르 용액에서 추출되지 않고 남은 용질의 농도.
9. 인용문헌(References)
이문득, 물리화학실험, 자유아카데미, 1997.
H.D. Crockford 외 3명, “물리화학실험”, 탐구당, 1997.
http://mbel.kaist.ac.kr/lecture/che201/2002-4.ppt.
추천자료
 용질사이의 용질분배와 분배계수
용질사이의 용질분배와 분배계수 [화공]응축 실험보고서
[화공]응축 실험보고서 2주_이성분 유기 혼합물계의 어는점 도표 작성
2주_이성분 유기 혼합물계의 어는점 도표 작성 순수물질 물질과 혼합물의 녹는점 측정
순수물질 물질과 혼합물의 녹는점 측정 어는점 내림을 통한 분자량 측정(예비+결과)
어는점 내림을 통한 분자량 측정(예비+결과) 1. Acetanilide의 재결정 (재결정 및 녹는점: Acetanilide의 재결정)
1. Acetanilide의 재결정 (재결정 및 녹는점: Acetanilide의 재결정) 어는점 내림 측정
어는점 내림 측정 (예비) 어는점 내림 측정 - 액의 어는점 내림을 이용하여 용질의 분자량을 결정한다
(예비) 어는점 내림 측정 - 액의 어는점 내림을 이용하여 용질의 분자량을 결정한다 [증기압, 증기압 정의, 증기압 측정, 헨리상수, 에탄올실험, 비활성 기체]증기압의 정의, 증...
[증기압, 증기압 정의, 증기압 측정, 헨리상수, 에탄올실험, 비활성 기체]증기압의 정의, 증... 일반화학실험 -알코올의 증류
일반화학실험 -알코올의 증류 Xylene(자일렌) 100만톤 생산 공정
Xylene(자일렌) 100만톤 생산 공정 단증류 실험
단증류 실험 녹음열- (예비+결과)보고서
녹음열- (예비+결과)보고서


































소개글