목차
CONTENTS ....................................................................Ⅰ
List ofTables ................................................Ⅱ
List of Figures .........................................Ⅱ
ABSTRACT .................................................Ⅲ
1.INTRODUCTION .........................................1
1.1.촉매 .....................................................1
1.1.1.촉매의 역사 ..........................................1
1.1.2.촉매의 정의 ........................................1
1.1.3.촉매의 특성 ...................................2
1.2.크로마토그래피 ...........................................4
1.2.1.크로마토그래피의 이용 .................................4
1.2.2.기체크로마토그래피 ............................5
1.2.3.기체크로마토그래피 칼럼 ..........................7
1.2.4.온도프로그래밍 ............................................8
1.2.5.정량분석 .....................................................8
1.3.실험목적 ...........................................9
2.EXPERIMENT ................................................10
2.1.실험기구 .................................................10
2.2.실험방법 ......................................................10
2.3.실험시 주의사항 ....................................10
3.RESULTS & DISCUSSION .....................................11
3.1.Raw data ...............................................11
3.2.Result .........................................13
3.3.Discussion ..............................................14
4.CONCLUSION ..................................................... 5.
REFERENCES ..............................................16
List ofTables ................................................Ⅱ
List of Figures .........................................Ⅱ
ABSTRACT .................................................Ⅲ
1.INTRODUCTION .........................................1
1.1.촉매 .....................................................1
1.1.1.촉매의 역사 ..........................................1
1.1.2.촉매의 정의 ........................................1
1.1.3.촉매의 특성 ...................................2
1.2.크로마토그래피 ...........................................4
1.2.1.크로마토그래피의 이용 .................................4
1.2.2.기체크로마토그래피 ............................5
1.2.3.기체크로마토그래피 칼럼 ..........................7
1.2.4.온도프로그래밍 ............................................8
1.2.5.정량분석 .....................................................8
1.3.실험목적 ...........................................9
2.EXPERIMENT ................................................10
2.1.실험기구 .................................................10
2.2.실험방법 ......................................................10
2.3.실험시 주의사항 ....................................10
3.RESULTS & DISCUSSION .....................................11
3.1.Raw data ...............................................11
3.2.Result .........................................13
3.3.Discussion ..............................................14
4.CONCLUSION ..................................................... 5.
REFERENCES ..............................................16
본문내용
끄고 빈 반응기의 히터를 켰다. 피크가 안정적으로 나올 때 까지 확인 한 후에 밸브 주입 작동을 하고 데이터를 수집 하였다. 데이터 수집 후 피크의 면적을 확인 하였다.
2.3. 실험 시 유의사항
- 실험 시 수소 기체가 발생하므로 주의한다.
- 반응기가 고온이므로 주의한다.
3. Results & Discussion
Table 2. Raw data
구분
촉매반응기
첫 번째
촉매반응기
두 번째
촉매반응기
세 번째
빈 반응기
적분면적값
0.002396
0.002486
0.002656
0.001469
적분면적값
0.0132
0.012925
0.0109
0.007603
적분면적값
0.06916
0.068389
0.066959
0.042583
농도(%)
13.265864
13.668387
14.420098
9.1139
농도(%)
20.385428
20.729759
20.373742
20.409052
농도(%)
26.512515
26.232912
25.713453
16.668589
유량값
(cc/min)
6.632932
6.834194
7.210049
4.55695
유량값
(cc/min)
10.192714
10.36488
10.186871
10.204526
유량값
(cc/min)
13.256258
13.116456
12.856727
8.334294
이론유량
(cc/min)
140
140
140
140
이론유량
(cc/min)
105
105
105
105
이론유량
(cc/min)
35
35
35
35
실제유량
(cc/min)
50
50
50
50
실제유량
(cc/min)
6.632932
6.834194
7.210049
4.55695
실제유량
(cc/min)
13.256258
13.116456
12.856727
8.334294
3.1. Raw data
Table 2 는 실험 결과 값을 나타내고 있다. 촉매 반응기에서의 데이터들은 비슷한 값들을 갖는 것을 확인할 수 있다. 또한 빈 반응기에서의 값은 촉매 반응기에서의 값보다 작아진 것을 확인할 수 있다. 수소 농도의 평균값은 13.8%, 일산화탄소 농도의 평균값은 20.5%, 이산화탄소 농도의 평균값은 26.2% 이다.
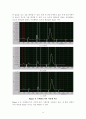
(a) 1번째
(b) 2번째
(c) 3번째
Figure 6. 촉매반응기의 시간대 피크
Figure 6 은 촉매반응기의 시간에 따른 그래프를 나타내고 있다. 세 번의 실험이 거의 비슷한 값들을 가지는 것을 확인할 수 있다.
Figure 7. 빈 반응기의 시간대 피크
Figure 7 은 빈 반응기의 시간에 따른 그래프이다. 촉매 반응기에서의 그래프와 피크의 시간은 비슷하지만 피크의 크기는 절반정도인 것을 확인할 수 있다.
3.2. Result
용질의 농도는 그래프 피크의 아래 면적에 비례한다. 또한 가벼운 기체일수록 먼저 피크를 보이게 된다. 메탄올과 물의 반응에서 생성되는 기체는 수소와 물 뿐만 아니라 일산화탄소, 이산화탄소, 메탄이 생성되게 된다.
촉매 반응기에서의 피크는 세 번의 반응 모두 비슷한 그래프를 얻었다. 이것을 빈 반응기의 그래프와 비교하여 보면 그래프 피크의 크기가 다른 것을 볼 수 있다. 촉매 반응기의 1번째 3번째 4번째 피크 크기보다 빈 반응기의 피크는 절반정도 낮아진 것을 확인할 수 있다. 이것은 면적이 줄어들었다고도 볼 수 있다. 면적값을 비교해 보면 약 40%~45%정도의 면적이 감소하였음을 알 수 있다. 이 결과를 통해 촉매반응기의 생성물질 농도가 빈 반응기의 생성물질 농도보다 크다고 볼 수 있다. 따라서 촉매는 정촉매이며 촉매반응기 에서의 생성물의 생성속도가 더 빠르다는 것을 알 수 있다.
또한 가벼운 기체일수록 먼저 빠져 나오게 되므로 첫 번째 피크는 분자량이 2 인 수소이며 2번째 피크는 분자량이 16인 메탄, 3번째 피크는 분자량이 28인 이산화탄소, 4번째 피크는 분자량이 44인 이산화탄소라는 것을 알 수 있다. 이론상으로는 메탄올이 반응하여 75% 수소와 25% 이산화탄소, 1%일산화탄소를 생성함을 알 수 있다. 하지만 실험 결과 촉매반응기와 빈 반응기 모두 이론값과는 다른 값을 나타내었다. 수소가 가장 적었고, 이산화탄소가 가장 많았다. 이렇게 이론값과 실제값이 차이가 나는 원인은 온도 및 압력의 변화, 촉매의 사용 등 반응할 때의 조건의 변화라고 생각된다.
3.3. Discussion
이번 실험은 촉매를 사용할 때와 촉매를 사용하지 않을 때의 반응정도를 비교해 보고 이론값과 실제 값을 비교해 보는 실험 이었다. 실험 그래프를 통하여 촉매를 사용할 때 반응 속도가 사용하지 않을 때 반응 속도보다 빠르다는 것을 알 수 있었다. 그러므로 촉매는 정촉매라는 것을 확인할 수 있었다. 또한 이론값과 실제값을 비교하여 보면 실제 값은 반응 조건을 어떻게 변화하느냐에 따라 다르게 나타난다는 것도 알 수 있었다.
4. Conclusion
이번 실험의 목적은 촉매층을 통과하는 반응과 촉매층을 통과하지 않는 반응을 비교하여 촉매의 역할을 알아보고 가스크로마토그래피를 통해서 실제 생성된 가스의 유량 및 농도와 이론적인 값을 통해 전환율을 알아보는 것이었다.
이번 실험을 통하여 가스크로마토그래피의 분석 방법과 기타 다른 크로마토그래피에 대해서도 알 수 있었다. 가스크로마토그래피의 전개용매 역할이 운반기체 즉, 케리어 가스라는 것도 알 수 있었고 케리어 가스와 칼럼의 변화에 따라서 반응 감도도 달라진다는 것도 알 수 있었다. 또한 촉매를 사용할 때 반응이 빠르다는 사실도 실험적으로 확인해 볼 수 있었다.
실험 결과 촉매를 사용할 때가 사용하지 않을 때 보다 반응 속도가 빠르다는 것을 확인해 볼 수 있었다. 또한 이론값과 실제값은 여러 변수들을 통하여 다르게 나타날 수 있다는 사실을 알 수 있었다.
컴퓨터 조작을 통하여 기기를 조작하고 반응을 실시간으로 관찰할 수 있었다.
5. REFERENCES
[1] H. Scott Fogler, "반응공학", 4판, PRENTICE HALL, 2006, p 709
[2] Daniel C. Harris, “최신분석화학”, 4판, 자유아카데미, 2009, p 487
[3] Gary D.Christian, “분석화학”, 6판, 자유아카데미, 2008, p 676
2.3. 실험 시 유의사항
- 실험 시 수소 기체가 발생하므로 주의한다.
- 반응기가 고온이므로 주의한다.
3. Results & Discussion
Table 2. Raw data
구분
촉매반응기
첫 번째
촉매반응기
두 번째
촉매반응기
세 번째
빈 반응기
적분면적값
0.002396
0.002486
0.002656
0.001469
적분면적값
0.0132
0.012925
0.0109
0.007603
적분면적값
0.06916
0.068389
0.066959
0.042583
농도(%)
13.265864
13.668387
14.420098
9.1139
농도(%)
20.385428
20.729759
20.373742
20.409052
농도(%)
26.512515
26.232912
25.713453
16.668589
유량값
(cc/min)
6.632932
6.834194
7.210049
4.55695
유량값
(cc/min)
10.192714
10.36488
10.186871
10.204526
유량값
(cc/min)
13.256258
13.116456
12.856727
8.334294
이론유량
(cc/min)
140
140
140
140
이론유량
(cc/min)
105
105
105
105
이론유량
(cc/min)
35
35
35
35
실제유량
(cc/min)
50
50
50
50
실제유량
(cc/min)
6.632932
6.834194
7.210049
4.55695
실제유량
(cc/min)
13.256258
13.116456
12.856727
8.334294
3.1. Raw data
Table 2 는 실험 결과 값을 나타내고 있다. 촉매 반응기에서의 데이터들은 비슷한 값들을 갖는 것을 확인할 수 있다. 또한 빈 반응기에서의 값은 촉매 반응기에서의 값보다 작아진 것을 확인할 수 있다. 수소 농도의 평균값은 13.8%, 일산화탄소 농도의 평균값은 20.5%, 이산화탄소 농도의 평균값은 26.2% 이다.
(a) 1번째
(b) 2번째
(c) 3번째
Figure 6. 촉매반응기의 시간대 피크
Figure 6 은 촉매반응기의 시간에 따른 그래프를 나타내고 있다. 세 번의 실험이 거의 비슷한 값들을 가지는 것을 확인할 수 있다.
Figure 7. 빈 반응기의 시간대 피크
Figure 7 은 빈 반응기의 시간에 따른 그래프이다. 촉매 반응기에서의 그래프와 피크의 시간은 비슷하지만 피크의 크기는 절반정도인 것을 확인할 수 있다.
3.2. Result
용질의 농도는 그래프 피크의 아래 면적에 비례한다. 또한 가벼운 기체일수록 먼저 피크를 보이게 된다. 메탄올과 물의 반응에서 생성되는 기체는 수소와 물 뿐만 아니라 일산화탄소, 이산화탄소, 메탄이 생성되게 된다.
촉매 반응기에서의 피크는 세 번의 반응 모두 비슷한 그래프를 얻었다. 이것을 빈 반응기의 그래프와 비교하여 보면 그래프 피크의 크기가 다른 것을 볼 수 있다. 촉매 반응기의 1번째 3번째 4번째 피크 크기보다 빈 반응기의 피크는 절반정도 낮아진 것을 확인할 수 있다. 이것은 면적이 줄어들었다고도 볼 수 있다. 면적값을 비교해 보면 약 40%~45%정도의 면적이 감소하였음을 알 수 있다. 이 결과를 통해 촉매반응기의 생성물질 농도가 빈 반응기의 생성물질 농도보다 크다고 볼 수 있다. 따라서 촉매는 정촉매이며 촉매반응기 에서의 생성물의 생성속도가 더 빠르다는 것을 알 수 있다.
또한 가벼운 기체일수록 먼저 빠져 나오게 되므로 첫 번째 피크는 분자량이 2 인 수소이며 2번째 피크는 분자량이 16인 메탄, 3번째 피크는 분자량이 28인 이산화탄소, 4번째 피크는 분자량이 44인 이산화탄소라는 것을 알 수 있다. 이론상으로는 메탄올이 반응하여 75% 수소와 25% 이산화탄소, 1%일산화탄소를 생성함을 알 수 있다. 하지만 실험 결과 촉매반응기와 빈 반응기 모두 이론값과는 다른 값을 나타내었다. 수소가 가장 적었고, 이산화탄소가 가장 많았다. 이렇게 이론값과 실제값이 차이가 나는 원인은 온도 및 압력의 변화, 촉매의 사용 등 반응할 때의 조건의 변화라고 생각된다.
3.3. Discussion
이번 실험은 촉매를 사용할 때와 촉매를 사용하지 않을 때의 반응정도를 비교해 보고 이론값과 실제 값을 비교해 보는 실험 이었다. 실험 그래프를 통하여 촉매를 사용할 때 반응 속도가 사용하지 않을 때 반응 속도보다 빠르다는 것을 알 수 있었다. 그러므로 촉매는 정촉매라는 것을 확인할 수 있었다. 또한 이론값과 실제값을 비교하여 보면 실제 값은 반응 조건을 어떻게 변화하느냐에 따라 다르게 나타난다는 것도 알 수 있었다.
4. Conclusion
이번 실험의 목적은 촉매층을 통과하는 반응과 촉매층을 통과하지 않는 반응을 비교하여 촉매의 역할을 알아보고 가스크로마토그래피를 통해서 실제 생성된 가스의 유량 및 농도와 이론적인 값을 통해 전환율을 알아보는 것이었다.
이번 실험을 통하여 가스크로마토그래피의 분석 방법과 기타 다른 크로마토그래피에 대해서도 알 수 있었다. 가스크로마토그래피의 전개용매 역할이 운반기체 즉, 케리어 가스라는 것도 알 수 있었고 케리어 가스와 칼럼의 변화에 따라서 반응 감도도 달라진다는 것도 알 수 있었다. 또한 촉매를 사용할 때 반응이 빠르다는 사실도 실험적으로 확인해 볼 수 있었다.
실험 결과 촉매를 사용할 때가 사용하지 않을 때 보다 반응 속도가 빠르다는 것을 확인해 볼 수 있었다. 또한 이론값과 실제값은 여러 변수들을 통하여 다르게 나타날 수 있다는 사실을 알 수 있었다.
컴퓨터 조작을 통하여 기기를 조작하고 반응을 실시간으로 관찰할 수 있었다.
5. REFERENCES
[1] H. Scott Fogler, "반응공학", 4판, PRENTICE HALL, 2006, p 709
[2] Daniel C. Harris, “최신분석화학”, 4판, 자유아카데미, 2009, p 487
[3] Gary D.Christian, “분석화학”, 6판, 자유아카데미, 2008, p 676
추천자료
 [화학공학실험]산화-환원 적정 실험 프레젠테이션 자료
[화학공학실험]산화-환원 적정 실험 프레젠테이션 자료 [화학공학기초실험] 2. 추출
[화학공학기초실험] 2. 추출 [화학공학기초실험] 3.초산에틸의 비누화 반응
[화학공학기초실험] 3.초산에틸의 비누화 반응 [화학공학실험]액체의 밀도 실험 결과레포트
[화학공학실험]액체의 밀도 실험 결과레포트 [화학실험] 친핵성 치환반응 결과보고서
[화학실험] 친핵성 치환반응 결과보고서  화학적 산소요구량(COD) 측정연혁, 화학적 산소요구량(COD) 실험기구와 시약, 화학적 산소요...
화학적 산소요구량(COD) 측정연혁, 화학적 산소요구량(COD) 실험기구와 시약, 화학적 산소요... [화학공학실험] 혼합조 실험 (예비+결과레포트)
[화학공학실험] 혼합조 실험 (예비+결과레포트) [화학반응실험][화학반응]화학반응 사례1(대사), 화학반응 사례2(색변화), 화학반응 사례3(정...
[화학반응실험][화학반응]화학반응 사례1(대사), 화학반응 사례2(색변화), 화학반응 사례3(정... 화공기사 실기 작업형 행동요령
화공기사 실기 작업형 행동요령 [단위실험] 레이놀즈 실험[Reynolds Number]
[단위실험] 레이놀즈 실험[Reynolds Number] 화학공학 실험 - 열풍온도제어
화학공학 실험 - 열풍온도제어 화학공학 기초 실험 - (결과) 염색 실험
화학공학 기초 실험 - (결과) 염색 실험 [화학실험] 나일론의 제조 : 분자 말단에 아민(-NH2)기와 카르복시(-COOH)기를 갖고 있는 서...
[화학실험] 나일론의 제조 : 분자 말단에 아민(-NH2)기와 카르복시(-COOH)기를 갖고 있는 서... 아세트아닐라이드(Acetanilide) : 아세틸화 반응을 이용하여 여러가지 합성의 중간체로 사용...
아세트아닐라이드(Acetanilide) : 아세틸화 반응을 이용하여 여러가지 합성의 중간체로 사용...