목차
1. 다른 종류의 점도 측정방법
2. 실험 결과 분석
3. 오차분석
<참조>
2. 실험 결과 분석
3. 오차분석
<참조>
본문내용
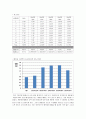
100%)의 경우 물과 혼합되게 되면 물과 에탄올 사이의 수소결합이 증가하여
점도가 점점 더 높아지게 된다. 그러나 에탄올의 농도가 약 60%를 기점으로 농도가 낮아질수록 점도도 감소하게 된다. 이는 이론상으로 에탄올이 60%일 때 물과의 가장 많은 수소결합을 한다고 알려져 있기 때문이다. 점도는 분자간의 응집력에 의하여 결정되는데 물과 에탄올의 경우는 수소결합이 분자간의 응집력에 가장 큰 영향을 준다. 그러므로 수소결합의 수가 용액의 점도와 비례관계로 볼 수 있다. 실제 실험에서 60%의 농도에 따른 점도를 측정하지 못하였지만 실험결과를 토대로 보면 50~75%에서 가장 높은 점도를 나타냈으므로 실제 이론적인 측면과 어느 정도 일치한다고 볼 수 있다.
3. 오차분석
표준 물 25도에서의 점도는 0.894cP이다. 그러므로 실험값과 비교했을 때 오차율은 다음과 같다.
그리고 에탄올(100%)의 경우에는 1.074cP이다. 에탄올의 경우 95%와 비교해 보았을 때 오차율은 다음과 같다.
이 경우, 실험값을 알코올 95%로 한 점에서 오차가 더 크게 발생했다.
오차의 원인으로는, 제일 먼저 혼합액을 제조하는 과정에서, 에탄올과 물의 비율을 맞출 때 실험에서 요구하는 양을 피펫으로 맞추는데 한계가 있었고, 실험을 하는 동안 용액의 온도가 항상 일정하게 유지되지 않고, 조금의 차이가 오차를 발생하게 하는 요인이 되었다. 또한 혼합액의 흐름에 따라 스톱워치를 이용해 시간을 측정할 때, 눈으로 시작점을 체크하고, 손으로 스톱워치를 누르기 때문에 용액이 정확하게 흐른 시간을 알 수 없었다. 그리고 실험실의 환경이나, 매 실험을 할 때 마다 변하는 환경 인자를 고려하지 않아 오차가 발생했다.
고찰
이번 실험을 통해서 에탄올의 농도에 따른 점도가 어떻게 바뀌는지 알 수 있었다. 특히 점도가 계속 증가하다가, 에탄올의 농도가 높을 때 다시 점도가 내려가는 현상이 새로웠다. 이러한 현상의 원인이 에탄올과 물의 수소결합이라는 사실을 보고서를 쓰면서 새롭게 알게되었다.
하지만 이번 실험도 다른 실험들과 마찬가지로 여러 가지 오차를 유발하는 요소들에 신경을 썼으나, 오차가 크게 발생한 점이 아쉬웠고, 또한 에탄올의 조성에 따른 표준 점성값들을 찾지 못해서 오차율을 분석하지 못한 것이 안타까웠다.
<참조>
http://blog.naver.com/gydnsdl0409?Redirect=Log&logNo=90134897204
점도 측정 결과 분석 [네이버 블로그 - 리아의 여행이야기]
http://www.cheric.org/education/prop/visc.pdf
다양한 점도측정 방법 [화학공학연구 정보센터 - http://www.cheric.org/]
http://medi.nvrqs.go.kr/homep/process/file/1079/1133_make.html
다양한 점도측정 방법 [농림수산검역검사 본부 - http://medi.qia.go.kr/]
http://en.wikipedia.org/wiki/Viscosity
에탄올과 물의 표준점도 값 [위키백과]
점도가 점점 더 높아지게 된다. 그러나 에탄올의 농도가 약 60%를 기점으로 농도가 낮아질수록 점도도 감소하게 된다. 이는 이론상으로 에탄올이 60%일 때 물과의 가장 많은 수소결합을 한다고 알려져 있기 때문이다. 점도는 분자간의 응집력에 의하여 결정되는데 물과 에탄올의 경우는 수소결합이 분자간의 응집력에 가장 큰 영향을 준다. 그러므로 수소결합의 수가 용액의 점도와 비례관계로 볼 수 있다. 실제 실험에서 60%의 농도에 따른 점도를 측정하지 못하였지만 실험결과를 토대로 보면 50~75%에서 가장 높은 점도를 나타냈으므로 실제 이론적인 측면과 어느 정도 일치한다고 볼 수 있다.
3. 오차분석
표준 물 25도에서의 점도는 0.894cP이다. 그러므로 실험값과 비교했을 때 오차율은 다음과 같다.
그리고 에탄올(100%)의 경우에는 1.074cP이다. 에탄올의 경우 95%와 비교해 보았을 때 오차율은 다음과 같다.
이 경우, 실험값을 알코올 95%로 한 점에서 오차가 더 크게 발생했다.
오차의 원인으로는, 제일 먼저 혼합액을 제조하는 과정에서, 에탄올과 물의 비율을 맞출 때 실험에서 요구하는 양을 피펫으로 맞추는데 한계가 있었고, 실험을 하는 동안 용액의 온도가 항상 일정하게 유지되지 않고, 조금의 차이가 오차를 발생하게 하는 요인이 되었다. 또한 혼합액의 흐름에 따라 스톱워치를 이용해 시간을 측정할 때, 눈으로 시작점을 체크하고, 손으로 스톱워치를 누르기 때문에 용액이 정확하게 흐른 시간을 알 수 없었다. 그리고 실험실의 환경이나, 매 실험을 할 때 마다 변하는 환경 인자를 고려하지 않아 오차가 발생했다.
고찰
이번 실험을 통해서 에탄올의 농도에 따른 점도가 어떻게 바뀌는지 알 수 있었다. 특히 점도가 계속 증가하다가, 에탄올의 농도가 높을 때 다시 점도가 내려가는 현상이 새로웠다. 이러한 현상의 원인이 에탄올과 물의 수소결합이라는 사실을 보고서를 쓰면서 새롭게 알게되었다.
하지만 이번 실험도 다른 실험들과 마찬가지로 여러 가지 오차를 유발하는 요소들에 신경을 썼으나, 오차가 크게 발생한 점이 아쉬웠고, 또한 에탄올의 조성에 따른 표준 점성값들을 찾지 못해서 오차율을 분석하지 못한 것이 안타까웠다.
<참조>
http://blog.naver.com/gydnsdl0409?Redirect=Log&logNo=90134897204
점도 측정 결과 분석 [네이버 블로그 - 리아의 여행이야기]
http://www.cheric.org/education/prop/visc.pdf
다양한 점도측정 방법 [화학공학연구 정보센터 - http://www.cheric.org/]
http://medi.nvrqs.go.kr/homep/process/file/1079/1133_make.html
다양한 점도측정 방법 [농림수산검역검사 본부 - http://medi.qia.go.kr/]
http://en.wikipedia.org/wiki/Viscosity
에탄올과 물의 표준점도 값 [위키백과]
추천자료
 액체의 굴절률 측정
액체의 굴절률 측정 일반화학 및 실험 - 용해열과 과냉각 상태 예비, 결과 리포트
일반화학 및 실험 - 용해열과 과냉각 상태 예비, 결과 리포트 과잉 부피
과잉 부피 생활속화학 술
생활속화학 술 Biodiesel 생성을 통한 Trans-Esterification 촉매반응에 관련된 결과보고서
Biodiesel 생성을 통한 Trans-Esterification 촉매반응에 관련된 결과보고서 페놀과 알코올의 비교, 에테르(Ether)의 물리적 성질
페놀과 알코올의 비교, 에테르(Ether)의 물리적 성질 알코올의 증류 (일반화학 실험보고서)
알코올의 증류 (일반화학 실험보고서) 알코올의 증류 (일반화학 실험보고서)
알코올의 증류 (일반화학 실험보고서) 물질의 합성 - 치환반응
물질의 합성 - 치환반응 일반화학실험 비누만들기(결과)_박현지
일반화학실험 비누만들기(결과)_박현지 [일반화학실험] 알코올의 증류
[일반화학실험] 알코올의 증류 화학공학 - Reduction of chlorobenzaldehyde with NaBH4 [유기합성]
화학공학 - Reduction of chlorobenzaldehyde with NaBH4 [유기합성] Sol-Gel법에 의한 SiO2 Gel 제조 실험(결과레포트)
Sol-Gel법에 의한 SiO2 Gel 제조 실험(결과레포트) 3.단증류 (결과)
3.단증류 (결과)




























소개글