|
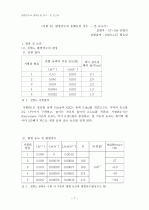
서 칼슘이온이 침전되는 역반응이 일어난다. 결과적으로 농도가 더 높은 수산화나트륨 용액일 수록 더 적은 칼슘 이온 농도를 보였다.
3). 각 용액에서의 용해도곱을 비교하고, 용해도곱이 상수임을 알아보자. 실험에서 얻은 값과 문헌에서 조
|
- 페이지 7페이지
- 가격 1,200원
- 등록일 2009.10.09
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
수산화칼슘 고체를 과량을 넣고, 10분간 잘 저어서 평형에 도달하도록 한다.
4). 각 비커의 용액을 뷰흐너 깔때기를 이용해서 감압하여 거르고, 거른 액을 각각 따로 비커에 보관한다. 이 때, 거른 액이 묽히지 말고, 각 용액의 온도를 기록한다.
|
- 페이지 5페이지
- 가격 1,000원
- 등록일 2009.10.09
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
수산화칼슘을 반 숟가락 정도를 퍼서 물에 녹인다고 적혀있었는데 반 숟가락이 어느 정도 인지 정확하게 몰라서 대략 어림잡아 넣었다. 그래서인지 각각의 비커에 수산화칼슘을 넣고 유리막대로 저었을 때 어떤 것은 조금 진한 흰색이었고
|
- 페이지 6페이지
- 가격 1,300원
- 등록일 2014.02.06
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
수산화 이온
1) ① NaOH → Na+ + OH-
2) 염기의 공통성과 특이성
3) 염기의 세기
[3] 중요한 염기
1) 수산화나트륨(NaOH) - 양잿물
2) Ca(OH)2 - 수산화칼슘(소석회)
3) NH3(암모니아) - 약한염기
▲ 루이스의 산과 염기
●산 (酸, Acid)
● 염
|
- 페이지 13페이지
- 가격 2,000원
- 등록일 2009.07.15
- 파일종류 한글(hwp)
- 참고문헌 없음
- 최근 2주 판매 이력 없음
|

|
는 낮아지고, 그럼에따라 전체적인 가성화율이 증가되는 것이다. 데이터시트에서도 시간이 지남에따라 가성화율이 증가하는 것을 볼 수 있다. 또 실험 초기에 수산화칼슘 용액과 탄산나트륨 용액을 석어서 끓여주었는데 탄산나트륨의 용해
|
- 페이지 7페이지
- 가격 500원
- 등록일 2004.05.23
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|