목차
1. 실험 날짜
2. 실험 제목
3. 실험 목표
4. 실험 이론
5. 실험 기구 및 시약
6. 실험 방법
7. 실험결과
8. 고찰
9. 참고 문헌
2. 실험 제목
3. 실험 목표
4. 실험 이론
5. 실험 기구 및 시약
6. 실험 방법
7. 실험결과
8. 고찰
9. 참고 문헌
본문내용
570
50
120
78
600
48
150
78
630
46
180
78
660
44
210
77
690
43
240
75
720
42
270
74
750
41
300
71
780
39
330
69
810
37
360
66
840
36
390
64
870
35
420
61
900
34
450
59
930
34
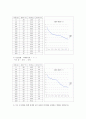
- 추정되는 어는 점 = 78°C
2) 나프탈렌 : 디페닐아민 = 3 : 7
어는 점 = 66°C , 44°C
시간(초)
온도(°C)
시간(초)
온도(°C)
0
80
480
38
30
75
510
37
60
73
540
36
90
70
570
35
120
66
600
34
150
64
630
33
180
58
660
32
210
56
690
31.8
240
54
720
30.8
270
46
750
30
300
44
780
29
330
44
810
29
360
42
840
28
390
40
870
28
420
40
900
28
450
38
930
3) 나프탈렌 : 디페닐아민 = 5 : 5
어는 점 = 52°C , 47°C
시간(초)
온도(°C)
시간(초)
온도(°C)
0
80
480
47
30
72
510
47
60
67
540
46
90
64
570
46
120
61
600
45
150
58
630
44
180
56
660
43
210
54
690
41
240
52
720
39
270
52
750
38
300
51
780
37
330
51
810
36
360
49
840
35
390
48
870
34
420
48
900
33
450
47
930
4) 나프탈렌 : 디페닐아민 = 7 : 3
- 어는 점 = 66°C , 60°C
시간(초)
온도(°C)
시간(초)
온도(°C)
0
80
480
51
30
78
510
48
60
72
540
45
90
68
570
42
120
67
600
40
150
66
630
38
180
66
660
36
210
64
690
34
240
62
720
34
270
61
750
33
300
60
780
32
330
60
810
31
360
60
840
31
390
60
870
30
420
58
900
30
450
55
930
5) 어는 점 내림을 통해 용매에 녹인 용질의 분자량을 결정하는 방법을 설명하시오.
ⓐ 유도 (어는 점 내림 상수 = , 몰랄농도 = , 용매의 질량 = , 용질의 질량 = , 용질의 분자량 = )
용액의 끓는 점 오름이나 어는 점 내림을 이용하면 용액 속에 녹아있는 용질의 분자량을 구할 수 있다. 어떤 용매 g에 분자량이 인 용질 g이 녹아있는 용액의 끓는 점 내림을 라하고 이 용매의 몰랄 오름 상수를 라고 가정한다. 몰랄농도은 용매 1000g속에 녹아 있는 용질의 몰수이므로 와 같다. 따라서 을 이용하여 용질의 분자량을 구할 수 있다.
ⓑ 나프탈렌 : 디페닐아민 = 3 : 7 일 때, 디페닐아민의 분자량= g/mol
식= = = 1322,2 g/mol
ⓒ 나프탈렌 : 디페닐아민 = 5 : 5 일 때, 디페닐아민의 분자량= g/mol
식= = = 261.5 g/mol
ⓓ 나프탈렌 : 디페닐아민 = 7 : 3 일 때, 디페닐아민의 분자량= g/mol
식= = = 182.1 g/mol
고찰: 이번 실험은 용액의 어는 점 내림을 시간에 따른 온도를 측정하여 냉각 곡선을 통해 알아보는 실험이었다. 측덩한 데이터를 바탕으로 냉각곡선을 그리고 냉각곡선의 기울기가 일정해지는 구간 즉 어는 점을 알아보는 것이다. 또한 어는 점 내림 현상을 통해 용질의 분자량을 결정했다. 실험을 하기 전에 가장 중요한 것은 실험에 대한 배경을 알고 어는점 내림이 어떤 것인지 정확히 아는 것이라고 생각한다. 실험을 통해 용액의 총괄성이 물질의 종류와는 상관없이 용질의 입자의 수에 의해서만 결정된다는 말을 이해할 수 있었다. 또한 이 실험에서 오차가 발생할 수 있는 원인은 나프탈렌을 물중탕 장치에 넣고 가열할 때 온도를 제대로 맞추지 않는다면 오차가 발생할 수 있다. 온도를 맞추고 30초 간격으로 계속온도를 재야한다. 이 과정에서는 물중탕을 통해 가열하는 과정인 만큼 안전에 주의하고 실험 결과를 빠른 시간 내에 적는 것이 오차를 줄일 수 있을 뿐만아니라 안전한 방법이다. 가열한 후 시험관의 물기를 제거하고 빈비커로 담는 이유는 대류현상을 방지하기 위해서이다. 이 과정이 잘 되지 않는 다면 공기의 대류현상으로 인한 오차가 발생할 수 있을 것이다. 이러한 과정을 처음에는 순수한 나프탈렌으로만 했다면 나프탈렌과 디페닐아민의 비율을 3:7, 5:5, 7:3 으로 바꾸어가며 실험을 계속한다. 실험 과정도 중요하지만 비율에 따른 시료의 무게를 정확하게 재야한다. 그 결과 순수한 나프탈렌의 어는 점, 나프탈렌과 디페닐아민의 어는점을 구할 수 있었다. 나프탈렌과 디페닐아민의 어는 점을 2개 구한 이유는 어는점 2개를 구하는 이유는 나프탈렌과 디페닐아민의 각각의 어는점이 내려갔다고 판단하기 때문이다. 이러한 이유로 각각의 어는점을 구할 수 있었다. 마지막으로 용액의 어는점 내림을 이용하여 용질의 분자량을 구하는 과정에서 어떤 것이 용매인지 용질인지 확실히 구분하여야 한다. 분자량을 계산할 때 용매를 나프탈렌으로 가정해야 디페닐아민의 분자량을 구할 수 있다. 실제 디페닐아민의 분자량은 169.23로 실험 결과와 오차가 조금 있다. 여러 오차의 원인이 있지만 이 실험에서 나프탈렌과 디페닐아민의 비율을 정확히 계산하는 것, 30초마다 정확히 온도를 재는 것, 실험의 정확도를 높이기 위한 반복적인 실험을 통해 오차를 줄일 수 있을 것이다. 더 정확한 실험 결과를 위해 마지막으로 실험결과를 점검하고 그 과정에서 잘못된 것이 있지 않았나 확인하는 것 또한 더 나은 결과 도출에 중요하다.
참고 문헌:
실험 이론: 네이버 지식 백과 화학 백과 어는 점 검색
실험 이론: 네이버 지식 백과 두산 백과 용액의 총괄성 검색
실험 이론: 네이버 지식 백과 두산 백과 끓는 점 오름 검색
실험 이론: 네이버 지식 백과 화학 물질 구조 사전 디페닐아민 검색
실험 이론: <줌달의 일반화학> 화학교재 연구회
실험 방법: 단국대학교 출반부 (공학용) <대학 화학실험법> 대학화학실험법 편찬위원회
50
120
78
600
48
150
78
630
46
180
78
660
44
210
77
690
43
240
75
720
42
270
74
750
41
300
71
780
39
330
69
810
37
360
66
840
36
390
64
870
35
420
61
900
34
450
59
930
34
- 추정되는 어는 점 = 78°C
2) 나프탈렌 : 디페닐아민 = 3 : 7
어는 점 = 66°C , 44°C
시간(초)
온도(°C)
시간(초)
온도(°C)
0
80
480
38
30
75
510
37
60
73
540
36
90
70
570
35
120
66
600
34
150
64
630
33
180
58
660
32
210
56
690
31.8
240
54
720
30.8
270
46
750
30
300
44
780
29
330
44
810
29
360
42
840
28
390
40
870
28
420
40
900
28
450
38
930
3) 나프탈렌 : 디페닐아민 = 5 : 5
어는 점 = 52°C , 47°C
시간(초)
온도(°C)
시간(초)
온도(°C)
0
80
480
47
30
72
510
47
60
67
540
46
90
64
570
46
120
61
600
45
150
58
630
44
180
56
660
43
210
54
690
41
240
52
720
39
270
52
750
38
300
51
780
37
330
51
810
36
360
49
840
35
390
48
870
34
420
48
900
33
450
47
930
4) 나프탈렌 : 디페닐아민 = 7 : 3
- 어는 점 = 66°C , 60°C
시간(초)
온도(°C)
시간(초)
온도(°C)
0
80
480
51
30
78
510
48
60
72
540
45
90
68
570
42
120
67
600
40
150
66
630
38
180
66
660
36
210
64
690
34
240
62
720
34
270
61
750
33
300
60
780
32
330
60
810
31
360
60
840
31
390
60
870
30
420
58
900
30
450
55
930
5) 어는 점 내림을 통해 용매에 녹인 용질의 분자량을 결정하는 방법을 설명하시오.
ⓐ 유도 (어는 점 내림 상수 = , 몰랄농도 = , 용매의 질량 = , 용질의 질량 = , 용질의 분자량 = )
용액의 끓는 점 오름이나 어는 점 내림을 이용하면 용액 속에 녹아있는 용질의 분자량을 구할 수 있다. 어떤 용매 g에 분자량이 인 용질 g이 녹아있는 용액의 끓는 점 내림을 라하고 이 용매의 몰랄 오름 상수를 라고 가정한다. 몰랄농도은 용매 1000g속에 녹아 있는 용질의 몰수이므로 와 같다. 따라서 을 이용하여 용질의 분자량을 구할 수 있다.
ⓑ 나프탈렌 : 디페닐아민 = 3 : 7 일 때, 디페닐아민의 분자량= g/mol
식= = = 1322,2 g/mol
ⓒ 나프탈렌 : 디페닐아민 = 5 : 5 일 때, 디페닐아민의 분자량= g/mol
식= = = 261.5 g/mol
ⓓ 나프탈렌 : 디페닐아민 = 7 : 3 일 때, 디페닐아민의 분자량= g/mol
식= = = 182.1 g/mol
고찰: 이번 실험은 용액의 어는 점 내림을 시간에 따른 온도를 측정하여 냉각 곡선을 통해 알아보는 실험이었다. 측덩한 데이터를 바탕으로 냉각곡선을 그리고 냉각곡선의 기울기가 일정해지는 구간 즉 어는 점을 알아보는 것이다. 또한 어는 점 내림 현상을 통해 용질의 분자량을 결정했다. 실험을 하기 전에 가장 중요한 것은 실험에 대한 배경을 알고 어는점 내림이 어떤 것인지 정확히 아는 것이라고 생각한다. 실험을 통해 용액의 총괄성이 물질의 종류와는 상관없이 용질의 입자의 수에 의해서만 결정된다는 말을 이해할 수 있었다. 또한 이 실험에서 오차가 발생할 수 있는 원인은 나프탈렌을 물중탕 장치에 넣고 가열할 때 온도를 제대로 맞추지 않는다면 오차가 발생할 수 있다. 온도를 맞추고 30초 간격으로 계속온도를 재야한다. 이 과정에서는 물중탕을 통해 가열하는 과정인 만큼 안전에 주의하고 실험 결과를 빠른 시간 내에 적는 것이 오차를 줄일 수 있을 뿐만아니라 안전한 방법이다. 가열한 후 시험관의 물기를 제거하고 빈비커로 담는 이유는 대류현상을 방지하기 위해서이다. 이 과정이 잘 되지 않는 다면 공기의 대류현상으로 인한 오차가 발생할 수 있을 것이다. 이러한 과정을 처음에는 순수한 나프탈렌으로만 했다면 나프탈렌과 디페닐아민의 비율을 3:7, 5:5, 7:3 으로 바꾸어가며 실험을 계속한다. 실험 과정도 중요하지만 비율에 따른 시료의 무게를 정확하게 재야한다. 그 결과 순수한 나프탈렌의 어는 점, 나프탈렌과 디페닐아민의 어는점을 구할 수 있었다. 나프탈렌과 디페닐아민의 어는 점을 2개 구한 이유는 어는점 2개를 구하는 이유는 나프탈렌과 디페닐아민의 각각의 어는점이 내려갔다고 판단하기 때문이다. 이러한 이유로 각각의 어는점을 구할 수 있었다. 마지막으로 용액의 어는점 내림을 이용하여 용질의 분자량을 구하는 과정에서 어떤 것이 용매인지 용질인지 확실히 구분하여야 한다. 분자량을 계산할 때 용매를 나프탈렌으로 가정해야 디페닐아민의 분자량을 구할 수 있다. 실제 디페닐아민의 분자량은 169.23로 실험 결과와 오차가 조금 있다. 여러 오차의 원인이 있지만 이 실험에서 나프탈렌과 디페닐아민의 비율을 정확히 계산하는 것, 30초마다 정확히 온도를 재는 것, 실험의 정확도를 높이기 위한 반복적인 실험을 통해 오차를 줄일 수 있을 것이다. 더 정확한 실험 결과를 위해 마지막으로 실험결과를 점검하고 그 과정에서 잘못된 것이 있지 않았나 확인하는 것 또한 더 나은 결과 도출에 중요하다.
참고 문헌:
실험 이론: 네이버 지식 백과 화학 백과 어는 점 검색
실험 이론: 네이버 지식 백과 두산 백과 용액의 총괄성 검색
실험 이론: 네이버 지식 백과 두산 백과 끓는 점 오름 검색
실험 이론: 네이버 지식 백과 화학 물질 구조 사전 디페닐아민 검색
실험 이론: <줌달의 일반화학> 화학교재 연구회
실험 방법: 단국대학교 출반부 (공학용) <대학 화학실험법> 대학화학실험법 편찬위원회































소개글