목차
1. Introduction
2. Theory
(1) Basic properties of species
(2) VLE (Vapor-Liquid Equilibrium)
(3) Activity coefficient
(4) Various models
1) Margules
2) van Laar
※국부 조성 모델 (local composition model)
3) Wilson
4) NRTL
5) UNIFAC Method
3. Procedure/Result
(1) VLE analysis
1) Raoult's law
2) Various models
① Margules
② van Laar
③ Wilson
④ NRTL
⑤ UNIFAC Method
(2) Consistency test
(3) 혼합 물성 변화
4. Discussion
① 코딩으로 인한 문제점
그래프의 해석
에 대한 해석
5. Conclusion
6. Reference & Coding
2. Theory
(1) Basic properties of species
(2) VLE (Vapor-Liquid Equilibrium)
(3) Activity coefficient
(4) Various models
1) Margules
2) van Laar
※국부 조성 모델 (local composition model)
3) Wilson
4) NRTL
5) UNIFAC Method
3. Procedure/Result
(1) VLE analysis
1) Raoult's law
2) Various models
① Margules
② van Laar
③ Wilson
④ NRTL
⑤ UNIFAC Method
(2) Consistency test
(3) 혼합 물성 변화
4. Discussion
① 코딩으로 인한 문제점
그래프의 해석
에 대한 해석
5. Conclusion
6. Reference & Coding
본문내용
잘못된 코딩으로 인해 결과가 틀리게 나온 것으로 해석을 했었지만, 코딩에는 아무런 문제가 없었다. 오히려 보다 정확한 증거자료로 우리가 사용하고 있는 교제 \"Introduction to Chemical Engineering Thermodynamics\", Smith, Page 420, Fig. 11.4
에서도 유사한 결론이 나와 있다는 것을 알 수 있었다.
위 그림에서 나타내듯이, Ethanol/Water의 경우에도 같은 결론이 나온다는 것을 확인할 수 있었다. 우리 조는 이러한 현상을 어떻게 해석을 할 것인가에 대해서 고민을 해보고, 다른 자료들의 조사를 통해서 합당한 결론을 토출해 내었다.
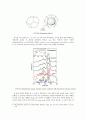
지난 40년간 이러한 현상을 Hydrophobic Effect로 설명하였다고 한다. Hydrophobic Effect란 다음 그림에서 볼 수 있듯이 물에 어떠한 용질을 섞을 경우, 물 분자들이 용질을 둘러싸는 현상을 말한다. 물 분자들은 Intermolecular Hydrogen Bonding을 통해서 물에 넣는 다른 용질을 둘러싸게 되고, 이러한 현상은 용질 분자로 하여금 어떠한 정렬, 혹은 구속을 하게 되므로 를 감소하게 만든다. 다만, 분자들은 매우 빠른 속도로 구조를 바꾸기도 하고 움직이기 때문에 Hydrophobic Effect만으로는 명확히 현상을 설명할 수 없었다.
하지만 지난 2003년, J. H. Guo \"The Molecular Structure of Alcohol-Water Mixtures\", Phys. Rev. Lett. 91, 157401 (2003), J. H. Guo, et al.
외 여러 명의 과학자들로 구성된 팀에 의해 정확한 실험결과를 토대로 이 현상을 설명하게 되었다. Guo 팀은 이번에 우리가 사용한 Methanol/Water at 298.15K를 전제로 Oxygen X-ray absorption과 selectively excited X-ray emission spectroscopy를 연구하였고 다음과 같은 결과를 획득하였다.
위 결과 자료를 통해서 알 수 있듯이, 실험적으로 구한 데이터 값은 ring과 chain 구조의 혼합체, 그 중에서도 대부분이 6이나 8로 구성되었다는 결론에 도달하게 된다. 물을 메탄올과 섞을 경우 많은 메탄올 chain이 물 분자와 수소결합을 이루게 된다. 이러한 결합은 어느 정도의 길이를 이루게 되면 굽어져서 open-ring 구조를 이루게 되는데, 이 구조가 매우 안정하기 때문에 의 값이 감소하게 되는 것이다.
즉, microscopic한 관점에서 물과 메탄올이 섞이는 과정을 살펴보면 완전하지 않으며, 아무리 오래나 시간이 지나더라도 완전해 지지 못한 다는 것을 알 수 있다.
다만 이러한 구조를 가지는 것은 실험적으로도 알 수 있듯이 매우 극소수이며, 열역학 제 2법칙을 위반하지 않기 위해서 이러한 구조를 가지는 것에 대해서 분자들이 스스로 저항하기 때문에, 비록 값은 작지만 양수의 값을 가지게 되는 것이다.
이때까지 이번 Term Project를 통해서 얻은 새로운 결과들에 대해서 살펴보았다. 이러한 결과들을 토론을 통해서 생각해 보고, 토출하게 됨으로서 열역학을 해석하며 이해하는데 더욱더 도움이 되는 시간이 되었다고 생각된다.
5. Conclusion
이번 프로젝트를 통해서 우리는 크게 세 가지를 얻게 되었다.
첫 째, VLE binary system을 우리가 친근한 물질로 적용해 봄으로서 그 현상을 직접 이해하는 시간이 되었다. 이론적으로만 배우던 그래프나 공식들을 직접 코딩을 통해서 확인을 할 수 있게 되었으며, 어떠한 물리적인 현상을 프로그램화 시키는 능력과 더불어 열역학에 대한 이해도를 높이게 되었다.
둘 째, 이때까지 배워왔던 이론들을 총집결해서 정리하는 시간이 되었을 뿐만 아니라, 앞으로 배워나가야 할 많은 지식과 이론, 현상들에 대해서 기대와 자신감을 가질 수 있게 해주는 시간이 되었다. 열역학이란 과목을 넘어 모든 분야에 대해 자신감을 가지게 되고, 끊임없이 문제를 제기하고 그 문제를 풀어나가기 위해서 노력하는 습관을 가지게 되었다.
마지막으로 세 번째, 조원들과 함께 작업은 분담하여 성취함으로서 평범한 인간관계에서 배울 수 없는 팀 구성원간의 team work를 습득하는 시간이 되었다고 생각된다. 어떠한 상황에는 팀의 한 구성원으로서, 다른 상황에서는 팀을 이끌어 나가는 리더로서 일을 성취해감으로서 성공적으로 이번 열역학 과제를 수행해 내었다고 생각된다.
아직까지 우리가 풀어나가야 할 이론들은 많이 남아 있다. 그러한 이론들에 대해서 호기심을 가지고, 문제를 제기해 가면서 우리 스스로의 발전을 도모해가도록 노력해야겠다.
6. Reference & Coding
이번 Term Project를 수행하기 위해서 다음과 같은 참고 자료들을 사용하였다.
- K. Kurihara et al, J. Chem. Eng. Data, vol, 40, pp, 679-684, 1995
- 화학공학연구정보센터(CHERIC), \"공정모사기에 필요한 열역학모델\", 조정호, 2002년
- H. Renon & J. M. Prausnitz, AIchE J., vol. 14, pp. 135-144, 1968
- G. M. Wilson, J. Am. Chem. Soc., vol 86, pp. 127-130, 1964
- 화학공학 열역학, Elliot, Lira, 고승태 [외]역. 아진출판사, 서울, 2001
- J. Gmehling, U. Onken, and W. Arlt, Vapor-Liquid Equilibrium Data Collection, Chemistry Data Service, vol. 1, parts 1-8, DECHEMA, Frankfurt/Main, 1974-1990
- \"Introduction to Chemical Engineering Thermodynamics\", Smith, Page 420, Fig. 11.4
- \"The Molecular Structure of Alcohol-Water Mixtures\", Phys. Rev. Lett. 91, 157401 (2003), J. H. Guo, et al.
에서도 유사한 결론이 나와 있다는 것을 알 수 있었다.
위 그림에서 나타내듯이, Ethanol/Water의 경우에도 같은 결론이 나온다는 것을 확인할 수 있었다. 우리 조는 이러한 현상을 어떻게 해석을 할 것인가에 대해서 고민을 해보고, 다른 자료들의 조사를 통해서 합당한 결론을 토출해 내었다.
지난 40년간 이러한 현상을 Hydrophobic Effect로 설명하였다고 한다. Hydrophobic Effect란 다음 그림에서 볼 수 있듯이 물에 어떠한 용질을 섞을 경우, 물 분자들이 용질을 둘러싸는 현상을 말한다. 물 분자들은 Intermolecular Hydrogen Bonding을 통해서 물에 넣는 다른 용질을 둘러싸게 되고, 이러한 현상은 용질 분자로 하여금 어떠한 정렬, 혹은 구속을 하게 되므로 를 감소하게 만든다. 다만, 분자들은 매우 빠른 속도로 구조를 바꾸기도 하고 움직이기 때문에 Hydrophobic Effect만으로는 명확히 현상을 설명할 수 없었다.
하지만 지난 2003년, J. H. Guo \"The Molecular Structure of Alcohol-Water Mixtures\", Phys. Rev. Lett. 91, 157401 (2003), J. H. Guo, et al.
외 여러 명의 과학자들로 구성된 팀에 의해 정확한 실험결과를 토대로 이 현상을 설명하게 되었다. Guo 팀은 이번에 우리가 사용한 Methanol/Water at 298.15K를 전제로 Oxygen X-ray absorption과 selectively excited X-ray emission spectroscopy를 연구하였고 다음과 같은 결과를 획득하였다.
위 결과 자료를 통해서 알 수 있듯이, 실험적으로 구한 데이터 값은 ring과 chain 구조의 혼합체, 그 중에서도 대부분이 6이나 8로 구성되었다는 결론에 도달하게 된다. 물을 메탄올과 섞을 경우 많은 메탄올 chain이 물 분자와 수소결합을 이루게 된다. 이러한 결합은 어느 정도의 길이를 이루게 되면 굽어져서 open-ring 구조를 이루게 되는데, 이 구조가 매우 안정하기 때문에 의 값이 감소하게 되는 것이다.
즉, microscopic한 관점에서 물과 메탄올이 섞이는 과정을 살펴보면 완전하지 않으며, 아무리 오래나 시간이 지나더라도 완전해 지지 못한 다는 것을 알 수 있다.
다만 이러한 구조를 가지는 것은 실험적으로도 알 수 있듯이 매우 극소수이며, 열역학 제 2법칙을 위반하지 않기 위해서 이러한 구조를 가지는 것에 대해서 분자들이 스스로 저항하기 때문에, 비록 값은 작지만 양수의 값을 가지게 되는 것이다.
이때까지 이번 Term Project를 통해서 얻은 새로운 결과들에 대해서 살펴보았다. 이러한 결과들을 토론을 통해서 생각해 보고, 토출하게 됨으로서 열역학을 해석하며 이해하는데 더욱더 도움이 되는 시간이 되었다고 생각된다.
5. Conclusion
이번 프로젝트를 통해서 우리는 크게 세 가지를 얻게 되었다.
첫 째, VLE binary system을 우리가 친근한 물질로 적용해 봄으로서 그 현상을 직접 이해하는 시간이 되었다. 이론적으로만 배우던 그래프나 공식들을 직접 코딩을 통해서 확인을 할 수 있게 되었으며, 어떠한 물리적인 현상을 프로그램화 시키는 능력과 더불어 열역학에 대한 이해도를 높이게 되었다.
둘 째, 이때까지 배워왔던 이론들을 총집결해서 정리하는 시간이 되었을 뿐만 아니라, 앞으로 배워나가야 할 많은 지식과 이론, 현상들에 대해서 기대와 자신감을 가질 수 있게 해주는 시간이 되었다. 열역학이란 과목을 넘어 모든 분야에 대해 자신감을 가지게 되고, 끊임없이 문제를 제기하고 그 문제를 풀어나가기 위해서 노력하는 습관을 가지게 되었다.
마지막으로 세 번째, 조원들과 함께 작업은 분담하여 성취함으로서 평범한 인간관계에서 배울 수 없는 팀 구성원간의 team work를 습득하는 시간이 되었다고 생각된다. 어떠한 상황에는 팀의 한 구성원으로서, 다른 상황에서는 팀을 이끌어 나가는 리더로서 일을 성취해감으로서 성공적으로 이번 열역학 과제를 수행해 내었다고 생각된다.
아직까지 우리가 풀어나가야 할 이론들은 많이 남아 있다. 그러한 이론들에 대해서 호기심을 가지고, 문제를 제기해 가면서 우리 스스로의 발전을 도모해가도록 노력해야겠다.
6. Reference & Coding
이번 Term Project를 수행하기 위해서 다음과 같은 참고 자료들을 사용하였다.
- K. Kurihara et al, J. Chem. Eng. Data, vol, 40, pp, 679-684, 1995
- 화학공학연구정보센터(CHERIC), \"공정모사기에 필요한 열역학모델\", 조정호, 2002년
- H. Renon & J. M. Prausnitz, AIchE J., vol. 14, pp. 135-144, 1968
- G. M. Wilson, J. Am. Chem. Soc., vol 86, pp. 127-130, 1964
- 화학공학 열역학, Elliot, Lira, 고승태 [외]역. 아진출판사, 서울, 2001
- J. Gmehling, U. Onken, and W. Arlt, Vapor-Liquid Equilibrium Data Collection, Chemistry Data Service, vol. 1, parts 1-8, DECHEMA, Frankfurt/Main, 1974-1990
- \"Introduction to Chemical Engineering Thermodynamics\", Smith, Page 420, Fig. 11.4
- \"The Molecular Structure of Alcohol-Water Mixtures\", Phys. Rev. Lett. 91, 157401 (2003), J. H. Guo, et al.














































소개글