목차
없음
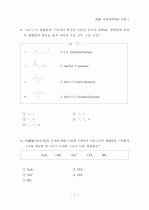
본문내용
생성물의 계수이다.)
① 3 ② 5
③ 6 ④ 7
⑤ 9
11
12
13
14
15
16
17
18
19
20
2
1
4
2
3
1
2
1
3
4
< 풀이 >
11. ㄴ. 4-methyl-1-pentene
ㄹ. 4-ethyl-2,2-dimethylhexane
12.
①
XeF4
평면사각형
②
NH4+
정사면체
③
SO42-
정사면체
④
CH4
정사면체
⑤
BF4-
정사면체
13. 서로 비교해서 H+ 을 내놓을 수 있는 물질이 산성이 강하다.
이중결합이 있는 고리 탄소하합물이 불안정해서 H+를 잘 내놓는다.
전기 음성도 가 큰 원소가 분자에 결합되어있으면 H+가 더 잘 떨어져
나온다.
14. 단일공명선의 Hz = 화학적 이동 상수(δ) × NMR 기기의 Hz
아세톤의 단일공명선 = 2.0 × 300 MHz = 600MHz
15. 온도와 압력이 일정한 조건에서 기체의 반응은
“반응 부피의 비 = 기체 반응 mol수 의 비” 이므로
1L의 P4와 6L의 H2의 반응은
1 mol의 P4와 6 mol의 H2와 반응했다는 말과 같으며 반응식은
P4 + 6H2 → 4 X
로 표현 할 수 있다.(X가 구하려는 답.) 이 때, PH3 만이 X가 될 수 있다.
16. 몰농도(M) = 용질몰수 (mol) ÷ 용액부피(L) = mol/L
따라서, 용질 A와 B 각각의 mol수를 알고 있다면 이제 수용액의 부피를 알아야 하는데, 그러기 위해서는 현재 수용액의 무게(=질량, mg)과 수용액의 밀도(단위부피당 질량, mg/mL)를 알아야 한다.
17. 반감기 t½ = 0.693/k 인 것으로 보아 이 반응의 반응속도식은 1차 반응속도식으로서, v = k[A] 이 된다.
반응 속도 v 값을 계산하려면, 속도상수 k와 [A]가 있어야 하므로,
일단 [A]는 문제에서 2.0×105 이라고 했고,
t½ 는 5분 즉 300초라고 했으므로,
300 = 0.693/k
k = 0.000231
그래서, v = k[A] = 0.000231 × 2.0×105 = 462 개/초
18. 특별히 암기할 것!!
Zn+(저스피, 고스핀), Ag+(고스핀 저스핀), Fe2+(저스핀), Pd4+(저스핀)
의 경우는 무조건 반자성을 가지며 다른 경우는 거의 상자성을 띤다.
19. 산화 전극은 (-)극, 환원전극은(+)극을 말하며, 두 개의 금속중 환원성이 높은 것은 환원전극이 되며, 그 금속이 표준환원전위값이 다른 하나의 금속 전극보다 높은 것이다. 그래서 표를 보고 환원성의 상대적 크기를 판단해 보면,
산화전극 D < B < A < E < C 환원전극
(낮은 환원전위) (높은 환원전위)
따라서, C가 표준환원전위가 가장 크다.
20. 반응식 계수 맞추는 법에서 산화수법을 적용시키면 아래 같이 반응식을 와성할 수 있다.
2Mg2+ + 5BiO3- + 14H+ → 2MnO4- + 5Bi3+ + 7H2O
※ 좀 더 자세한 풀이 동영상 강의를 원하신다면 네이버 까페
http://cafe.naver.com/chemistryacademy.cafe 에서 무료강의를 청강하세요.
① 3 ② 5
③ 6 ④ 7
⑤ 9
11
12
13
14
15
16
17
18
19
20
2
1
4
2
3
1
2
1
3
4
< 풀이 >
11. ㄴ. 4-methyl-1-pentene
ㄹ. 4-ethyl-2,2-dimethylhexane
12.
①
XeF4
평면사각형
②
NH4+
정사면체
③
SO42-
정사면체
④
CH4
정사면체
⑤
BF4-
정사면체
13. 서로 비교해서 H+ 을 내놓을 수 있는 물질이 산성이 강하다.
이중결합이 있는 고리 탄소하합물이 불안정해서 H+를 잘 내놓는다.
전기 음성도 가 큰 원소가 분자에 결합되어있으면 H+가 더 잘 떨어져
나온다.
14. 단일공명선의 Hz = 화학적 이동 상수(δ) × NMR 기기의 Hz
아세톤의 단일공명선 = 2.0 × 300 MHz = 600MHz
15. 온도와 압력이 일정한 조건에서 기체의 반응은
“반응 부피의 비 = 기체 반응 mol수 의 비” 이므로
1L의 P4와 6L의 H2의 반응은
1 mol의 P4와 6 mol의 H2와 반응했다는 말과 같으며 반응식은
P4 + 6H2 → 4 X
로 표현 할 수 있다.(X가 구하려는 답.) 이 때, PH3 만이 X가 될 수 있다.
16. 몰농도(M) = 용질몰수 (mol) ÷ 용액부피(L) = mol/L
따라서, 용질 A와 B 각각의 mol수를 알고 있다면 이제 수용액의 부피를 알아야 하는데, 그러기 위해서는 현재 수용액의 무게(=질량, mg)과 수용액의 밀도(단위부피당 질량, mg/mL)를 알아야 한다.
17. 반감기 t½ = 0.693/k 인 것으로 보아 이 반응의 반응속도식은 1차 반응속도식으로서, v = k[A] 이 된다.
반응 속도 v 값을 계산하려면, 속도상수 k와 [A]가 있어야 하므로,
일단 [A]는 문제에서 2.0×105 이라고 했고,
t½ 는 5분 즉 300초라고 했으므로,
300 = 0.693/k
k = 0.000231
그래서, v = k[A] = 0.000231 × 2.0×105 = 462 개/초
18. 특별히 암기할 것!!
Zn+(저스피, 고스핀), Ag+(고스핀 저스핀), Fe2+(저스핀), Pd4+(저스핀)
의 경우는 무조건 반자성을 가지며 다른 경우는 거의 상자성을 띤다.
19. 산화 전극은 (-)극, 환원전극은(+)극을 말하며, 두 개의 금속중 환원성이 높은 것은 환원전극이 되며, 그 금속이 표준환원전위값이 다른 하나의 금속 전극보다 높은 것이다. 그래서 표를 보고 환원성의 상대적 크기를 판단해 보면,
산화전극 D < B < A < E < C 환원전극
(낮은 환원전위) (높은 환원전위)
따라서, C가 표준환원전위가 가장 크다.
20. 반응식 계수 맞추는 법에서 산화수법을 적용시키면 아래 같이 반응식을 와성할 수 있다.
2Mg2+ + 5BiO3- + 14H+ → 2MnO4- + 5Bi3+ + 7H2O
※ 좀 더 자세한 풀이 동영상 강의를 원하신다면 네이버 까페
http://cafe.naver.com/chemistryacademy.cafe 에서 무료강의를 청강하세요.