목차
1. 열역학 법칙
2. 열역학 1법칙
2. 열역학 1법칙
본문내용
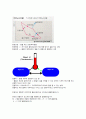
실린더에 포함된 기체에 일정량의 열이 가해지고 피스톤이 1위치에서 2위치로 상승했다고 한다면 가해지는 열량을 Q, 피스톤이 외부에 한 일을W, 기체의 내부에너지 변화는 U2-U1(△U) 이다
열역학 제 1법칙에 의해 Q = (U2-U1) + W(피스톤자체가 한 일이므로 부호가 (-) )
Q = (U2-U1) + P(V2-V1)
= (U2+P2V2) (U1+P1V1)
=H2 H1= △H
외부로부터 열이 가해져서 계의 내부에너지, 압력, 부피가 한꺼번에 변화했을 때, 그 변화하는 모든 물성을 하나의 변수로 나타낸 것!
엔트로피-‘물질의 상태가 변화하는 경로에 관계없이 항상 일정한값을 가지는 양’
물질의 초기와 말의 상태가 같다 하더라도 거친 경로에 따라 이동한열량이 다르다.
즉, 물질이 한곳에 모여있지 않고 전체에 골고루 퍼져 있으려는 자연의 성질 이라고 할 수 있겠음
등압과정(부피증가, 압력일정)
Q = △H
등용과정(부피일정, 압력증가)
부피가 일정하면 일을 하지 않으므로 역학적에너지의 변화는 없고, 계에 전달된 열량은 모두 기체의 내부에너지의 변화에만 사용. Q = △U
현열- ‘열이 전달되었을 때, 온도의 변화로 나타나는 열’
잠열- ‘물질의 상변화가 일어날 때 수반되는 열’
- 입자의 운동속도(운동에너지)와는 관계없이 입자의간격을 크게 하여 입자의 위치에너지를 증가시킴
증발열>용융열 ->> 고체에서 액체가 될 때보다 액체에서 기체가 될 때 부피변화가 훨씬 큼
압력이 높으면 기체로 존재하는 수증기의 위치에너지가 작아지고 수증기와 물의 에너지차이는 곧 잠열과같으므로 압력이 높을 때, 잠열이 감소!
열역학 제 1법칙에 의해 Q = (U2-U1) + W(피스톤자체가 한 일이므로 부호가 (-) )
Q = (U2-U1) + P(V2-V1)
= (U2+P2V2) (U1+P1V1)
=H2 H1= △H
외부로부터 열이 가해져서 계의 내부에너지, 압력, 부피가 한꺼번에 변화했을 때, 그 변화하는 모든 물성을 하나의 변수로 나타낸 것!
엔트로피-‘물질의 상태가 변화하는 경로에 관계없이 항상 일정한값을 가지는 양’
물질의 초기와 말의 상태가 같다 하더라도 거친 경로에 따라 이동한열량이 다르다.
즉, 물질이 한곳에 모여있지 않고 전체에 골고루 퍼져 있으려는 자연의 성질 이라고 할 수 있겠음
등압과정(부피증가, 압력일정)
Q = △H
등용과정(부피일정, 압력증가)
부피가 일정하면 일을 하지 않으므로 역학적에너지의 변화는 없고, 계에 전달된 열량은 모두 기체의 내부에너지의 변화에만 사용. Q = △U
현열- ‘열이 전달되었을 때, 온도의 변화로 나타나는 열’
잠열- ‘물질의 상변화가 일어날 때 수반되는 열’
- 입자의 운동속도(운동에너지)와는 관계없이 입자의간격을 크게 하여 입자의 위치에너지를 증가시킴
증발열>용융열 ->> 고체에서 액체가 될 때보다 액체에서 기체가 될 때 부피변화가 훨씬 큼
압력이 높으면 기체로 존재하는 수증기의 위치에너지가 작아지고 수증기와 물의 에너지차이는 곧 잠열과같으므로 압력이 높을 때, 잠열이 감소!

























소개글