목차
Table of Contents
List of Tables
List of Figures
AbstractⅡ
1. Introductio1
1-1. 에탄올의 역사 및 바이오 에탄올의 필요성
1-2. 바이오 에탄올의 재료 및 생산
1-3. 배지 구성 및 종류
1-4. 배지 멸균
2. Experiment
2-1. 실험시약 / 기구
2-2 실험 방법
3. Result & Discussion
3-1. Result
3-2. Calculation
Reference
List of Tables
Table 1. Raw Data.
List of Figures
Fig.1. 생산과정과 식물 재료정제습벽탑 장치.
Fig.2. 성장곡선
Fig.3. 비증식 속도
Fig.4. Autoclave
Fig.5. 시간 - 질량
Fig.6. 시간 - UV
Fig.7. 시간 - 당도 측정
List of Tables
List of Figures
AbstractⅡ
1. Introductio1
1-1. 에탄올의 역사 및 바이오 에탄올의 필요성
1-2. 바이오 에탄올의 재료 및 생산
1-3. 배지 구성 및 종류
1-4. 배지 멸균
2. Experiment
2-1. 실험시약 / 기구
2-2 실험 방법
3. Result & Discussion
3-1. Result
3-2. Calculation
Reference
List of Tables
Table 1. Raw Data.
List of Figures
Fig.1. 생산과정과 식물 재료정제습벽탑 장치.
Fig.2. 성장곡선
Fig.3. 비증식 속도
Fig.4. Autoclave
Fig.5. 시간 - 질량
Fig.6. 시간 - UV
Fig.7. 시간 - 당도 측정
본문내용
미생물 농도의 증가는 미생물 농도에 비례하는 1차반응이다.
미생물이 증식하면 기질은 감소한다. 기질이 없으면 미생물은 자신의 세포를 산화시켜서 에너지로 소비하게 되는데 이 과정을 내호흡, 자산화 과정이라 한다. 세포의 자산화 반응식을 표현하면
C5H7O2N + 5O2 → 5CO2 + 2H2O + NH3
그럼 미생물농도는 감소하게 된다. 시간의 변화에 따른 미생물 농도의 감소는 미생물 농도에 비례한다.
그렇다면 유기물이 있는 시료에 미생물을 식종하면 초기에는 미생물이 증식하고 미생물이 증식하면서 기질이 감소하면 나중에는 미생물이 감소한다. 증식그래프와 감소그래프를 종합하면 위의 Fig.2과 같다.[4],[5]
2. Experiment
2-1. 실험시약 / 기구
Yeast Extract, Dexrose, Peptone, Agar
Autoclave, Clean bench, 백금이
2-2 실험 방법
실험은 3일에 걸쳐서 실시 하였다. 첫째 날 액체배지와 고체배지를 만들었다.
100ml, 200ml 2개, 300ml(고체)만들었는데 각각의 시약의 %를 틀리게 하여 생성 했다. 액체배지는 무게를 측정하여 500ml 삼각 플라스크에 넣고 100ml를 넣어 용해 시켰다. 이때 삼각 플라스크 밑 부분이 shaking을 더욱 원활하게 하기 위해 홈이 파져 있는것을 사용하였다. 이는 와류를 만들게 하였으며 고체배지양은 petri dish에 약 25~30ml를 생각하여 제조 하였다. 삼각플라스크에 면전, 호일로 덮어주었다. 삼각플라스크들을 Autoclave 멸균해주었다. 121℃에서 15분간 멸균해주는데 1시간 30분후 꺼내어 clean bench에 넣어두었다. 액체배지는clean bench에그대로 두고 고체배지는 petri dish10개에 부어 하루이상 건조 시켰다. 이때 삼각플라스크에서 고체배지를 따르기 전 알콜 램프로 멸균을 해주었으며 액체배지가 식으면 백금이를 알콜램프로 멸균해준 후 Yeast를 약간 묻혀 액체배지에 넣어주었다. 삼각플라스크 입구, 면전, 호일 등을 알콜 램프로 멸균 해주었다. 마지막으로 진탕 배양기에서 24시간동안 배양시켰다. 둘째날 24시간 키운 액체배지에서 화염 멸균된 백금이를 식힌후 균을 묻힌 후 고체배지에 streaking 해주었다. 그리고나서 플레이트를 뒤집어서 incubator에넣고 하루 배양시켰다. 셋째날 10시간이상 한시간 마다 UV측정, 당분석, sampling 질량측정을 하였으며 역시 마찬가지로 모든 실험을 할때는 화염 멸균을 실시 하였다.
Fig.4. Autoclave
3. Result & Conclusion
3-1. Result
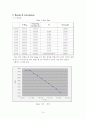
Table 1. Raw Data
무게Ag
B(samling 하지않은것)
UV
당도(mg/l)
09:50
377.12
378.43
18500
11:00
377.04
378.35
0.059
17256
12:00
372.38
378.34
0.068
17213
13:00
368.02
378.29
0.080
17175
14:00
363.73
378.27
0.107
17138
15:00
359.55
378.34
0.161
16811
16:00
355.21
378.31
0.266
16609
17:00
350.92
378.29
0.465
16601
18:00
346.69
378.22
0.758
16222
19:00
340.83
376.53
0.998(50ml희석)
16009
위와 같은 실험을 한 결과 Table 1.과 같은 결과를 얻었으며 시간이 갈수록 질량과 당도가 감소하는걸 알수 있었으며 UV 측정역시 늘어난 것을 알수 있었다.
그래프로 도식화 하면
Fig.5. 시간 - 질량
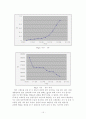
Fig.6. 시간 - UV
Fig.7. 시간 - 당도 측정
위의 그래프를 보면 알 수 있듯이 질량과 당은 감소하는 것을 알수 있다. 실제 샘플링하지 않은 삼각플라스크의 질량 변화는 2g정도 밖에 차이가 나지 않지만 실험 기구세척 할때는 에탄올의 냄새를 확연이 맡을 수 있었다. 특히 질량과 UV측정 그래프를 보면 성장곡선의 지연기에 해당되는 초기 값의 비교가 확연하다. 이는 실제 성장곡선에서의 모습과 비슷하나 당의 측정 그래프에는 초기 당 측정 시 오류를 범한 기록 값이 나왔다. 실험의 바이오 에탄올은 미량 생성 되었지만 분명한 에탄올 생성을 알 수 있었으며 마지막 측정 시 에도 지속적인 반응이 발생하고 있다는 걸 알 수 있다.
3-2 Conclusion
실험조원 모두가 바이오생물 실험은 처음이어여서 그런지 많은 어려움이 있었다.
하지만 직접 배지를 만들어 보며 접종해가며 바이오에 대한 많은 관심을 갖게 되었으며 실험의 내용도 쉽게 이해할 수 있어 많은 노력을 하였다. 실제 에탄올의 생성된 양을 측정할 수는 없었지만 실제 생성 되었다는 것을 알 수 있었고 바이오실험의 가장 중요한 부분은 멸균 이라는 것을 많이 느꼈다. 사실 첫 실험이라 그런지 많은 부분 오차가 있었다. 특히 clean bench에서의 실험시 정확한 멸균을 하지 않은것이다. 또한 sampling시 실내의 공기중에 있는 세균, 또는 먼지등이 효모 대사과정에 많은 부분 영향이 미쳤을거라 생각한다. 또한 실험기구의 오작동(당 측정)이 있었으며 배지 접종시 역시 배지가 찢어지거나 스크래치를 못한 경우도 많았다. 성장곡선과의 유사한 그래프를 얻을수 있어 이번 실험은 조금이나마 만족한 실험 이었다. 하지만 모두들 바이오 에탄올에 대해 아직 무지하며 많이 알아가야 하는것에 대해 인지하였다. 앞으로 화석연료의 대체 에너지로 많이 활용될수 있는 바이오 에탄올의 실험은 조원 모두에게 많은 정보와 관심을 갖게 해 주었다.
4. Reference
[1] 김종호, 최병철 , 전남대학교출판부, 바이오 에탄올 제조기술 및 활용 10p, 2007
[2] 윤천석, 대체에너지, 인터비젼, 2004
[3] 김영민외, 라이프 사이언스, 미생물학-7판 Prescott's microbiology, 2008
[4] L.M. Prescott, J.P. Harley, D.A. Klein 저, 김경민 외 6인 역.일반미생물학. 2003, 104∼ 124p
[5] 이갑상, 응용미생물학. 대학서림. 2000, 107∼120pp
미생물이 증식하면 기질은 감소한다. 기질이 없으면 미생물은 자신의 세포를 산화시켜서 에너지로 소비하게 되는데 이 과정을 내호흡, 자산화 과정이라 한다. 세포의 자산화 반응식을 표현하면
C5H7O2N + 5O2 → 5CO2 + 2H2O + NH3
그럼 미생물농도는 감소하게 된다. 시간의 변화에 따른 미생물 농도의 감소는 미생물 농도에 비례한다.
그렇다면 유기물이 있는 시료에 미생물을 식종하면 초기에는 미생물이 증식하고 미생물이 증식하면서 기질이 감소하면 나중에는 미생물이 감소한다. 증식그래프와 감소그래프를 종합하면 위의 Fig.2과 같다.[4],[5]
2. Experiment
2-1. 실험시약 / 기구
Yeast Extract, Dexrose, Peptone, Agar
Autoclave, Clean bench, 백금이
2-2 실험 방법
실험은 3일에 걸쳐서 실시 하였다. 첫째 날 액체배지와 고체배지를 만들었다.
100ml, 200ml 2개, 300ml(고체)만들었는데 각각의 시약의 %를 틀리게 하여 생성 했다. 액체배지는 무게를 측정하여 500ml 삼각 플라스크에 넣고 100ml를 넣어 용해 시켰다. 이때 삼각 플라스크 밑 부분이 shaking을 더욱 원활하게 하기 위해 홈이 파져 있는것을 사용하였다. 이는 와류를 만들게 하였으며 고체배지양은 petri dish에 약 25~30ml를 생각하여 제조 하였다. 삼각플라스크에 면전, 호일로 덮어주었다. 삼각플라스크들을 Autoclave 멸균해주었다. 121℃에서 15분간 멸균해주는데 1시간 30분후 꺼내어 clean bench에 넣어두었다. 액체배지는clean bench에그대로 두고 고체배지는 petri dish10개에 부어 하루이상 건조 시켰다. 이때 삼각플라스크에서 고체배지를 따르기 전 알콜 램프로 멸균을 해주었으며 액체배지가 식으면 백금이를 알콜램프로 멸균해준 후 Yeast를 약간 묻혀 액체배지에 넣어주었다. 삼각플라스크 입구, 면전, 호일 등을 알콜 램프로 멸균 해주었다. 마지막으로 진탕 배양기에서 24시간동안 배양시켰다. 둘째날 24시간 키운 액체배지에서 화염 멸균된 백금이를 식힌후 균을 묻힌 후 고체배지에 streaking 해주었다. 그리고나서 플레이트를 뒤집어서 incubator에넣고 하루 배양시켰다. 셋째날 10시간이상 한시간 마다 UV측정, 당분석, sampling 질량측정을 하였으며 역시 마찬가지로 모든 실험을 할때는 화염 멸균을 실시 하였다.
Fig.4. Autoclave
3. Result & Conclusion
3-1. Result
Table 1. Raw Data
무게Ag
B(samling 하지않은것)
UV
당도(mg/l)
09:50
377.12
378.43
18500
11:00
377.04
378.35
0.059
17256
12:00
372.38
378.34
0.068
17213
13:00
368.02
378.29
0.080
17175
14:00
363.73
378.27
0.107
17138
15:00
359.55
378.34
0.161
16811
16:00
355.21
378.31
0.266
16609
17:00
350.92
378.29
0.465
16601
18:00
346.69
378.22
0.758
16222
19:00
340.83
376.53
0.998(50ml희석)
16009
위와 같은 실험을 한 결과 Table 1.과 같은 결과를 얻었으며 시간이 갈수록 질량과 당도가 감소하는걸 알수 있었으며 UV 측정역시 늘어난 것을 알수 있었다.
그래프로 도식화 하면
Fig.5. 시간 - 질량
Fig.6. 시간 - UV
Fig.7. 시간 - 당도 측정
위의 그래프를 보면 알 수 있듯이 질량과 당은 감소하는 것을 알수 있다. 실제 샘플링하지 않은 삼각플라스크의 질량 변화는 2g정도 밖에 차이가 나지 않지만 실험 기구세척 할때는 에탄올의 냄새를 확연이 맡을 수 있었다. 특히 질량과 UV측정 그래프를 보면 성장곡선의 지연기에 해당되는 초기 값의 비교가 확연하다. 이는 실제 성장곡선에서의 모습과 비슷하나 당의 측정 그래프에는 초기 당 측정 시 오류를 범한 기록 값이 나왔다. 실험의 바이오 에탄올은 미량 생성 되었지만 분명한 에탄올 생성을 알 수 있었으며 마지막 측정 시 에도 지속적인 반응이 발생하고 있다는 걸 알 수 있다.
3-2 Conclusion
실험조원 모두가 바이오생물 실험은 처음이어여서 그런지 많은 어려움이 있었다.
하지만 직접 배지를 만들어 보며 접종해가며 바이오에 대한 많은 관심을 갖게 되었으며 실험의 내용도 쉽게 이해할 수 있어 많은 노력을 하였다. 실제 에탄올의 생성된 양을 측정할 수는 없었지만 실제 생성 되었다는 것을 알 수 있었고 바이오실험의 가장 중요한 부분은 멸균 이라는 것을 많이 느꼈다. 사실 첫 실험이라 그런지 많은 부분 오차가 있었다. 특히 clean bench에서의 실험시 정확한 멸균을 하지 않은것이다. 또한 sampling시 실내의 공기중에 있는 세균, 또는 먼지등이 효모 대사과정에 많은 부분 영향이 미쳤을거라 생각한다. 또한 실험기구의 오작동(당 측정)이 있었으며 배지 접종시 역시 배지가 찢어지거나 스크래치를 못한 경우도 많았다. 성장곡선과의 유사한 그래프를 얻을수 있어 이번 실험은 조금이나마 만족한 실험 이었다. 하지만 모두들 바이오 에탄올에 대해 아직 무지하며 많이 알아가야 하는것에 대해 인지하였다. 앞으로 화석연료의 대체 에너지로 많이 활용될수 있는 바이오 에탄올의 실험은 조원 모두에게 많은 정보와 관심을 갖게 해 주었다.
4. Reference
[1] 김종호, 최병철 , 전남대학교출판부, 바이오 에탄올 제조기술 및 활용 10p, 2007
[2] 윤천석, 대체에너지, 인터비젼, 2004
[3] 김영민외, 라이프 사이언스, 미생물학-7판 Prescott's microbiology, 2008
[4] L.M. Prescott, J.P. Harley, D.A. Klein 저, 김경민 외 6인 역.일반미생물학. 2003, 104∼ 124p
[5] 이갑상, 응용미생물학. 대학서림. 2000, 107∼120pp