본문내용
4
KD 평균값 = (1.137+1.835+1.204)/3=1.392
수치 및 결과(Data & Results)
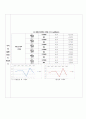
표3. 아세트산수용액과 1-부탄올 각각의 log값(평균농도)
아세트산수용액 + 1-부탄올
0.5N 아세트산 수용액 (20ml)
1-부탄올층
log CA
-0.776
물층
log CB
-0.939
0.5N 아세트산 수용액 (40ml)
1-부탄올층
log CA
-0.708
물층
log CB
-0.790
1.0N 아세트산 수용액 (20ml)
1-부탄올층
log CA
-0.678
물층
log CB
-0.714
1.0N 아세트산 수용액 (40ml)
1-부탄올층
log CA
-1.398
물층
log CB
-1.444
1.5N 아세트산 수용액 (20ml)
1-부탄올층
log CA
-0.366
물층
log CB
-0.381
1.5N 아세트산 수용액 (40ml)
1-부탄올층
log CA
-0.983
물층
log CB
-1.244
↑1-부탄올층 의 그래프 ↑물층의 그래프
표4. n의 값구하기.
아세트산수용액 + 1-부탄올
0.5N 아세트산수용액(20ml)
1.423
0.5N 아세트산수용액(40ml)
1.108
1.0N 아세트산수용액(20ml)
1.084
1.0N 아세트산수용액(40ml)
1.102
1.5N 아세트산수용액(20ml)
1.770
1.5N 아세트산수용액(40ml
1.394
결론
-n 값의 의미
농도의 따른 변수
2) 적은 양의 추출 용매를 여러 번 사용하는 것이 같은 양의 용매를 한번 사용하는 것보다 효과적인지에 대한 실험값의 비교.
*앞의 실험 결과로 미루어 보아 적은 양의 추출 용매가 더 효과적인걸 알수 있다.
5) 실험방법 5번에서 같은 부피의 물을 넣어서 적정을 하는 이유
-아래층 10mL 나 증류수 10mL를 가한 용액이나 아세트산의 이온화된 양은 동일하므로 물을 가하여 적정 하는 것은 실험의 적확성을 높이기 위함이다.그리고 증류수를 넣지 않고 실험을 할 경우에 시료의 양이 적으면 마그네틱 바가 잠기지 않고 교반을 하게 되면 시료가 사방으로 튀어서 실험값에 영향을 줄수도 있기 때문에 적정을 하는 것이다.
--------------------------------------------------------------------------------------------------------------------------------------------------
이번 실험 결과,보다 적은 양의 추출용매를 여러번 사용하는 것이 같은양의 용매를 사용하는것보다 훨씬 효과적이라는 결론이 도출되었다.또한 물층과 1-부탄올 층 이 평형을 이루게 될 때 평형상수 k를 분배계수 KD 라고 하고,이 실험을 통하여 도출된 값으로 농도의 따른 변수값과 분배계수KD를 구할수 있었다.그리고 증류스를 넣음으로써 실험의 정확성을 높일수 있다는 결과도 나왔다.
-)실험결과를 보면 그래프가 일정한 방향이 아닌 지그재그 형태인데 이 이유는 실험값이 정확하지 않고 오차값이 포함되어서 그래프의 결과값의 산출이 위와같은 그래프의 모형을 띄우게 된것이다.
KD 평균값 = (1.137+1.835+1.204)/3=1.392
수치 및 결과(Data & Results)
표3. 아세트산수용액과 1-부탄올 각각의 log값(평균농도)
아세트산수용액 + 1-부탄올
0.5N 아세트산 수용액 (20ml)
1-부탄올층
log CA
-0.776
물층
log CB
-0.939
0.5N 아세트산 수용액 (40ml)
1-부탄올층
log CA
-0.708
물층
log CB
-0.790
1.0N 아세트산 수용액 (20ml)
1-부탄올층
log CA
-0.678
물층
log CB
-0.714
1.0N 아세트산 수용액 (40ml)
1-부탄올층
log CA
-1.398
물층
log CB
-1.444
1.5N 아세트산 수용액 (20ml)
1-부탄올층
log CA
-0.366
물층
log CB
-0.381
1.5N 아세트산 수용액 (40ml)
1-부탄올층
log CA
-0.983
물층
log CB
-1.244
↑1-부탄올층 의 그래프 ↑물층의 그래프
표4. n의 값구하기.
아세트산수용액 + 1-부탄올
0.5N 아세트산수용액(20ml)
1.423
0.5N 아세트산수용액(40ml)
1.108
1.0N 아세트산수용액(20ml)
1.084
1.0N 아세트산수용액(40ml)
1.102
1.5N 아세트산수용액(20ml)
1.770
1.5N 아세트산수용액(40ml
1.394
결론
-n 값의 의미
농도의 따른 변수
2) 적은 양의 추출 용매를 여러 번 사용하는 것이 같은 양의 용매를 한번 사용하는 것보다 효과적인지에 대한 실험값의 비교.
*앞의 실험 결과로 미루어 보아 적은 양의 추출 용매가 더 효과적인걸 알수 있다.
5) 실험방법 5번에서 같은 부피의 물을 넣어서 적정을 하는 이유
-아래층 10mL 나 증류수 10mL를 가한 용액이나 아세트산의 이온화된 양은 동일하므로 물을 가하여 적정 하는 것은 실험의 적확성을 높이기 위함이다.그리고 증류수를 넣지 않고 실험을 할 경우에 시료의 양이 적으면 마그네틱 바가 잠기지 않고 교반을 하게 되면 시료가 사방으로 튀어서 실험값에 영향을 줄수도 있기 때문에 적정을 하는 것이다.
--------------------------------------------------------------------------------------------------------------------------------------------------
이번 실험 결과,보다 적은 양의 추출용매를 여러번 사용하는 것이 같은양의 용매를 사용하는것보다 훨씬 효과적이라는 결론이 도출되었다.또한 물층과 1-부탄올 층 이 평형을 이루게 될 때 평형상수 k를 분배계수 KD 라고 하고,이 실험을 통하여 도출된 값으로 농도의 따른 변수값과 분배계수KD를 구할수 있었다.그리고 증류스를 넣음으로써 실험의 정확성을 높일수 있다는 결과도 나왔다.
-)실험결과를 보면 그래프가 일정한 방향이 아닌 지그재그 형태인데 이 이유는 실험값이 정확하지 않고 오차값이 포함되어서 그래프의 결과값의 산출이 위와같은 그래프의 모형을 띄우게 된것이다.




























소개글