목차
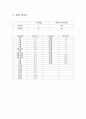
1. 실험 결과치
2. 실험결과의 정리 및 고찰
2. 실험결과의 정리 및 고찰
본문내용
은 열용량과 크기는 같은 물의 질량을 말한다.
물의 비열이1 이므로 그 물질의 열용량과 같은 물의 질량이 있으면 열역학적으로
그 물질과 같은 효과를 낼 수 있다.
A라는 물질의 열용량이 40[cal/c]이라면 물당량은 40g이다.
7) 실험에 사용한 연료의 문헌에 나와 있는 발열량 값과 실험에서 얻 은 연료의 발열량 값을 비교하시오.
ㅇ 문헌에 나와 있는 연료의 발열량:
백등유(Domestic Heating Kerosene)
- 일명 : 다증유 용제 또는 세정용등유
- 아날린점가정난방(가정조명) 및 가정 연료용(석유스토브,석유곤로),
각종 발동기(내연기관)용 연료 페인트, 니스의 용제, 살충제,
- 농약유제, 세정용경유(Diesel)
- 비중 : 0.82~0.90
- 비점범위 : 200~370
- 발열량 : 11141Kcal/Kg
ㅇ 실험에서 얻은 연료의 발열량 : 9845.59 cal/g
5) Discussion
이번 실험은 액체 및 고체연료의 발열량 측정 실험으로서 단열식 봄 열량계를 사용하여 발열량을 측정함으로써 공급된 에너지 량을 알아내는 실험이다. 미지의 연료에 대한 발열량을 알아보기 위한 실험으로 1g을 기준으로 실험하였다.
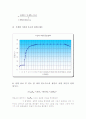
우선 발열량이 무엇인지 알아보면 발열량이란 연료에 대해서만 정의되는 양으로 연료 1kg이 연소할 때 나오는 열량이라고 말할 수 있다. 실험결과를 분석해보면, 그래프에서 확인 할 수 있듯이 처음 5분간은 온도변화가 적다. 이 시간은 연소가 시작되기 전의 시간으로 이때의 온도변화 이유는 점화 선에 의한 열 발생과 교반기에 의한 자체적인 온도 상승으로 이해할 수 있다. 그 이유는 강제대류를 시키기 위하여 봄 열량계 안에서 프로팰러를 돌려주기 때문이다. 이러한 온도 상승을 보정해 주기 위하여 e₃와 R1(b-a)를 통해 보상해 주었다.
점화가 시작되는 시간인 5분 이후로는 온도가 급격히 증가함을 살펴볼 수 있다. 그리고 총 온도상승의 60%가 되는 구간부터는 온도구배가 서서히 완만해지기 시작하며 12분이 지난 이후부터는 거의 온도변화가 없게된다.
실험으로 계산된 연료의 발열량은 9845.59cal/g로서 백등유의 발열량 11141cal/g의 88.37%정도의 발열량이 측정되었다. 오차발생의 원인으로는 이 실험에서 가장 중요하다고 볼 수 있는 온도 측정이 가장 큰 이유라고 생각되어진다. 온도계를 눈금으로 읽다보니 아주 정확한 값을 읽어내기 힘들기 때문이다. 그리고 처음 전열선 10cm를 점화 후 길이측정에서도 전열선이 곧지 않아서 길이 측정에서도 약간의 오차가 발생했을 거라는 생각이 든다. 그리고 c점 온도변화율이 일정해지는 지점을 찾기 가 힘들어 임의로 10분 (온도변화율 약0.1)로 지정한것과 마지막으로 산소량이 적어서 완전연소가 일어나지 못했을 가능성도 제기할 수 있다.
위와 같은 여러 가지 이유로 이론상 백등유의 발열량보다 11.63%정도 족은 발열량이 측정되었으나 이론상의 수치와 거의 일치하며 기본적인 실험의 원리와 발열량의 개념을 이해하는 데에는 별 무리가 없었던 실험이라 생각된다.
물의 비열이1 이므로 그 물질의 열용량과 같은 물의 질량이 있으면 열역학적으로
그 물질과 같은 효과를 낼 수 있다.
A라는 물질의 열용량이 40[cal/c]이라면 물당량은 40g이다.
7) 실험에 사용한 연료의 문헌에 나와 있는 발열량 값과 실험에서 얻 은 연료의 발열량 값을 비교하시오.
ㅇ 문헌에 나와 있는 연료의 발열량:
백등유(Domestic Heating Kerosene)
- 일명 : 다증유 용제 또는 세정용등유
- 아날린점가정난방(가정조명) 및 가정 연료용(석유스토브,석유곤로),
각종 발동기(내연기관)용 연료 페인트, 니스의 용제, 살충제,
- 농약유제, 세정용경유(Diesel)
- 비중 : 0.82~0.90
- 비점범위 : 200~370
- 발열량 : 11141Kcal/Kg
ㅇ 실험에서 얻은 연료의 발열량 : 9845.59 cal/g
5) Discussion
이번 실험은 액체 및 고체연료의 발열량 측정 실험으로서 단열식 봄 열량계를 사용하여 발열량을 측정함으로써 공급된 에너지 량을 알아내는 실험이다. 미지의 연료에 대한 발열량을 알아보기 위한 실험으로 1g을 기준으로 실험하였다.
우선 발열량이 무엇인지 알아보면 발열량이란 연료에 대해서만 정의되는 양으로 연료 1kg이 연소할 때 나오는 열량이라고 말할 수 있다. 실험결과를 분석해보면, 그래프에서 확인 할 수 있듯이 처음 5분간은 온도변화가 적다. 이 시간은 연소가 시작되기 전의 시간으로 이때의 온도변화 이유는 점화 선에 의한 열 발생과 교반기에 의한 자체적인 온도 상승으로 이해할 수 있다. 그 이유는 강제대류를 시키기 위하여 봄 열량계 안에서 프로팰러를 돌려주기 때문이다. 이러한 온도 상승을 보정해 주기 위하여 e₃와 R1(b-a)를 통해 보상해 주었다.
점화가 시작되는 시간인 5분 이후로는 온도가 급격히 증가함을 살펴볼 수 있다. 그리고 총 온도상승의 60%가 되는 구간부터는 온도구배가 서서히 완만해지기 시작하며 12분이 지난 이후부터는 거의 온도변화가 없게된다.
실험으로 계산된 연료의 발열량은 9845.59cal/g로서 백등유의 발열량 11141cal/g의 88.37%정도의 발열량이 측정되었다. 오차발생의 원인으로는 이 실험에서 가장 중요하다고 볼 수 있는 온도 측정이 가장 큰 이유라고 생각되어진다. 온도계를 눈금으로 읽다보니 아주 정확한 값을 읽어내기 힘들기 때문이다. 그리고 처음 전열선 10cm를 점화 후 길이측정에서도 전열선이 곧지 않아서 길이 측정에서도 약간의 오차가 발생했을 거라는 생각이 든다. 그리고 c점 온도변화율이 일정해지는 지점을 찾기 가 힘들어 임의로 10분 (온도변화율 약0.1)로 지정한것과 마지막으로 산소량이 적어서 완전연소가 일어나지 못했을 가능성도 제기할 수 있다.
위와 같은 여러 가지 이유로 이론상 백등유의 발열량보다 11.63%정도 족은 발열량이 측정되었으나 이론상의 수치와 거의 일치하며 기본적인 실험의 원리와 발열량의 개념을 이해하는 데에는 별 무리가 없었던 실험이라 생각된다.


























소개글