목차
1. 결과치 (result)
2. 실험 결과 정리 및 고찰
3. 토론 및 토의 (Debate or DISCUSSION)
2. 실험 결과 정리 및 고찰
3. 토론 및 토의 (Debate or DISCUSSION)
본문내용
당량이라고 한다.
예를 들어 A라는 물질의 열용량이 40[kcal/℃]이라면 물당량은 40kg이다.
실험에 사용한 연료의 문헌에 나와 있는 발열량 값과 실험에서 얻은 발열량 값을 비교하시오.
▶문헌에 나와있는 연료의 발열량
명명
= 백등유, 다중유 용제, 세정용등유
분류
= 농약유제, 세정용 경유(Diesel)
비중
= 0.82~0.90
비점 범위
= 200~370
발열량
= 11,000kcal/kg
▶실험에서 얻은 연료의 발열량
실험값
이론값
9716.040 cal/g
11,172.612cal/g
▶오차
9716.04cal/g-11,000cal/g=-1,283.96cal/g
3. 토론 및 토의 (Debate or DISCUSSION)
이번 실험은 발열량 측정시험으로 고제나 액체의 발열량을 측정하는데 주로 이용되는 등온식 봄(bomb) 열량계를 측정해 봄으로서 열량계의 사용방법을 익히고, 발열량에 대한 이해를 깊게 하고자 한 실험이었다. 연료의 발열량은 완전 연소 생성물의 온도를 반응물의 초기 온도까지 낮출 때 얻은 총 열로 정의되며, 연소과정은 발열반응이므로 항상 양의 값으로 측정된다. 또한 발열량은 연료의 단위 질량당 (고제나 액체연료), 또는 연료 단위 체적 당(기체연료)의 값으로 보통 표시하는데 실험에서는 백등유 1g을 기준으로 하여 발열량을 측정하였다.
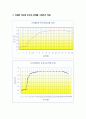
결과치를 살펴 보면 초기의 점화 전 5분간을 살펴보면 거의 온도가 일정한 것을 알 수 있다. 이때 온도가 약간 상승한 까닭은 물이 대기중의 온도보다 낮으므로 대기에서 봄 내부로 흘러 들어간 열량과 점화시 물의 온도를 골고루 분포시키기 위해 휘젓기 날개를 돌려 그때 공급해 준 에너지가 물로 약간 이동한 것으로 보여진다. 이때의 온도상승은 연료의 발렬양과는 무관하므로 보정해 주기 위하여 항이 상승온도를 구하기 위한 식에 들어간 것이다. 또한 9분 이후로는 온도 상승률이 약 1℃/min으로 일정하다가 온도변화가 없는 17℃구간으로 진입하였다. 17℃이후로는 연료에서 얻는 열이 더 이상 물의 온도를 상승시키지 못하고 유지되다가 결국 외부로 열이 방출되어 40분 이후로는 온도가 점점 떨어지게 되었다.
이번시험에서 구한 백등유의 발열량 결과치는 9716.04cal/g으로 실제 문헌에서 기록되어 있는 발열량보다 1,283.96 cal/g 작게 나오게 되었다. 발열량이 이렇게 크게 오차가 난 이유로는 연료가 연소하여 발생한 열이 물의 온도를 상승 시킨것만 생각하고 봄 외부로 빠져나간 열량은 측정 할 수 없기 때문에 생긴 오차가 크다고 볼 수 있다. 또한 온도변화를 사람의 눈으로 측정하기 때문에 정확한 시간에 정확한 값을 측정하지 못 한 것이 오차의 한 원인이 될수 있으며, 사용후의 전열선 조각들의 길이를 측정할 때 조각이 여러개로 나뉘어 측정하는데 오차가 일어난 것도 작은 원인이 될 수 있겠다. 오차율은 11.66%로 위의 상황을 감안한다면 외부로 빠져나가서 측정되자 않는 열이 상당히 크다는 것을 알 수 있겠다.
발열량은 종류가 여러 가지가 있어서 기록시에는 발열량의 종류를 기입하여야 한다. 이번 실험에서는 봄 뚜껑 안쪽에 물이 없었는데 실험 후 물이 고여 있는 것을 볼 수 있었다. 이결과로 인해 봄 내의 연료가 공기와 만나 연소하면서 생긴 수증기가 물로 응결하면서 방출된 열량까지 봄의 온도를 높이는데 사용되었다는 것을 알 수 있었다. 따라서 이번실험에서 측정한 발열량은 고위발열량임을 알 수 있다.
이번 실험을 통하여 발열량이 종류에 따라 다르며 발열량 기입시 꼭 발열량종류를 기입해야 한다는 것을 알게 되었다. 또한 발열량의 개념과 물당량의 개념을 알게 되었고, 열량계의 사용방법을 익힐수 있었던 실험이었다.
예를 들어 A라는 물질의 열용량이 40[kcal/℃]이라면 물당량은 40kg이다.
실험에 사용한 연료의 문헌에 나와 있는 발열량 값과 실험에서 얻은 발열량 값을 비교하시오.
▶문헌에 나와있는 연료의 발열량
명명
= 백등유, 다중유 용제, 세정용등유
분류
= 농약유제, 세정용 경유(Diesel)
비중
= 0.82~0.90
비점 범위
= 200~370
발열량
= 11,000kcal/kg
▶실험에서 얻은 연료의 발열량
실험값
이론값
9716.040 cal/g
11,172.612cal/g
▶오차
9716.04cal/g-11,000cal/g=-1,283.96cal/g
3. 토론 및 토의 (Debate or DISCUSSION)
이번 실험은 발열량 측정시험으로 고제나 액체의 발열량을 측정하는데 주로 이용되는 등온식 봄(bomb) 열량계를 측정해 봄으로서 열량계의 사용방법을 익히고, 발열량에 대한 이해를 깊게 하고자 한 실험이었다. 연료의 발열량은 완전 연소 생성물의 온도를 반응물의 초기 온도까지 낮출 때 얻은 총 열로 정의되며, 연소과정은 발열반응이므로 항상 양의 값으로 측정된다. 또한 발열량은 연료의 단위 질량당 (고제나 액체연료), 또는 연료 단위 체적 당(기체연료)의 값으로 보통 표시하는데 실험에서는 백등유 1g을 기준으로 하여 발열량을 측정하였다.
결과치를 살펴 보면 초기의 점화 전 5분간을 살펴보면 거의 온도가 일정한 것을 알 수 있다. 이때 온도가 약간 상승한 까닭은 물이 대기중의 온도보다 낮으므로 대기에서 봄 내부로 흘러 들어간 열량과 점화시 물의 온도를 골고루 분포시키기 위해 휘젓기 날개를 돌려 그때 공급해 준 에너지가 물로 약간 이동한 것으로 보여진다. 이때의 온도상승은 연료의 발렬양과는 무관하므로 보정해 주기 위하여 항이 상승온도를 구하기 위한 식에 들어간 것이다. 또한 9분 이후로는 온도 상승률이 약 1℃/min으로 일정하다가 온도변화가 없는 17℃구간으로 진입하였다. 17℃이후로는 연료에서 얻는 열이 더 이상 물의 온도를 상승시키지 못하고 유지되다가 결국 외부로 열이 방출되어 40분 이후로는 온도가 점점 떨어지게 되었다.
이번시험에서 구한 백등유의 발열량 결과치는 9716.04cal/g으로 실제 문헌에서 기록되어 있는 발열량보다 1,283.96 cal/g 작게 나오게 되었다. 발열량이 이렇게 크게 오차가 난 이유로는 연료가 연소하여 발생한 열이 물의 온도를 상승 시킨것만 생각하고 봄 외부로 빠져나간 열량은 측정 할 수 없기 때문에 생긴 오차가 크다고 볼 수 있다. 또한 온도변화를 사람의 눈으로 측정하기 때문에 정확한 시간에 정확한 값을 측정하지 못 한 것이 오차의 한 원인이 될수 있으며, 사용후의 전열선 조각들의 길이를 측정할 때 조각이 여러개로 나뉘어 측정하는데 오차가 일어난 것도 작은 원인이 될 수 있겠다. 오차율은 11.66%로 위의 상황을 감안한다면 외부로 빠져나가서 측정되자 않는 열이 상당히 크다는 것을 알 수 있겠다.
발열량은 종류가 여러 가지가 있어서 기록시에는 발열량의 종류를 기입하여야 한다. 이번 실험에서는 봄 뚜껑 안쪽에 물이 없었는데 실험 후 물이 고여 있는 것을 볼 수 있었다. 이결과로 인해 봄 내의 연료가 공기와 만나 연소하면서 생긴 수증기가 물로 응결하면서 방출된 열량까지 봄의 온도를 높이는데 사용되었다는 것을 알 수 있었다. 따라서 이번실험에서 측정한 발열량은 고위발열량임을 알 수 있다.
이번 실험을 통하여 발열량이 종류에 따라 다르며 발열량 기입시 꼭 발열량종류를 기입해야 한다는 것을 알게 되었다. 또한 발열량의 개념과 물당량의 개념을 알게 되었고, 열량계의 사용방법을 익힐수 있었던 실험이었다.




























소개글