목차
실험제목
실험목적
실험 이론
실험 방법
기구 및 시약
실험결과
토의 및 결과
결론
참고문헌
실험목적
실험 이론
실험 방법
기구 및 시약
실험결과
토의 및 결과
결론
참고문헌
본문내용
에 넣는다.
⑤ 80℃에서 84℃까지 기-액평형데이터를 얻기위해 80℃까지 올리면서 혼합용액 (liquid)과 응축액(vapor)의 질량을 비중병을 이용해 측정, 기록한다.
⑥ 식을 이용해 wt% 조성을 구한다.
⑦ mol wt%로 구한다. 이것을 책에 있는 평형도와 비교한다.
7. 실험 결과
1) 검량선 작성
Name
Weight 1st
Weight 2nd
Weight 3rd
Weight Ave
0 W%
0.997
0.998
0.996
0.9975
100 W%
0.788
0.787
0.788
0.787
y = ax + b
0.9975a + b =0, 0.787a + b =100, y = -475x + 473.81
Temp
(℃)
Liquid Weight
(g)
Liquid
Weight
Fraction
Liquid
mol
Fraction
x
Vapor
Weight
(g)
Vapor
Weight
Fraction
Vapor
mol
Fraction
y
77℃
0.901
45.8
0.322
0.81
89.06
0.821
79℃
0.916
38.71
0.262
0.831
79.085
0.68
81℃
0.923
35.39
0.235
0.864
63.41
0.49
83℃
0.937
28.735
0.185
0.881
55.335
0.41
2) 기-액 평형 실험
3) Calculate the Liquid Weight fraction
①
②
③
④
4) Calculate the Vapor Weight fraction
①
②
③
④
5) Calculate the Liquid mol Fraction
①
②
③
④
6) Calculate the Vapor mol Fraction
①
②
③
④
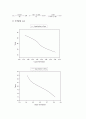
7) 기액평형 도표
8) 문헌값과 실험값의 비교
이론값 T(℃)
x
y
실험값 T(℃)
x
y
78
0.3
0.665
77
0.322
0.821
81.7
0.2
0.613
79
0.262
0.68
84.4
0.15
0.517
81
0.235
0.49
83
0.185
0.41
8. 고 찰
이번 실험은 일정한 압력 하에서 단증류 조건에 가장 잘 부합하는 증류수와 메탄올 혼합 용액을 일정한 온도로 증발시켜 혼합 증기와의 평형 관계를 기록하고 그래프에 플롯하여 기-액 평형관계를 관찰하는 실험으로 약간의 계산을 필요로 하지만 실험자체는 비교적 간단한 실험 이었다. 먼저 증류수, 메탄올 혼합액을 Boiler 안에 넣고 일정 온도 까지 온도를 높이면서 혼합용액과 응축액의 질량을 측정하고 wt%조성과 mol wt%를 각각 구한다. 이 실험은 높은 온도까지 가열하므로 화상의 위험성이 있다. 따라서 실험을 할 때 장갑을 착용하고 실험기구를 조심히 다루도록 해야 한다. 또한 보일러에 투여하는 증류수와 메탄올의 비와 일정 온도후의 질량이 이번실험의 관건이므로 되도록 정확히 측정하도록 노력해야한다.
그렇게 실험한 결과값이 위와 같이 나왔다. 우리가 측정한 실험값을 문헌값과 비교해본 결과 x값은 대체로 만족스러운 결과를 얻었으나 y값이 문헌값과 다소 차이를 보였다. 게다가 모든 y의 실험값이 문헌값보다 높거나 낮게 나온것이 아니라 어느부분은 높게나오고 어느부분을 낮게 나오는등 뒤죽박죽으로 나왔다. 따라서 기액평형 그래프도 완만한 곡선이 아닌 2차식의 곡선으로 나왔다. 이 결과는 실험시 약간의 오차가 발생했을 것이라 생각되고 그 오차를 생각해본 결과 보일러를 일정온도까지 올리는데 시간이 너무 오래 걸려 우리가 일정한속도로 가열시키지 않고 계속 변화시킨데 원인이 있었을 것이라 생각된다. 또한 목표온도까지 높이는데 80℃정도부터 온도가 올라가는 시간이 너무 오래 걸려 실험책에 나와있는 온도에서 약간 하향조절을 했고, 처음 투입하는 혼합물의 비의 오차도 있을 수 있을 것이라 생각된다. 마지막으로 실험하면서 실험책 상에서 실험방법에 나오지 않아 한동안 냉각수를 흘려보내지 않다가 뒤늦게 알게 되어 한참 후에 냉각수를 흘려보낸 점 또한 오차의 원인이었을 것이라 생각된다. 이처럼 이번 실험은 기-액평형 장치를 처음 접해보아서 장치 이해하고 다루는데 어려움이 많았다. 하지만 실험 후 기-액평형관계에 대해 이해할 수 있었고 장치 작동법과 원리에 대하여 알게 된 계기가 되었다.
9. 참고 문헌
① 일반화학실험/형설출판사/ 권규혁외 9명/ p45~49
② 화공열역학(2005)/ Mcgrawhill/ J.M.smith외 1명/ p432~445
③ 화학공학/ 사이텍미디어/ 성기천외 2명/ p455~468
⑤ 80℃에서 84℃까지 기-액평형데이터를 얻기위해 80℃까지 올리면서 혼합용액 (liquid)과 응축액(vapor)의 질량을 비중병을 이용해 측정, 기록한다.
⑥ 식을 이용해 wt% 조성을 구한다.
⑦ mol wt%로 구한다. 이것을 책에 있는 평형도와 비교한다.
7. 실험 결과
1) 검량선 작성
Name
Weight 1st
Weight 2nd
Weight 3rd
Weight Ave
0 W%
0.997
0.998
0.996
0.9975
100 W%
0.788
0.787
0.788
0.787
y = ax + b
0.9975a + b =0, 0.787a + b =100, y = -475x + 473.81
Temp
(℃)
Liquid Weight
(g)
Liquid
Weight
Fraction
Liquid
mol
Fraction
x
Vapor
Weight
(g)
Vapor
Weight
Fraction
Vapor
mol
Fraction
y
77℃
0.901
45.8
0.322
0.81
89.06
0.821
79℃
0.916
38.71
0.262
0.831
79.085
0.68
81℃
0.923
35.39
0.235
0.864
63.41
0.49
83℃
0.937
28.735
0.185
0.881
55.335
0.41
2) 기-액 평형 실험
3) Calculate the Liquid Weight fraction
①
②
③
④
4) Calculate the Vapor Weight fraction
①
②
③
④
5) Calculate the Liquid mol Fraction
①
②
③
④
6) Calculate the Vapor mol Fraction
①
②
③
④
7) 기액평형 도표
8) 문헌값과 실험값의 비교
이론값 T(℃)
x
y
실험값 T(℃)
x
y
78
0.3
0.665
77
0.322
0.821
81.7
0.2
0.613
79
0.262
0.68
84.4
0.15
0.517
81
0.235
0.49
83
0.185
0.41
8. 고 찰
이번 실험은 일정한 압력 하에서 단증류 조건에 가장 잘 부합하는 증류수와 메탄올 혼합 용액을 일정한 온도로 증발시켜 혼합 증기와의 평형 관계를 기록하고 그래프에 플롯하여 기-액 평형관계를 관찰하는 실험으로 약간의 계산을 필요로 하지만 실험자체는 비교적 간단한 실험 이었다. 먼저 증류수, 메탄올 혼합액을 Boiler 안에 넣고 일정 온도 까지 온도를 높이면서 혼합용액과 응축액의 질량을 측정하고 wt%조성과 mol wt%를 각각 구한다. 이 실험은 높은 온도까지 가열하므로 화상의 위험성이 있다. 따라서 실험을 할 때 장갑을 착용하고 실험기구를 조심히 다루도록 해야 한다. 또한 보일러에 투여하는 증류수와 메탄올의 비와 일정 온도후의 질량이 이번실험의 관건이므로 되도록 정확히 측정하도록 노력해야한다.
그렇게 실험한 결과값이 위와 같이 나왔다. 우리가 측정한 실험값을 문헌값과 비교해본 결과 x값은 대체로 만족스러운 결과를 얻었으나 y값이 문헌값과 다소 차이를 보였다. 게다가 모든 y의 실험값이 문헌값보다 높거나 낮게 나온것이 아니라 어느부분은 높게나오고 어느부분을 낮게 나오는등 뒤죽박죽으로 나왔다. 따라서 기액평형 그래프도 완만한 곡선이 아닌 2차식의 곡선으로 나왔다. 이 결과는 실험시 약간의 오차가 발생했을 것이라 생각되고 그 오차를 생각해본 결과 보일러를 일정온도까지 올리는데 시간이 너무 오래 걸려 우리가 일정한속도로 가열시키지 않고 계속 변화시킨데 원인이 있었을 것이라 생각된다. 또한 목표온도까지 높이는데 80℃정도부터 온도가 올라가는 시간이 너무 오래 걸려 실험책에 나와있는 온도에서 약간 하향조절을 했고, 처음 투입하는 혼합물의 비의 오차도 있을 수 있을 것이라 생각된다. 마지막으로 실험하면서 실험책 상에서 실험방법에 나오지 않아 한동안 냉각수를 흘려보내지 않다가 뒤늦게 알게 되어 한참 후에 냉각수를 흘려보낸 점 또한 오차의 원인이었을 것이라 생각된다. 이처럼 이번 실험은 기-액평형 장치를 처음 접해보아서 장치 이해하고 다루는데 어려움이 많았다. 하지만 실험 후 기-액평형관계에 대해 이해할 수 있었고 장치 작동법과 원리에 대하여 알게 된 계기가 되었다.
9. 참고 문헌
① 일반화학실험/형설출판사/ 권규혁외 9명/ p45~49
② 화공열역학(2005)/ Mcgrawhill/ J.M.smith외 1명/ p432~445
③ 화학공학/ 사이텍미디어/ 성기천외 2명/ p455~468





























소개글