-
 1
1
-
 2
2
-
 3
3
-
 4
4
-
 5
5
-
 6
6
-
 7
7
-
 8
8
-
 9
9
-
 10
10
-
 11
11
-
 12
12
-
 13
13
-
 14
14
-
 15
15
-
 16
16
-
 17
17
-
 18
18
-
 19
19
-
 20
20
-
 21
21
-
 22
22
-
 23
23
-
 24
24
-
 25
25
-
 26
26
-
 27
27
-
 28
28
-
 29
29
-
 30
30
-
 31
31
-
 32
32
-
 33
33
-
 34
34
-
 35
35
-
 36
36
-
 37
37
-
 38
38
-
 39
39
-
 40
40
-
 41
41
-
 42
42
-
 43
43
-
 44
44
-
 45
45
-
 46
46
-
 47
47
-
 48
48
-
 49
49
-
 50
50
-
 51
51
-
 52
52
-
 53
53
-
 54
54
-
 55
55
-
 56
56
-
 57
57
-
 58
58
-
 59
59
-
 60
60
-
 61
61
-
 62
62
-
 63
63
-
 64
64
-
 65
65
-
 66
66
-
 67
67
-
 68
68
-
 69
69
-
 70
70
-
 71
71
-
 72
72
-
 73
73
-
 74
74
-
 75
75
-
 76
76
-
 77
77
-
 78
78
-
 79
79
-
 80
80
-
 81
81
-
 82
82
-
 83
83
-
 84
84
-
 85
85
-
 86
86
-
 87
87
-
 88
88
-
 89
89
-
 90
90
-
 91
91
-
 92
92
-
 93
93
-
 94
94
-
 95
95
-
 96
96
-
 97
97
-
 98
98
-
 99
99
-
 100
100
-
 101
101
-
 102
102
-
 103
103
-
 104
104
-
 105
105
-
 106
106
-
 107
107
-
 108
108
-
 109
109
-
 110
110
-
 111
111
-
 112
112
-
 113
113
-
 114
114
-
 115
115
-
 116
116
-
 117
117
-
 118
118
-
 119
119
-
 120
120
-
 121
121
-
 122
122
-
 123
123
-
 124
124
-
 125
125
-
 126
126
-
 127
127
-
 128
128
-
 129
129
-
 130
130
-
 131
131
-
 132
132
-
 133
133
-
 134
134
-
 135
135
-
 136
136
-
 137
137
-
 138
138
-
 139
139
-
 140
140
-
 141
141
-
 142
142
-
 143
143
-
 144
144
본 자료는 10페이지 의 미리보기를 제공합니다. 이미지를 클릭하여 주세요.

-
1
-
2
-
3
-
4
-
5
-
6
-
7
-
8
-
9
-
10
-
11
-
12
-
13
-
14
-
15
-
16
-
17
-
18
-
19
-
20
-
21
-
22
-
23
-
24
-
25
-
26
-
27
-
28
-
29
-
30
-
31
-
32
-
33
-
34
-
35
-
36
-
37
-
38
-
39
-
40
-
41
-
42
-
43
-
44
-
45
-
46
-
47
-
48
-
49
-
50
-
51
-
52
-
53
-
54
-
55
-
56
-
57
-
58
-
59
-
60
-
61
-
62
-
63
-
64
-
65
-
66
-
67
-
68
-
69
-
70
-
71
-
72
-
73
-
74
-
75
-
76
-
77
-
78
-
79
-
80
-
81
-
82
-
83
-
84
-
85
-
86
-
87
-
88
-
89
-
90
-
91
-
92
-
93
-
94
-
95
-
96
-
97
-
98
-
99
-
100
-
101
-
102
-
103
-
104
-
105
-
106
-
107
-
108
-
109
-
110
-
111
-
112
-
113
-
114
-
115
-
116
-
117
-
118
-
119
-
120
-
121
-
122
-
123
-
124
-
125
-
126
-
127
-
128
-
129
-
130
-
131
-
132
-
133
-
134
-
135
-
136
-
137
-
138
-
139
-
140
-
141
-
142
-
143
-
144


본문내용
-chloro-2-methylpropane
(c) 1, 2-dichloroethane(d) 1, 1, 2-trichloroethene
12. (a) 2, 2-dichloropentane(b) 3-bromo-1-butene
(c) 1, 2-dichloro-2-fluoropropane(d) p-dichlorobenzene
13. 대부분의 페놀은 커다란 비극성 부분을 가지는 상대적으로 고분자량 화합물이다. 따라서 물에 대한 용해도가 낮다.
14.
(a) 2-butanol :
(b) cyclobexanol :
(c) 1, 4-butanediol :
15.
(a) methoxymethane
(b) 2-ethoxypropane
(c) 1, 3-dimethoxybutane
(d) ethoxybenzene
(e) methoxycyclobutane
또는
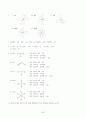
16. (a) R, R', R''는 같을 수도 있고 다를 수도 있다.
1차 아민
2차 아민
3차 아민
(b) (CH3)2CHNH2는 2차 아민이 아니고 1차 아민이다. NH3(암모니아)의 구조에서 수소 1개만 유기그룹으로 치환된 것을 볼 수 있다.
17.
(a) 2-methylbutanal
(b) propanal
(c) o-methoxybenzaldehyde
(d) butanone
(e) bromopropanone
(f) 3-heptanone
18.
(a) methylpropanoic acid
(b) 3-bromobutanoic acid
(c) p-nitrobenzoic acid
(d) potassium benzoate
(e) 2-aminopropanoic acid
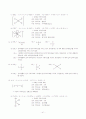
19.
(a)
: ethyl ethanoate
(b)
: methyl methanoate
20. (a) 자외선 하에서 에탄의 염소화 반응은 자유라디칼 반응이다. 먼저 자외선에 의해 염소문자가 분리되어 반응성이 큰 염소라디칼이 형성되어 반응이 개시된다. 이 반응성이 큰 염소라디칼은 에탄에 있는 수소하나를 떼어내어 HCl과 C2H5 라디칼을 형성한다. 이 C2H5 라디칼은 다시 또 다른 Cl2 분자에서 Cl 원자를 떼어내어 일치환된 염화에탄과 또 하나의 Cl 라디칼을 형성하여 반응은 연쇄적으로 일어난다. 계속적인 반응은 최대로 염소화된 C2Cl6를 형성할 때까지 진행될 수 있다.
(b) (c)
과량의 Cl2 존재하에서 치환반응은 계속 진행되어 다음 화합물들이 얻어진다.
21. 알켄의 비극성 용액에 브롬이 첨가되면, 브롬이 알켄과 반응하여 무색의 화합물을 생성하므로 용액의 색깔은 브롬의 오렌색에서 무색으로 변하게 된다. 그러나 알칸의 용액에 브롬을 첨가하며 자외선이나 다른 촉매가 없는한 감지할만한 속도의 반응이 일어나지 않는다.
22. (a) 치환반응(b) 제거반응(c) 치환반응
23.
24. (a) 이중결합을 사이에 둔 네 개의 치환체가 모두 같으므로 Cis, trans 이성질체가 존재할 수 없다.
(b)
Cis와 trans 이성질체로 존재할 수 있다.
(c) 방향족 고리는 평면이므로 Cis, trans 이성질체가 존재할 수 없다.
(d) 두 개의 치환체가 링에서 같은 원소에 결합되어 있으므로 Cis, trans 이성질체가 존재할 수 없다.
25. (a) 광학이성질 현상을 나타낼 수 있다. 네 개의 다른 그룹이 중심 탄소에 결합하고 있어 거울상이 겹쳐질 수 있다.
(b) 광학이성질 현상을 나타낼 수 없다. 중심 탄소에 결합한 두 그룹이 같기 때문에 거울상이 겹쳐질 수 있다.
(c) 광학이성질 현상을 나타낼 수 있다. 중심 탄소에 네 개의 다른 그룹이 결합하고 있어 거울상이 겹쳐질 수 있다.
(d) 광학이성질 현상을 나타낼 수 있다. 이중결합을 이루는 탄소들은 평면의 기하구조를 가지므로 거울상은 겹쳐질 수 있다.
26. 아민은 N(질소)에 있는 비공유 전자상을 가지고 있어 H+를 받아들일 수 있으므로 브론스테드-로리 염기이다. 수용액에서 아민은 가수분해되어 평형에서 수산화이온을 생성한다.
암모니아 : NH3(ag) + H2O(ℓ) NH4+(ag) + OH-(ag)
아민(1차) : RNH2(ag) + H2O(ℓ) RNH3+(ag) + OH-(ag)
27. 이 각각의 두 염은 약염기의 짝산을 포함한다. 보다 약한 염기의 짝산이 보다 강산성을 나타내므로, 같은 0.1M 용액에서 aniline hyolrochloride(C6H5NH3Cl) 용액이 더 산성이다.
28. (a) 산화(b) 산화(c) 환원(e) 환원
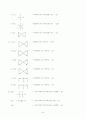
29. (a)
(b)
(c)
30. (a) 알코올(b) 에터(c) 페놀(d) 케톤
31. (a)
: carboxylic acid (카르복시산 기)
(b)
: double bond(이중결합), allcene(알켄)
: ester(에스터 기)
(c)
: phenol(페놀 기)
: nitro(니트로 기)
: ketone(케톤 기), Carbonyl(카보닐 기)
: alcohol(알코올 기)
(d)
: amine(아민 기)
32. (a)
(b)
(c)
33. (a)
(b)
(c)
34. 시클로헥산은 평면 고리 모양으로 존재하지 못하는데, 이는 sp3 탄소의 결합각인 109.5와 비교하여 평면 육각형일 때의 결합각(120)이 다르기 때문이며, 평면 고리가 이러한 무리(strain)을 피하기 위해 휘어져서 평면 구조를 벗어나게 된다.
35. (a) 가지가 없는 알칸의 경우 분자량이 증가함에 따라 녹는점과 끓는점이 일반적으로 증가한다.
(b) 분자량에 따라 녹는점, 끓는점이 증가할 것으로 기대된다.
(c) 분자가 커지면 표면적이 커지고, 따라서 분자간의 상호작용력이 증가하게 된다. 증가된 상호작용령은 고체가 녹는것을 억제하게 되므로, 이 상호작용력을 극복하고 고체가 녹게 하려면 더 많은 에너지가 필요하게 된다. 따라서 분자가 클수록 더 높은 온도에서 녹거나 끓게 된다.
36. butanone
37. (a) 공명구조는 같은 원자 배열을 가지지만 결합 전자쌍의 배열리 다른 구조들이다.
(b)
(c) 벤젠에서 이중결합에 참여하는 6개의 전자는 확장된 -결합계에 전체적으로 골고루 퍼져있다. 이 확장된 -겹침계는 6개의 탄소원자에서 각각의 6개의 p궤도함수 겹쳐 형성된다.
(c) 1, 2-dichloroethane(d) 1, 1, 2-trichloroethene
12. (a) 2, 2-dichloropentane(b) 3-bromo-1-butene
(c) 1, 2-dichloro-2-fluoropropane(d) p-dichlorobenzene
13. 대부분의 페놀은 커다란 비극성 부분을 가지는 상대적으로 고분자량 화합물이다. 따라서 물에 대한 용해도가 낮다.
14.
(a) 2-butanol :
(b) cyclobexanol :
(c) 1, 4-butanediol :
15.
(a) methoxymethane
(b) 2-ethoxypropane
(c) 1, 3-dimethoxybutane
(d) ethoxybenzene
(e) methoxycyclobutane
또는
16. (a) R, R', R''는 같을 수도 있고 다를 수도 있다.
1차 아민
2차 아민
3차 아민
(b) (CH3)2CHNH2는 2차 아민이 아니고 1차 아민이다. NH3(암모니아)의 구조에서 수소 1개만 유기그룹으로 치환된 것을 볼 수 있다.
17.
(a) 2-methylbutanal
(b) propanal
(c) o-methoxybenzaldehyde
(d) butanone
(e) bromopropanone
(f) 3-heptanone
18.
(a) methylpropanoic acid
(b) 3-bromobutanoic acid
(c) p-nitrobenzoic acid
(d) potassium benzoate
(e) 2-aminopropanoic acid
19.
(a)
: ethyl ethanoate
(b)
: methyl methanoate
20. (a) 자외선 하에서 에탄의 염소화 반응은 자유라디칼 반응이다. 먼저 자외선에 의해 염소문자가 분리되어 반응성이 큰 염소라디칼이 형성되어 반응이 개시된다. 이 반응성이 큰 염소라디칼은 에탄에 있는 수소하나를 떼어내어 HCl과 C2H5 라디칼을 형성한다. 이 C2H5 라디칼은 다시 또 다른 Cl2 분자에서 Cl 원자를 떼어내어 일치환된 염화에탄과 또 하나의 Cl 라디칼을 형성하여 반응은 연쇄적으로 일어난다. 계속적인 반응은 최대로 염소화된 C2Cl6를 형성할 때까지 진행될 수 있다.
(b) (c)
과량의 Cl2 존재하에서 치환반응은 계속 진행되어 다음 화합물들이 얻어진다.
21. 알켄의 비극성 용액에 브롬이 첨가되면, 브롬이 알켄과 반응하여 무색의 화합물을 생성하므로 용액의 색깔은 브롬의 오렌색에서 무색으로 변하게 된다. 그러나 알칸의 용액에 브롬을 첨가하며 자외선이나 다른 촉매가 없는한 감지할만한 속도의 반응이 일어나지 않는다.
22. (a) 치환반응(b) 제거반응(c) 치환반응
23.
24. (a) 이중결합을 사이에 둔 네 개의 치환체가 모두 같으므로 Cis, trans 이성질체가 존재할 수 없다.
(b)
Cis와 trans 이성질체로 존재할 수 있다.
(c) 방향족 고리는 평면이므로 Cis, trans 이성질체가 존재할 수 없다.
(d) 두 개의 치환체가 링에서 같은 원소에 결합되어 있으므로 Cis, trans 이성질체가 존재할 수 없다.
25. (a) 광학이성질 현상을 나타낼 수 있다. 네 개의 다른 그룹이 중심 탄소에 결합하고 있어 거울상이 겹쳐질 수 있다.
(b) 광학이성질 현상을 나타낼 수 없다. 중심 탄소에 결합한 두 그룹이 같기 때문에 거울상이 겹쳐질 수 있다.
(c) 광학이성질 현상을 나타낼 수 있다. 중심 탄소에 네 개의 다른 그룹이 결합하고 있어 거울상이 겹쳐질 수 있다.
(d) 광학이성질 현상을 나타낼 수 있다. 이중결합을 이루는 탄소들은 평면의 기하구조를 가지므로 거울상은 겹쳐질 수 있다.
26. 아민은 N(질소)에 있는 비공유 전자상을 가지고 있어 H+를 받아들일 수 있으므로 브론스테드-로리 염기이다. 수용액에서 아민은 가수분해되어 평형에서 수산화이온을 생성한다.
암모니아 : NH3(ag) + H2O(ℓ) NH4+(ag) + OH-(ag)
아민(1차) : RNH2(ag) + H2O(ℓ) RNH3+(ag) + OH-(ag)
27. 이 각각의 두 염은 약염기의 짝산을 포함한다. 보다 약한 염기의 짝산이 보다 강산성을 나타내므로, 같은 0.1M 용액에서 aniline hyolrochloride(C6H5NH3Cl) 용액이 더 산성이다.
28. (a) 산화(b) 산화(c) 환원(e) 환원
29. (a)
(b)
(c)
30. (a) 알코올(b) 에터(c) 페놀(d) 케톤
31. (a)
: carboxylic acid (카르복시산 기)
(b)
: double bond(이중결합), allcene(알켄)
: ester(에스터 기)
(c)
: phenol(페놀 기)
: nitro(니트로 기)
: ketone(케톤 기), Carbonyl(카보닐 기)
: alcohol(알코올 기)
(d)
: amine(아민 기)
32. (a)
(b)
(c)
33. (a)
(b)
(c)
34. 시클로헥산은 평면 고리 모양으로 존재하지 못하는데, 이는 sp3 탄소의 결합각인 109.5와 비교하여 평면 육각형일 때의 결합각(120)이 다르기 때문이며, 평면 고리가 이러한 무리(strain)을 피하기 위해 휘어져서 평면 구조를 벗어나게 된다.
35. (a) 가지가 없는 알칸의 경우 분자량이 증가함에 따라 녹는점과 끓는점이 일반적으로 증가한다.
(b) 분자량에 따라 녹는점, 끓는점이 증가할 것으로 기대된다.
(c) 분자가 커지면 표면적이 커지고, 따라서 분자간의 상호작용력이 증가하게 된다. 증가된 상호작용령은 고체가 녹는것을 억제하게 되므로, 이 상호작용력을 극복하고 고체가 녹게 하려면 더 많은 에너지가 필요하게 된다. 따라서 분자가 클수록 더 높은 온도에서 녹거나 끓게 된다.
36. butanone
37. (a) 공명구조는 같은 원자 배열을 가지지만 결합 전자쌍의 배열리 다른 구조들이다.
(b)
(c) 벤젠에서 이중결합에 참여하는 6개의 전자는 확장된 -결합계에 전체적으로 골고루 퍼져있다. 이 확장된 -겹침계는 6개의 탄소원자에서 각각의 6개의 p궤도함수 겹쳐 형성된다.
추천자료
 일반화학실험 결과보고서 - 마그네슘의 연소
일반화학실험 결과보고서 - 마그네슘의 연소 일반화학실험 결과보고서 - Cyclodextrin을 이용한 형광의 증가
일반화학실험 결과보고서 - Cyclodextrin을 이용한 형광의 증가 일반화학실험-전기분해와 도금
일반화학실험-전기분해와 도금 일반화학실험-결정장 갈라짐 에너지의 측정
일반화학실험-결정장 갈라짐 에너지의 측정 일반화학 d구역 원소 정리
일반화학 d구역 원소 정리 수문학연습문제풀이
수문학연습문제풀이 일반화학실험_FT-IR을 이용한 분자식 및 분자 구조 구하기
일반화학실험_FT-IR을 이용한 분자식 및 분자 구조 구하기 일반화학실험 - 물의 기화엔탈피와 엔트로피 변화의 측정
일반화학실험 - 물의 기화엔탈피와 엔트로피 변화의 측정 일반화학실험 - 표준산, 염기 적정용액 실험
일반화학실험 - 표준산, 염기 적정용액 실험 일반화학 실험보고서 - Ascorbic acid의 분자량 결정
일반화학 실험보고서 - Ascorbic acid의 분자량 결정 일반화학실험 - 어는점 내림법에 의한 분자량 측정
일반화학실험 - 어는점 내림법에 의한 분자량 측정 일반화학실험 - 반응열측정 실험
일반화학실험 - 반응열측정 실험 일반화학실험 - 카페인의 추출과 분리
일반화학실험 - 카페인의 추출과 분리 일반화학실험 - 어는점 내림 측정
일반화학실험 - 어는점 내림 측정


















소개글