목차
Exp. No 3 - 시계반응
일반화학회
일반화학회
본문내용
있어 가장 좋은 방법은 무엇인가?
(2)고찰
지난 실험에서는 온도가 반응물질에 미치는 영향을 알아보는 것이라면, 이번 실험은 반응물의 농도가 반응 속도에 미치는 영향을 알아 보는 것이 없다.
고등학교 공통과학 시간에 이미 이런 내용에 대해 이론을 배웠도 또한 실험을 한 적이 있다. 하지만 요번 실험 고등학교 때랑 다른 점은, 두 가지의 반응 경로를 통해서 색깔 변화를 관찰할 수 있다는 것이다. 앞의 결과 분석에서 언급했었는데, 실험보고서를 작성하면서 왜 Na2S2O3(티오황산나트륨)를 넣는지 잘 몰랐다. 처음에는 ‘반응을 빠르게 하려고 정촉매를 넣는 것이구나!’ 생각하고 인터넷 검색을 해보았는데 I2 분자를 빨리 없애주어 결국 마지막에 남은 I2 분자로 녹말과 시계반응을 일으킨다는 것을 알게 되었다.
또한 KCl과 K(NH4)2SO4를 넣어주는 이유를 그냥 다른 것으로 채우기 위해서인지 알았는데 그것이 아니고 이온의 세기를 맞추어 주기 위해서라는 사실도 알 수 있었다.
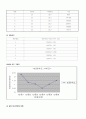
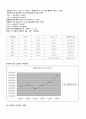
결과는 실험이 쉽고, 또한 쉬운 만큼 정확성 있게 했기 때문에 반응 속도결과는 잘 나온 것 같은데, 온도가 모든 반응에서 일정하다는 것이 조금 수상하다. 내가 가지고 있는 지식에 의하면 반응속도가 빠른 것이 온도가 더 높게 나와야 되는데 그러지 못한 것이 아쉽다.
(3) 오차가 난 이유
① 용액을 만들기 위해서 시약을 정량으로 달아서 넣어야 되는데 이분에서 오차가 생겼을 수 있다.
② 0.005M의 Na2S2O3(티오황산나트륨)용액을 제조할 때 사용한 시약은 5수하물(5H20)이 붙어 있는 시약이라서 용액제조계산에서 오차가 생겼을 수 있다.
③ 삼각 플라스크, 피펫등 에 오염 되어있어 정확한 결과를 얻기 못했을 수 있다.
④ 색깔 변화가 너무 갑작스럽게 일어나서 정확하게 파악하지 못했을 수 있다.
⑤ 실험결과에서 온도 부분에서 오차가 많이 난 것 같은데, 온도계를 각각 다른 것을 사용했지 때문에 정확성이 떨어 질수 있다. 또한 아날로그 온도계라서 세밀한 온도를 못 측정 할 수 있다.
(4) 느낀 점
앞에서 언급 했듯이 대체적으로 실험이 쉬웠다. 또한 정확한 실험을 하려고 열심히 실험했기 때문에 반응속도는 어느 정도 재현성 있게 한 것 같았다. 하지만 온도 변화에서 정확한 결과를 얻지 못해서 아쉽다. 다른 학교의 시계반응 실험 매뉴얼을 보니 반응속도를 구하는 다향 방법이 있다는 것을 깨달았고 또한 그 분분에 관해서도 공부를 해 봐야겠다.
(2)고찰
지난 실험에서는 온도가 반응물질에 미치는 영향을 알아보는 것이라면, 이번 실험은 반응물의 농도가 반응 속도에 미치는 영향을 알아 보는 것이 없다.
고등학교 공통과학 시간에 이미 이런 내용에 대해 이론을 배웠도 또한 실험을 한 적이 있다. 하지만 요번 실험 고등학교 때랑 다른 점은, 두 가지의 반응 경로를 통해서 색깔 변화를 관찰할 수 있다는 것이다. 앞의 결과 분석에서 언급했었는데, 실험보고서를 작성하면서 왜 Na2S2O3(티오황산나트륨)를 넣는지 잘 몰랐다. 처음에는 ‘반응을 빠르게 하려고 정촉매를 넣는 것이구나!’ 생각하고 인터넷 검색을 해보았는데 I2 분자를 빨리 없애주어 결국 마지막에 남은 I2 분자로 녹말과 시계반응을 일으킨다는 것을 알게 되었다.
또한 KCl과 K(NH4)2SO4를 넣어주는 이유를 그냥 다른 것으로 채우기 위해서인지 알았는데 그것이 아니고 이온의 세기를 맞추어 주기 위해서라는 사실도 알 수 있었다.
결과는 실험이 쉽고, 또한 쉬운 만큼 정확성 있게 했기 때문에 반응 속도결과는 잘 나온 것 같은데, 온도가 모든 반응에서 일정하다는 것이 조금 수상하다. 내가 가지고 있는 지식에 의하면 반응속도가 빠른 것이 온도가 더 높게 나와야 되는데 그러지 못한 것이 아쉽다.
(3) 오차가 난 이유
① 용액을 만들기 위해서 시약을 정량으로 달아서 넣어야 되는데 이분에서 오차가 생겼을 수 있다.
② 0.005M의 Na2S2O3(티오황산나트륨)용액을 제조할 때 사용한 시약은 5수하물(5H20)이 붙어 있는 시약이라서 용액제조계산에서 오차가 생겼을 수 있다.
③ 삼각 플라스크, 피펫등 에 오염 되어있어 정확한 결과를 얻기 못했을 수 있다.
④ 색깔 변화가 너무 갑작스럽게 일어나서 정확하게 파악하지 못했을 수 있다.
⑤ 실험결과에서 온도 부분에서 오차가 많이 난 것 같은데, 온도계를 각각 다른 것을 사용했지 때문에 정확성이 떨어 질수 있다. 또한 아날로그 온도계라서 세밀한 온도를 못 측정 할 수 있다.
(4) 느낀 점
앞에서 언급 했듯이 대체적으로 실험이 쉬웠다. 또한 정확한 실험을 하려고 열심히 실험했기 때문에 반응속도는 어느 정도 재현성 있게 한 것 같았다. 하지만 온도 변화에서 정확한 결과를 얻지 못해서 아쉽다. 다른 학교의 시계반응 실험 매뉴얼을 보니 반응속도를 구하는 다향 방법이 있다는 것을 깨달았고 또한 그 분분에 관해서도 공부를 해 봐야겠다.
추천자료
 (일반화학실험) 비누화반응
(일반화학실험) 비누화반응 [화학실험] 알코올의 반응
[화학실험] 알코올의 반응 화학 - 에스테르화 반응
화학 - 에스테르화 반응 [유기화학실험] 아민의 반응
[유기화학실험] 아민의 반응 [화학실험보고서] 금속의 반응성
[화학실험보고서] 금속의 반응성 [일반화학실험] 반응열과 헤스의 법칙(Hess` law)
[일반화학실험] 반응열과 헤스의 법칙(Hess` law) [화학실험] 반응속도에 미치는 온도의 영향
[화학실험] 반응속도에 미치는 온도의 영향 [유기화학 실험] 08. p니트로아닐린(p-nitroaniline)의 제조 예비 : 이번 실험은 방향족 니트...
[유기화학 실험] 08. p니트로아닐린(p-nitroaniline)의 제조 예비 : 이번 실험은 방향족 니트... [유기화학 실험] 08. p니트로아닐린(p-nitroaniline)의 제조 결과 : 이번 실험은 방향족 니트...
[유기화학 실험] 08. p니트로아닐린(p-nitroaniline)의 제조 결과 : 이번 실험은 방향족 니트... [일반화학] 반응속도와 농도의 영향
[일반화학] 반응속도와 농도의 영향 [일반화학] 마그네슘의 연소 반응을 이용한 산소의 원자량 결정 : 마그네슘의 연소 반응을 통...
[일반화학] 마그네슘의 연소 반응을 이용한 산소의 원자량 결정 : 마그네슘의 연소 반응을 통... [생물학 실험] 단백질(蛋白質) 검출 : 생명현상과 생물체를 이루는 중요한 구성요소 중 단백...
[생물학 실험] 단백질(蛋白質) 검출 : 생명현상과 생물체를 이루는 중요한 구성요소 중 단백... [유기화학] 알코올의 반응 : Lucas(루카스) 시약을 통해 1차, 2차, 3차 알코올의 반응과 구...
[유기화학] 알코올의 반응 : Lucas(루카스) 시약을 통해 1차, 2차, 3차 알코올의 반응과 구... 일반화학실험 - 비누화반응
일반화학실험 - 비누화반응

























소개글