본문내용
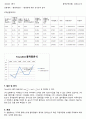
의 양이 증가하는 것을 그래프의 기울기는 양의 값인 것을 보아 확인할 수 있다.
5. 토의
이 실험에서는 각각의 플라스크에 흡착평형이 제대로 일어났는지 혹은 적정과정에 오차를 주의하며 해야한다. 오차의 원인으로는
1. 월요일날 오후에 실험을 진행한 후 수요일 낮까지 만 2일이 되지 않는 시간으로 인해 흡착평형이 제대로 일어나지 않았을 수 있다.
2. 적정에 사용하는 NaOH, 그리고 유기산인 아세트산() 수용액의 농도를 만드는데 있어 오차가 있을 수 있다.
3. 활성탄을 섞을 때 거름종이에 활성탄이 아주 약간 남아있어서 다 섞지 못한 것이 오차가 될 수 있다.
4. 활성탄을 여과할 때 비커에 물이 남아있어 오차가 생겼을 수 있다.
5. 1N 농도의 NaOH수용액을 제조할 때, 고체의 NaOH가 눈금실린더에 가라앉아 완전히 섞이지 않은 것이 오차가 될 수 있다.
6. 적정하는 과정에 뷰렛의 눈금을 읽는 것 혹은 지시약을 넣는데 있어 오차가 발생했을 수 있다.
그 외에도 이번 실험을 하면서, 아세트산이 공기 중으로 나가지 않도록 주의를 해야한다. 그리고 활성탄을 아세트산에 섞어줄 때 활성탄이 플라스크 벽에 붙으면 용액 속에 있을 때보다 흡착이 덜 일어날 수도 있다. 그것 또한 오차의 요인이 될 수 있기 때문에 주의해야한다. 또한 적정을 할 때 뷰렛의 눈금을 잘 읽어야 하고, 색이 변하는 지점에서는 아주 미량씩 천천히 넣어야(0.1ml씩 넣는다는지) 오차를 줄일 수 있을 것이다.
6. 결론
이번 실험에서는 농도가 다른 아세트산 용액을 만든 후 각각 활성탄 2g씩 섞어 흡착평형이 일어나게 하였다. 흡착은 2개의 상이 접할 때, 그 상을 구성하고 있는 성분물질이 경계면에 농축되는 현상을 말하며, 흡착평형은 흡착상태가 평형관계에 있는 것을 의미한다. 따라서 흡착평형이 이루어지기 위해서는 흡착이 된 후 일정시간이 필요하다. 이번 실험에서는 흡착평형이 일어나게 하는데 있어 시간이 약간 모자랐던 것
은 아닌가 하는 생각이 든다. 흡착평형을 시킨 후, 남아있는 아세트산의 용액을 적정하여 흡착에 사용된 아세트산의 몰수를 계산하였다.
흡착량을 계산해 보았을 때 비교적 아세트산의 농도가 높을수록 더 많은 흡착이 일어나야 하는데 오차로 인해 반드시 그렇지는 않은 것을 보아 실험이 썩 잘 된 편은 아닌 것 같다.
Freundlich 흡착등온식을 이용하여 그래프를 그려보고, 용액의 농도와 흡착되는 양의 관계에 대해 알아보니 대략적인 경향은 맞게 나왔다. 아세트산이 활성탄에 흡착되는 것은 물리흡착으로 van der waals force에 의해서 흡착된다. 농도가 높아질수록 입자간의 상호작용 포텐셜이 커지고, 이 때문에 흡착되는 양이 많아진다고 볼 수 있다.
7. 참고문헌
물리화학, 녹문당, 이재원 외 저, 2002, p.163~168, p.409~414
화학공학의 단위조작, 임굉, 임재석공저, 내하출판사, 2009, p.208~242, p.277~282
흡착공학, Motoyuki Suzuki 저, 손진언 역, 형설출판사, 2000, p. 308~344
5. 토의
이 실험에서는 각각의 플라스크에 흡착평형이 제대로 일어났는지 혹은 적정과정에 오차를 주의하며 해야한다. 오차의 원인으로는
1. 월요일날 오후에 실험을 진행한 후 수요일 낮까지 만 2일이 되지 않는 시간으로 인해 흡착평형이 제대로 일어나지 않았을 수 있다.
2. 적정에 사용하는 NaOH, 그리고 유기산인 아세트산() 수용액의 농도를 만드는데 있어 오차가 있을 수 있다.
3. 활성탄을 섞을 때 거름종이에 활성탄이 아주 약간 남아있어서 다 섞지 못한 것이 오차가 될 수 있다.
4. 활성탄을 여과할 때 비커에 물이 남아있어 오차가 생겼을 수 있다.
5. 1N 농도의 NaOH수용액을 제조할 때, 고체의 NaOH가 눈금실린더에 가라앉아 완전히 섞이지 않은 것이 오차가 될 수 있다.
6. 적정하는 과정에 뷰렛의 눈금을 읽는 것 혹은 지시약을 넣는데 있어 오차가 발생했을 수 있다.
그 외에도 이번 실험을 하면서, 아세트산이 공기 중으로 나가지 않도록 주의를 해야한다. 그리고 활성탄을 아세트산에 섞어줄 때 활성탄이 플라스크 벽에 붙으면 용액 속에 있을 때보다 흡착이 덜 일어날 수도 있다. 그것 또한 오차의 요인이 될 수 있기 때문에 주의해야한다. 또한 적정을 할 때 뷰렛의 눈금을 잘 읽어야 하고, 색이 변하는 지점에서는 아주 미량씩 천천히 넣어야(0.1ml씩 넣는다는지) 오차를 줄일 수 있을 것이다.
6. 결론
이번 실험에서는 농도가 다른 아세트산 용액을 만든 후 각각 활성탄 2g씩 섞어 흡착평형이 일어나게 하였다. 흡착은 2개의 상이 접할 때, 그 상을 구성하고 있는 성분물질이 경계면에 농축되는 현상을 말하며, 흡착평형은 흡착상태가 평형관계에 있는 것을 의미한다. 따라서 흡착평형이 이루어지기 위해서는 흡착이 된 후 일정시간이 필요하다. 이번 실험에서는 흡착평형이 일어나게 하는데 있어 시간이 약간 모자랐던 것
은 아닌가 하는 생각이 든다. 흡착평형을 시킨 후, 남아있는 아세트산의 용액을 적정하여 흡착에 사용된 아세트산의 몰수를 계산하였다.
흡착량을 계산해 보았을 때 비교적 아세트산의 농도가 높을수록 더 많은 흡착이 일어나야 하는데 오차로 인해 반드시 그렇지는 않은 것을 보아 실험이 썩 잘 된 편은 아닌 것 같다.
Freundlich 흡착등온식을 이용하여 그래프를 그려보고, 용액의 농도와 흡착되는 양의 관계에 대해 알아보니 대략적인 경향은 맞게 나왔다. 아세트산이 활성탄에 흡착되는 것은 물리흡착으로 van der waals force에 의해서 흡착된다. 농도가 높아질수록 입자간의 상호작용 포텐셜이 커지고, 이 때문에 흡착되는 양이 많아진다고 볼 수 있다.
7. 참고문헌
물리화학, 녹문당, 이재원 외 저, 2002, p.163~168, p.409~414
화학공학의 단위조작, 임굉, 임재석공저, 내하출판사, 2009, p.208~242, p.277~282
흡착공학, Motoyuki Suzuki 저, 손진언 역, 형설출판사, 2000, p. 308~344
추천자료
 절삭력 측정 실험-기계공학 응용실험
절삭력 측정 실험-기계공학 응용실험 [기계공학실험] 충격실험
[기계공학실험] 충격실험 전자공학실험- Diode 응용회로
전자공학실험- Diode 응용회로 [부산대학교 기계공학응용실험] 제트 유동장 실험
[부산대학교 기계공학응용실험] 제트 유동장 실험 [부산대학교 기계공학응용실험] 열전달 실험
[부산대학교 기계공학응용실험] 열전달 실험 [부산대학교 기계공학응용실험] 인장 실험
[부산대학교 기계공학응용실험] 인장 실험 [부산대학교 기계공학응용실험] 스트레인 게이지 응용 실험
[부산대학교 기계공학응용실험] 스트레인 게이지 응용 실험 [부산대학교 기계공학응용실험] 기계시스템운동의 가시화 & 기초진동실험
[부산대학교 기계공학응용실험] 기계시스템운동의 가시화 & 기초진동실험 홍익대학교 기계공학실험 PSD센서 실험보고서
홍익대학교 기계공학실험 PSD센서 실험보고서 홍익대학교 기계공학실험 마찰계수측정 실험보고서
홍익대학교 기계공학실험 마찰계수측정 실험보고서 홍익대학교 기계공학실험 역설계 실험보고서
홍익대학교 기계공학실험 역설계 실험보고서 홍익대학교 기계공학실험 이중열교환기 실험보고서
홍익대학교 기계공학실험 이중열교환기 실험보고서 홍익대학교 기계공학실험 증기압축식 열펌프 실험보고서
홍익대학교 기계공학실험 증기압축식 열펌프 실험보고서 기계공학응용실험 - 기계시스템 운동의 가시화 결과보고서
기계공학응용실험 - 기계시스템 운동의 가시화 결과보고서




























소개글