목차
1] Cover Page
2] Abstract
3] Table Of Contents
4] Introduction
5] Experimental
6] Results & Discussion
7] References
2] Abstract
3] Table Of Contents
4] Introduction
5] Experimental
6] Results & Discussion
7] References
본문내용
}
57.53770
2
73.825 + { 0.0176 × (-33.70478)} over {2 × 0.8239 }
73.46500
3
16.297 + {0.0264 × (-33.70478) } over {2 × 1.0355 }
15.86735
4
15.194 + { 0.0361 × (-33.70478)} over {2 ×1.2053 }
14.68925
5
17.696 + {0.0458 ×(-33.70478) } over {2 × 1.3551 }
17.12642
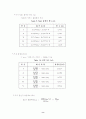
5-3-13. NaCl과 H2O물의 분 몰랄부피
Table 15. NaCl과 H2O 물의 분 몰랄 부피
NaCl의 무게(%)
A
B
1
2
18.10155
57.53770
2
4
18.10111
73.46500
3
6
18.10845
15.86735
4
8
18.11352
14.68925
5
10
18.11953
17.12642
5-4. Discussion
: 이번 실험은 조성을 미리 알고 있는 용액(NaCl-H2O계)에서의 NaCl과 H2O의 분몰 랄 부피를 결정하는 실험이었다. 용액의 조성에 따라서, 겉보기 부피와 각 물질들의 분몰랄 부피가 달라질것이라고 예상하였고, 실험을 통해서 계 산을 해본 결과 예상한것과 같이 나타내어졌다.
실험을 할 때 각각 농도가 다른 NaCl 용액을 만들어야 하는데 그 용액을 용해 시 킬 때 마그네틱 바를 사용하여 녹는 속도를 빠르게 하여 실험 시간을 단축하기도 한다. 또 육안으로는 잘 모르지만 손으로 흔들어 녹였을때는 잘 녹지 않았을 수도 있으므로 마그네틱 바를 사용하면 보다 시간도 절약하고 확실히 실험을 할 수 있 다. 마그네틱 바를 사용하여 용액을 녹일 때 비중병이 플라스크가 깨지기도 하였다.
이번 실험은 실험을 하는 것은 무척이나 간단하였지만 결과 레포트를 쓰는 과정은 제일 힘들었던 것 같다. 분 몰랄부피를 알기 위해서는 여러 가지 물리적 개념들을 알아 두어야 한다. 그래서 그런지 계산과정도 까다로웠다.
계산을 하고나니 오차가 발생하였다.
먼저 비중병 사용시 좀더 주의를 기울여야 보다 좋은 Data가 나올수 있을 것 같다. 즉, 비중병에 용액을 채울때는 용액을 넘치도록 채워 주어야 하고, 그 다음 무게 측정시에는 표면의 물기를 완전히 제거하여 주어야 한다. 비 중병에 용액을 정확히 채운다는 것도 무척이나 어려운 일이었다. 또한 실 험 전 비중병과 플라스크의 내부의 습기를 완전히 제거하지 못한 것이 잘 못이었던 것 같다.
또 실온에서의 측정은 정확한 온도가 아니었으므로 온도차를 고려해보아야 할 것같다. 또 우리가 실험을 하는 날의 습도도 실험 값이 달라지는데 영향 을 미치지 않았나 하는 추측을 해 볼 수 있다.
1. Abstract
이번 실험의 목적은 조성(무게 %로 나타낸 것)을 미리 알고 있는 여러 NaCl - H2O 용액들 중에서의 물과 소금의 분몰랄 부피를 결정하는 데 있다.
이 실험은 여러 가지 농도의 NaCl용액과 증류수를 이용하여 분 몰랄 부피를 측정하고 계산 과정을 습득할 수 있다. 계산을 하기 위해서는 이론적인 값들을 먼저 알아야 한다. 이론적인 값들은 문헌을 통해서 알 수 있으며 이론에서 나온 밀도를 이용하여 분 몰랄 부피를 계산한다.
먼저 상온과 항온조에서의 실험을 병행하여 온도가 다를 때 어떠한 결과가 나오는지 온도에 따른 비교를 할 수 있었다. 상온은 25℃였고 항온조는 35℃로 일정하게 유지하면서 실험을 수행하였다.
우선 실험 방법을 알아보자면 다음과 같다. 우선 건조한 공기가 차 있는 5개의 비중병의 무게를 단다. 그리고 각각의 비중병에 증류수를 24ml 채우고 부피선을 표시한 다음, 다시 25ml를 채우고 30 의 항온조에 3~5분 정도 넣어 뒀다가 빼어 무게를 잰다. 그 후에 5개의 비중병에 1ml의 증류수를 피펫으로 채워 넣는다. 그리고 다시 무게를 단다. 이 무게들을 가지고, 비중병 안에 들어있는 공기의 질량을 알 수 있고, 그에 따른 빈 비중병의 무게와 플라스크의 부피 또한 알 수 있게 되었다.
이 때 비중병을 건조 오븐에서 완전히 말린 후 사용했어야 하는데 우리는 실험 시간 전에 아직 마르지 않거나 이물질이 묻어있는 비중병을 다시 씻고 티슈로 닦아서 실험을 하였기 때문에 완벽히 건조되지 않은 상태에서 실험을 한 것이 오차의 원인이라고 추정되고 피펫으로 증류수를 넣었기 때문에 정확히 일정한 양을 넣었다고 보기 어려운 점도 오차의 원인으로 추정된다.
또 NaCl역시 위와 같은 방법으로 실험을 하엿다. NaCl은 100㎖의 증류수에 각각 2g, 4g, 6g, 8g, 10g 씩을 넣어 다섯 가지 농도의 용액을 만들어서 실험을 하였다. 위에서와 마찬가지로 비중병의 완전 건조의 미비함과 피펫의 정확한 사용이 오차의 원인으로 추정되며 또한 NaCl을 용해 시킬 때 그것이 이상적인 모습으로 Nacl이 H2O 와 균일하게 섞여있는지의 여부와 완전히 포화되었는가에 대한 점도 오차의 원인으로 볼 수 있겠다.
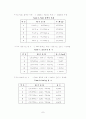
2. Table Of Contents
순 서 Page
1] Cover Page ――――――――――――――
2] Abstract ――――――――――――――
3] Table Of Contents ――――――――――
4] Introduction ―――――――――――――― 1
5] Experimental ―――――――――――――― 4
6] Results & Discussion ――――――――――― 5
7] References ―――――――――――――――― 13
6. References
1] 신형식, Laboratory Manual, 전북대학교 환경화학공학부,
Chap. 3, page. 6 ∼ 10, 2003
2] http://mbel.kaist.ac.kr/lecture/che201/2002-2.ppt
박선원, - 분몰랄부피의 측정 실험(공정시스템 연구실)
3] Rovert H. Perry, Perry's Chemical Engineers' Hand Book,
6th edition, Mc Graw-Hill, singapore, 1985
4] Gordon.M.Barrow, 물리화학, 자유아카데미, 1996,
pp 272-295
57.53770
2
73.825 + { 0.0176 × (-33.70478)} over {2 × 0.8239 }
73.46500
3
16.297 + {0.0264 × (-33.70478) } over {2 × 1.0355 }
15.86735
4
15.194 + { 0.0361 × (-33.70478)} over {2 ×1.2053 }
14.68925
5
17.696 + {0.0458 ×(-33.70478) } over {2 × 1.3551 }
17.12642
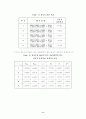
5-3-13. NaCl과 H2O물의 분 몰랄부피
Table 15. NaCl과 H2O 물의 분 몰랄 부피
NaCl의 무게(%)
A
B
1
2
18.10155
57.53770
2
4
18.10111
73.46500
3
6
18.10845
15.86735
4
8
18.11352
14.68925
5
10
18.11953
17.12642
5-4. Discussion
: 이번 실험은 조성을 미리 알고 있는 용액(NaCl-H2O계)에서의 NaCl과 H2O의 분몰 랄 부피를 결정하는 실험이었다. 용액의 조성에 따라서, 겉보기 부피와 각 물질들의 분몰랄 부피가 달라질것이라고 예상하였고, 실험을 통해서 계 산을 해본 결과 예상한것과 같이 나타내어졌다.
실험을 할 때 각각 농도가 다른 NaCl 용액을 만들어야 하는데 그 용액을 용해 시 킬 때 마그네틱 바를 사용하여 녹는 속도를 빠르게 하여 실험 시간을 단축하기도 한다. 또 육안으로는 잘 모르지만 손으로 흔들어 녹였을때는 잘 녹지 않았을 수도 있으므로 마그네틱 바를 사용하면 보다 시간도 절약하고 확실히 실험을 할 수 있 다. 마그네틱 바를 사용하여 용액을 녹일 때 비중병이 플라스크가 깨지기도 하였다.
이번 실험은 실험을 하는 것은 무척이나 간단하였지만 결과 레포트를 쓰는 과정은 제일 힘들었던 것 같다. 분 몰랄부피를 알기 위해서는 여러 가지 물리적 개념들을 알아 두어야 한다. 그래서 그런지 계산과정도 까다로웠다.
계산을 하고나니 오차가 발생하였다.
먼저 비중병 사용시 좀더 주의를 기울여야 보다 좋은 Data가 나올수 있을 것 같다. 즉, 비중병에 용액을 채울때는 용액을 넘치도록 채워 주어야 하고, 그 다음 무게 측정시에는 표면의 물기를 완전히 제거하여 주어야 한다. 비 중병에 용액을 정확히 채운다는 것도 무척이나 어려운 일이었다. 또한 실 험 전 비중병과 플라스크의 내부의 습기를 완전히 제거하지 못한 것이 잘 못이었던 것 같다.
또 실온에서의 측정은 정확한 온도가 아니었으므로 온도차를 고려해보아야 할 것같다. 또 우리가 실험을 하는 날의 습도도 실험 값이 달라지는데 영향 을 미치지 않았나 하는 추측을 해 볼 수 있다.
1. Abstract
이번 실험의 목적은 조성(무게 %로 나타낸 것)을 미리 알고 있는 여러 NaCl - H2O 용액들 중에서의 물과 소금의 분몰랄 부피를 결정하는 데 있다.
이 실험은 여러 가지 농도의 NaCl용액과 증류수를 이용하여 분 몰랄 부피를 측정하고 계산 과정을 습득할 수 있다. 계산을 하기 위해서는 이론적인 값들을 먼저 알아야 한다. 이론적인 값들은 문헌을 통해서 알 수 있으며 이론에서 나온 밀도를 이용하여 분 몰랄 부피를 계산한다.
먼저 상온과 항온조에서의 실험을 병행하여 온도가 다를 때 어떠한 결과가 나오는지 온도에 따른 비교를 할 수 있었다. 상온은 25℃였고 항온조는 35℃로 일정하게 유지하면서 실험을 수행하였다.
우선 실험 방법을 알아보자면 다음과 같다. 우선 건조한 공기가 차 있는 5개의 비중병의 무게를 단다. 그리고 각각의 비중병에 증류수를 24ml 채우고 부피선을 표시한 다음, 다시 25ml를 채우고 30 의 항온조에 3~5분 정도 넣어 뒀다가 빼어 무게를 잰다. 그 후에 5개의 비중병에 1ml의 증류수를 피펫으로 채워 넣는다. 그리고 다시 무게를 단다. 이 무게들을 가지고, 비중병 안에 들어있는 공기의 질량을 알 수 있고, 그에 따른 빈 비중병의 무게와 플라스크의 부피 또한 알 수 있게 되었다.
이 때 비중병을 건조 오븐에서 완전히 말린 후 사용했어야 하는데 우리는 실험 시간 전에 아직 마르지 않거나 이물질이 묻어있는 비중병을 다시 씻고 티슈로 닦아서 실험을 하였기 때문에 완벽히 건조되지 않은 상태에서 실험을 한 것이 오차의 원인이라고 추정되고 피펫으로 증류수를 넣었기 때문에 정확히 일정한 양을 넣었다고 보기 어려운 점도 오차의 원인으로 추정된다.
또 NaCl역시 위와 같은 방법으로 실험을 하엿다. NaCl은 100㎖의 증류수에 각각 2g, 4g, 6g, 8g, 10g 씩을 넣어 다섯 가지 농도의 용액을 만들어서 실험을 하였다. 위에서와 마찬가지로 비중병의 완전 건조의 미비함과 피펫의 정확한 사용이 오차의 원인으로 추정되며 또한 NaCl을 용해 시킬 때 그것이 이상적인 모습으로 Nacl이 H2O 와 균일하게 섞여있는지의 여부와 완전히 포화되었는가에 대한 점도 오차의 원인으로 볼 수 있겠다.
2. Table Of Contents
순 서 Page
1] Cover Page ――――――――――――――
2] Abstract ――――――――――――――
3] Table Of Contents ――――――――――
4] Introduction ―――――――――――――― 1
5] Experimental ―――――――――――――― 4
6] Results & Discussion ――――――――――― 5
7] References ―――――――――――――――― 13
6. References
1] 신형식, Laboratory Manual, 전북대학교 환경화학공학부,
Chap. 3, page. 6 ∼ 10, 2003
2] http://mbel.kaist.ac.kr/lecture/che201/2002-2.ppt
박선원, - 분몰랄부피의 측정 실험(공정시스템 연구실)
3] Rovert H. Perry, Perry's Chemical Engineers' Hand Book,
6th edition, Mc Graw-Hill, singapore, 1985
4] Gordon.M.Barrow, 물리화학, 자유아카데미, 1996,
pp 272-295
추천자료
 평형상 용질 분배
평형상 용질 분배 용질사이의 용질분배와 분배계수
용질사이의 용질분배와 분배계수 일반화학실험 엔탈피의 측정(결과리포트)
일반화학실험 엔탈피의 측정(결과리포트) 산, 염기 적정 실험
산, 염기 적정 실험 08변리사(자연과학개론)화학풀이
08변리사(자연과학개론)화학풀이 [일반화학실험] 화학 반응 속도
[일반화학실험] 화학 반응 속도 [일반화학실험] 빈혈 치료제(Iron pill)의 철(Fe)의 정량
[일반화학실험] 빈혈 치료제(Iron pill)의 철(Fe)의 정량 중화적정 실험보고서
중화적정 실험보고서 CSTR 결과
CSTR 결과 [화학실험] 산화-환원 적정 - 과망간산법(과망간산칼륨 용액의 표준화)
[화학실험] 산화-환원 적정 - 과망간산법(과망간산칼륨 용액의 표준화) 일반물리학 실험 -평형 분배
일반물리학 실험 -평형 분배 [실험 보고서] 용매추출 (Solvent Extraction) {실험 이론, Data 처리, 결과 분석}.pptx
[실험 보고서] 용매추출 (Solvent Extraction) {실험 이론, Data 처리, 결과 분석}.pptx [기본물리학] 평형의 결정-수용액에서 활성탄에 의한 유기산의 흡착 : 활성탄과 흡착의 정의...
[기본물리학] 평형의 결정-수용액에서 활성탄에 의한 유기산의 흡착 : 활성탄과 흡착의 정의... 초산에틸의 검화
초산에틸의 검화