목차
1. 실험제목
2. 실험목적
3. 이론적 고찰
▶ 분별증류관의 원리
4. 재료
5. 기구 및 기기 (이론적 고찰에 있는 그림 참조)
6. 실험방법
7. 실험 시 유의사항
8. 실험결과 및 고찰
9. 이론에 의해 예상해본 실험결과와 오차가 발생한 부분
10. 오차의 이유
11. 참고문헌
2. 실험목적
3. 이론적 고찰
▶ 분별증류관의 원리
4. 재료
5. 기구 및 기기 (이론적 고찰에 있는 그림 참조)
6. 실험방법
7. 실험 시 유의사항
8. 실험결과 및 고찰
9. 이론에 의해 예상해본 실험결과와 오차가 발생한 부분
10. 오차의 이유
11. 참고문헌
본문내용
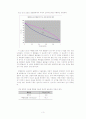
증류량 5ml 이전의 측정치는 구하지 못하였다. 그러나 그 후의 증류된 메틸알코올의 양과 온도 관계를 살펴보면 초기에는 일정한 속도로 증류가 되었으나, 시간이 흐르고 온도가 높아질 수 록 증류되는 속도가 점점 줄어들면서 비교적 높은 온도까지 올라가서야 일정량의 증류된 메틸알코올을 얻어낼 수가 있었다. 메틸알코올의 끓는점인 64.7℃를 훨씬 넘긴 82℃가 되었을 때 실험을 중단했음에도 불구하고, 처음에 둥근 플라스크에 넣었던 메틸알코올 15ml에는 못 미치는 13ml의 증류된 메틸알코올을 얻을 수 있었다.
상온에서의 액체 온도 : 26℃
증류된 양(ml)
측정 온도 (℃)
0
66 (끓기 시작)
5
72
7
74
9
76
11
77
13
82
9. 이론에 의해 예상해본 실험결과와 오차가 발생한 부분
이론에 의하면 50:50 메탄올-물의 액체 혼합물은 76℃에서 끓기 시작하지만 실제로는 66℃를 가리키는 지점에서 끓기 시작했다. 이는 온도계의 위치가 유리관 위쪽에 있기 때문에 증기가 올라오면서 어느 정도 식었기 때문이다.
또한 증류된 메탄올은 실험에 사용했던 메탄올보다 적게 증류되었다. 그 사이의 오차를 알아보았다.
비교적 큰 오차가 발생하였음을 알 수 있었다. 이는 아직 모든 메탄올이 증류되지 못하였을 가능성이 있으나, 그 가능성은 희박하고 유리관에 붙어있던 액체나 기체가 미쳐 메스실린더로 빠져나오지 못했을 가능성이나, 유리관이 완전히 밀봉되지 못하여 공기 중으로 빠져나갔을 가능성을 생각해 볼 수 있다.
10. 오차의 이유
적어도 실험에서는 3번이상의 측정을 하여 그 평균값을 측정해야하지만, 시간 관계 상 단 1번의 실험을 하여 분별증류를 하였으므로 오차가 발생할 수 있다.
메탄올-물 혼합물과 온도계와의 거리가 멀리 떨어져 있었으므로 실제 혼합물의 온도는 알 수 없었으므로, 혼합물의 온도는 이미 물의 끓는점인 100℃를 넘겼을 수도 있다.
미량의 물 수증기도 증류되어서 빠져나왔을 수도 있다.
유리관이 완전히 밀봉되지 않아서 일부의 기체가 빠져나갔을 수도 있다.
완전히 흘러내리지 못한 액체나 기체가 유리관에 붙어있을 수 있다.
11. 참고문헌
일반화학 fourth edition, Oxtoby Freeman Block 원저 (화학교재편찬위원회 옮김), Thomson, 2005
교사를 위한 신나는 화학실험, Bassam Z. Skakhashiri 원저 (김경숙 외 9명 공역), 自由아카데미, 2002
상온에서의 액체 온도 : 26℃
증류된 양(ml)
측정 온도 (℃)
0
66 (끓기 시작)
5
72
7
74
9
76
11
77
13
82
9. 이론에 의해 예상해본 실험결과와 오차가 발생한 부분
이론에 의하면 50:50 메탄올-물의 액체 혼합물은 76℃에서 끓기 시작하지만 실제로는 66℃를 가리키는 지점에서 끓기 시작했다. 이는 온도계의 위치가 유리관 위쪽에 있기 때문에 증기가 올라오면서 어느 정도 식었기 때문이다.
또한 증류된 메탄올은 실험에 사용했던 메탄올보다 적게 증류되었다. 그 사이의 오차를 알아보았다.
비교적 큰 오차가 발생하였음을 알 수 있었다. 이는 아직 모든 메탄올이 증류되지 못하였을 가능성이 있으나, 그 가능성은 희박하고 유리관에 붙어있던 액체나 기체가 미쳐 메스실린더로 빠져나오지 못했을 가능성이나, 유리관이 완전히 밀봉되지 못하여 공기 중으로 빠져나갔을 가능성을 생각해 볼 수 있다.
10. 오차의 이유
적어도 실험에서는 3번이상의 측정을 하여 그 평균값을 측정해야하지만, 시간 관계 상 단 1번의 실험을 하여 분별증류를 하였으므로 오차가 발생할 수 있다.
메탄올-물 혼합물과 온도계와의 거리가 멀리 떨어져 있었으므로 실제 혼합물의 온도는 알 수 없었으므로, 혼합물의 온도는 이미 물의 끓는점인 100℃를 넘겼을 수도 있다.
미량의 물 수증기도 증류되어서 빠져나왔을 수도 있다.
유리관이 완전히 밀봉되지 않아서 일부의 기체가 빠져나갔을 수도 있다.
완전히 흘러내리지 못한 액체나 기체가 유리관에 붙어있을 수 있다.
11. 참고문헌
일반화학 fourth edition, Oxtoby Freeman Block 원저 (화학교재편찬위원회 옮김), Thomson, 2005
교사를 위한 신나는 화학실험, Bassam Z. Skakhashiri 원저 (김경숙 외 9명 공역), 自由아카데미, 2002