목차
1. 서론
2. 연료전지이론
3. 실험방법및 실험
4. 결과
5. 결론
6.참고문헌
2. 연료전지이론
3. 실험방법및 실험
4. 결과
5. 결론
6.참고문헌
본문내용
량은 이다. 실험에서 생성된 수소의 부피는 이므로, 패러데이 효율은 91% 이다.
4.3. 수소연료전지의 전력측정
수소기체가 전기에너지로 변환하는 전력특성을 측정하기위해서 저항에 따른 전압과 전류를 측정한다. 일정한 값의 결과를 얻기 위해서 각 측정값의 사이에는 약 20초 간 여유를 둔다. 표 3은 저항에 따른 전류-전압 특성과 수소 화학 전지의 전력을 나타낸 것으로 부하저항이 2Ω에서 최대출력을 나타내었다.
화학 전지의 에너지 효율과 패러데이 효율을 산출하기 위해 전해조의 수소 저장 탱크의 출력 단자를 화학 전지의 입력 단자에 연결하였다. 화학 전지의 출력 단자를 닫고 수소를 만큼 채운 후 시스템을 환기시키기 위해서 화학 전지의 출력 단자를 연다. 에너지 효율을 결정하기 위해 2Ω의 부하저항을 사용하였다. 화학 전지와 저항 사이의 회로를 재연결한 순간부터 수소의 부피가 일정하게 감소되는 양에 따른 시간과 전압, 전류를 측정하였고 그 결과는 표 4와 같다.
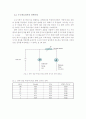
그림 8. 전류-전압 특성과 PEM 화학 전지의 전력 회로도
표 3. 전류-전압 특성과 PEM 화학 전지의 전력
R(Ω)
V[volts]
I[A]
P[W] P=V×I
100
0.89
0.02
0.018
33
0.86
0.05
0.043
10
0.82
0.06
0.049
3.3
0.73
0.15
0.109
2
0.71
0.54
0.383
1
0.48
0.67
0.322
표 4. 수소기체의 부피 감소에 따른 시간과 전압-전류
V[cm3]
t[s]
V[volts]
I[A]
20
0
0.71
0.53
15
104
0.71
0.53
10
203
0.71
0.53
5
308
0.71
0.53
0
414
0.71
0.53
수소기체의 에너지변환 효율은 수소의 최대 발열량에 대한 전기에너지 변환 효율로 다음 식으로 계산한다.
여기서, 는 수소 발열량(), 는 단위 부피당 생성된 수소 기체, 는 전압, 는 전류 및 는 초 단위의 시간 이다. 수소 기체에 대한 에너지변환 효율 는 70%로 계산 되었다.
태양전지효율에 관한 결과 분석은 다음과 같이 생각할 수 있다. 보통 다결정 실리콘으로 된 태양전지들의 효율이 15% 범위까지 상용화된 것으로 보고 되고 있는데[5], 10%에서 결정된 값은 다소 적은 값으로 한 여름날에 실험한다면 증가하리라고 본다. 태양전지판에 부딪치는 모든 광자들이 전하 운반체로 전환되는 것도 아니고, 빛의 일부는 표면에 닿는 즉시 반사되기도 한다. 또한 전하 운반체들의 재결합과 태양전지의 내부 저항에 의한 반도체 내의 저항 손실 등과 같은 전기적인 손실이 효율 저하의 요인이라고 생각된다.
전해조의 전압-전류에 따른 특성 결과 분석에서는 표 1에서와 같이 일정 전압에 이르기 전까지는 전류가 흐르지 않음을 확인할 수 있다. 이론적인 분해전압은 1.23V인데 실험 결과에 따르면 1.5V에서 물 분해가 발생한다. 이유는 실제로는 전이 저항 때문에 분해 전압은 과전압의 결과로써 이론값보다 크기 때문이다. 분해 전압의 이론과 실제 값 사이의 차이는 전극 물질의 합성과 종류, 전해조의 온도 등 여러 변수에 의존한다. 전해조에서의 수소에너지변환 효율은 78%이다. 이것은 전해조에 의해 사용된 전기적인 에너지의 78%가 수소 기체로 저장된다는 것을 의미한다. 손실은 전극 주변의 저항성분 때문에 과전압으로부터 발생한다. 과전압은 일반적으로 실제 분해 전압과 이론 전압과의 편차에서 발생한다. 전해조 전지의 내부 저항과 빛의 산란은 전지 내에서 가스의 손실로 나타난다. 또한 PEM 전해조의 패러데이 효율에서 생기는 손실 9%도 포함된다. 이것은 전지 내 기체의 확산 손실에 기인하며, 확산 손실은 전해조의 얇은 막을 통하여 기체의 일부가 확산되고 촉매와 반응하여 물을 형성 시킨다는 사실로부터 발생한다.
수소연료의 효율 측정에서는 화학 에너지가 내는 최대 출력 전력은 0.71V, 0.54A로 0.4W이다. 수소의 발열량과 비교해 보면 수소화학 전지의 에너지변환 효율은 70%이고, 패러데이 효율은 100%로 예상 값과 일치하였다.
5. 결 론
수소제조기술의 경우 태양광 및 촉매에 의한 물의 전해방법 등 다양한 방법이 제안 되고 있으나, 소형의 연료전지로 주목 받고 있는 것은 메탄올 연료전지(DMFC) 이다, 이 연료전지는 연료가 수소가 아닌 메탄올(CH2OH)로 사용하는데, 상온에서 액체이고 용기에 넣을 수 있기 때문에 운반, 판매가 용이하여 사업화가 활발하게 진행되고 있다. 이런 형태의 수소연료전지가 휴대전화나 노트북 같은 기기의 리튬 전원 대신 이용될 것으로 보인다. 본 논문에서는 태양전지를 전력원으로 하고 전해조 내에서 백금을 촉매로 한 두 전극 사이에서 물을 전기분해하여 수소를 모으고, 이 수소를 양성자교환 전해질막으로 만든 연료전지를 이용해 전기를 발생시켰다. 수소가 공급되는 전극에서도 백금 촉매의 도움으로 수소를 양성자와 음전하로 분해하고, 이 중 양성자는 전해질막으로 이동하여 음극의 산소와 결합함으로써 물이 되고, 음전하는 전선을 따라 음극으로 이동하게 되는데 이것이 바로 수소전지의 전력원이 된다. 이러한 고체 고분자격막형 수소연료전지장치에서 태양전지의 효율은 10%였고, 물을 전기분해하는 전해조의 효율은 1.9V, 1.73A에서 78%이었으며, 수소연료전지의 에너지변환 효율은 70%이었다. 이러한 소형의 태양광판 수소연료전지는 야외 전등과 같은 소전력원에 널리 활용되리라 본다.
6. 참고문헌
[1] 김종원 외, 수소에너지, 아진출판 (2005).
[2] Newton Graphic Science Magazine, 계몽사, Vol.22, Nov. (2006) p.28.
[3] C. Voigt, S. Hoeller, U. Kueter, Fuel Cell Technology for Classroom. Instruction, Wassserstoff-Energi-Systeme GmbH, Norderstedt (2005).
[4] 이병규 외, 에너지와 환경, 녹문당 (2005).
[5] 김경해, 이준신, 물리학과 첨단기술, 한국물리학회, July (2006) p.17.
[6] 연료전지, 산업자원부한국산업기술재단 (2006).
4.3. 수소연료전지의 전력측정
수소기체가 전기에너지로 변환하는 전력특성을 측정하기위해서 저항에 따른 전압과 전류를 측정한다. 일정한 값의 결과를 얻기 위해서 각 측정값의 사이에는 약 20초 간 여유를 둔다. 표 3은 저항에 따른 전류-전압 특성과 수소 화학 전지의 전력을 나타낸 것으로 부하저항이 2Ω에서 최대출력을 나타내었다.
화학 전지의 에너지 효율과 패러데이 효율을 산출하기 위해 전해조의 수소 저장 탱크의 출력 단자를 화학 전지의 입력 단자에 연결하였다. 화학 전지의 출력 단자를 닫고 수소를 만큼 채운 후 시스템을 환기시키기 위해서 화학 전지의 출력 단자를 연다. 에너지 효율을 결정하기 위해 2Ω의 부하저항을 사용하였다. 화학 전지와 저항 사이의 회로를 재연결한 순간부터 수소의 부피가 일정하게 감소되는 양에 따른 시간과 전압, 전류를 측정하였고 그 결과는 표 4와 같다.
그림 8. 전류-전압 특성과 PEM 화학 전지의 전력 회로도
표 3. 전류-전압 특성과 PEM 화학 전지의 전력
R(Ω)
V[volts]
I[A]
P[W] P=V×I
100
0.89
0.02
0.018
33
0.86
0.05
0.043
10
0.82
0.06
0.049
3.3
0.73
0.15
0.109
2
0.71
0.54
0.383
1
0.48
0.67
0.322
표 4. 수소기체의 부피 감소에 따른 시간과 전압-전류
V[cm3]
t[s]
V[volts]
I[A]
20
0
0.71
0.53
15
104
0.71
0.53
10
203
0.71
0.53
5
308
0.71
0.53
0
414
0.71
0.53
수소기체의 에너지변환 효율은 수소의 최대 발열량에 대한 전기에너지 변환 효율로 다음 식으로 계산한다.
여기서, 는 수소 발열량(), 는 단위 부피당 생성된 수소 기체, 는 전압, 는 전류 및 는 초 단위의 시간 이다. 수소 기체에 대한 에너지변환 효율 는 70%로 계산 되었다.
태양전지효율에 관한 결과 분석은 다음과 같이 생각할 수 있다. 보통 다결정 실리콘으로 된 태양전지들의 효율이 15% 범위까지 상용화된 것으로 보고 되고 있는데[5], 10%에서 결정된 값은 다소 적은 값으로 한 여름날에 실험한다면 증가하리라고 본다. 태양전지판에 부딪치는 모든 광자들이 전하 운반체로 전환되는 것도 아니고, 빛의 일부는 표면에 닿는 즉시 반사되기도 한다. 또한 전하 운반체들의 재결합과 태양전지의 내부 저항에 의한 반도체 내의 저항 손실 등과 같은 전기적인 손실이 효율 저하의 요인이라고 생각된다.
전해조의 전압-전류에 따른 특성 결과 분석에서는 표 1에서와 같이 일정 전압에 이르기 전까지는 전류가 흐르지 않음을 확인할 수 있다. 이론적인 분해전압은 1.23V인데 실험 결과에 따르면 1.5V에서 물 분해가 발생한다. 이유는 실제로는 전이 저항 때문에 분해 전압은 과전압의 결과로써 이론값보다 크기 때문이다. 분해 전압의 이론과 실제 값 사이의 차이는 전극 물질의 합성과 종류, 전해조의 온도 등 여러 변수에 의존한다. 전해조에서의 수소에너지변환 효율은 78%이다. 이것은 전해조에 의해 사용된 전기적인 에너지의 78%가 수소 기체로 저장된다는 것을 의미한다. 손실은 전극 주변의 저항성분 때문에 과전압으로부터 발생한다. 과전압은 일반적으로 실제 분해 전압과 이론 전압과의 편차에서 발생한다. 전해조 전지의 내부 저항과 빛의 산란은 전지 내에서 가스의 손실로 나타난다. 또한 PEM 전해조의 패러데이 효율에서 생기는 손실 9%도 포함된다. 이것은 전지 내 기체의 확산 손실에 기인하며, 확산 손실은 전해조의 얇은 막을 통하여 기체의 일부가 확산되고 촉매와 반응하여 물을 형성 시킨다는 사실로부터 발생한다.
수소연료의 효율 측정에서는 화학 에너지가 내는 최대 출력 전력은 0.71V, 0.54A로 0.4W이다. 수소의 발열량과 비교해 보면 수소화학 전지의 에너지변환 효율은 70%이고, 패러데이 효율은 100%로 예상 값과 일치하였다.
5. 결 론
수소제조기술의 경우 태양광 및 촉매에 의한 물의 전해방법 등 다양한 방법이 제안 되고 있으나, 소형의 연료전지로 주목 받고 있는 것은 메탄올 연료전지(DMFC) 이다, 이 연료전지는 연료가 수소가 아닌 메탄올(CH2OH)로 사용하는데, 상온에서 액체이고 용기에 넣을 수 있기 때문에 운반, 판매가 용이하여 사업화가 활발하게 진행되고 있다. 이런 형태의 수소연료전지가 휴대전화나 노트북 같은 기기의 리튬 전원 대신 이용될 것으로 보인다. 본 논문에서는 태양전지를 전력원으로 하고 전해조 내에서 백금을 촉매로 한 두 전극 사이에서 물을 전기분해하여 수소를 모으고, 이 수소를 양성자교환 전해질막으로 만든 연료전지를 이용해 전기를 발생시켰다. 수소가 공급되는 전극에서도 백금 촉매의 도움으로 수소를 양성자와 음전하로 분해하고, 이 중 양성자는 전해질막으로 이동하여 음극의 산소와 결합함으로써 물이 되고, 음전하는 전선을 따라 음극으로 이동하게 되는데 이것이 바로 수소전지의 전력원이 된다. 이러한 고체 고분자격막형 수소연료전지장치에서 태양전지의 효율은 10%였고, 물을 전기분해하는 전해조의 효율은 1.9V, 1.73A에서 78%이었으며, 수소연료전지의 에너지변환 효율은 70%이었다. 이러한 소형의 태양광판 수소연료전지는 야외 전등과 같은 소전력원에 널리 활용되리라 본다.
6. 참고문헌
[1] 김종원 외, 수소에너지, 아진출판 (2005).
[2] Newton Graphic Science Magazine, 계몽사, Vol.22, Nov. (2006) p.28.
[3] C. Voigt, S. Hoeller, U. Kueter, Fuel Cell Technology for Classroom. Instruction, Wassserstoff-Energi-Systeme GmbH, Norderstedt (2005).
[4] 이병규 외, 에너지와 환경, 녹문당 (2005).
[5] 김경해, 이준신, 물리학과 첨단기술, 한국물리학회, July (2006) p.17.
[6] 연료전지, 산업자원부한국산업기술재단 (2006).