목차
1.측정 원리
2.실험기구
3.실험시약
표정과정
4.실험과정
5.농도 계산
⁂결과및토론
2.실험기구
3.실험시약
표정과정
4.실험과정
5.농도 계산
⁂결과및토론
본문내용
25-50
50-90
90-130
130-210
210-330
330-445
445-
5.5
5.1
5.0
4.9
4.8
4.7
4.6
4.5
50
100
50
100
50
50
50
25
0.001
0.002
0.002
0.02
0.02
0.02
0.02
0.02
④보다 낮은 알칼리도를 위해 필요한 만큼 적정액을 희석한다. 희석시킨 적정액을 위해 새로운 뷰렛을 사용한다.
2)알칼리도
①여과하지 않은 시료 100ml을 측정하여 비이커로 옮긴다. 알칼리도가 높고 적정량이 25ml이상이 사용된다면, 100ml미만의 시료를 사용한다. 자석바와 pH전극을 비이커에 넣고 자석교반기의 가동시킨다.
다른 방법으로 색 지시약을 사용할 수 있다.
②초기 pH, 시료량 그리고 시료의 온도를 기록한다.
③초기 pH가 8.3이상이면 0.02N 황산용액으로 적정하고 적정량을 기록한다. 이는 페놀프탈레인 종말점이 된다.
④pH가 4.5가될 때까지 적정하고 적정량을 기록한다. 이는 총알칼리도의 종말점이다.
5.농도 계산
여기서 A : 시료를 위해 사용된 표준 황산 용액 (ml)
B : 바탕실험을 위해 사용된 표준 황산 용액 (ml)
N : 황산의 노르말 농도
결과
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
보은하수
6.68
6.42
6.26
6.12
5.96
5.84
5.69
5.56
5.39
5.19
4.92
4.5
침출수
6.82
6.65
6.58
6.51
6.41
6.31
6.16
6.06
5.97
5.86
5.74
5.63
5.49
5.32
5.15
4.96
4.75
4.54
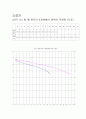
pH가 4.5 될 때 까지의 0.02N황산 용액의 적정량 (도표)
보은하수의 알칼리도
A : 11ml
B : l
N : 0.02N
보은 하수의 알칼리도 :
즉
침출수의 알칼리도
A : 17ml
B :
N : 0.02N
침출수의 알칼리도 :
즉
토론
알칼리도정의
수중에 함유 돼 있는 알칼리분을 탄산칼슘(CaCO3)으로 환산하여 1L중의 mg량으로 표시한 것이다. 알칼리분이란 용존하는 탄산염류(CO3), 탄산수소염류(HCO3), 수산화물류(OH) 등을 말한다.
즉, 산을 중화시키는데 필요한 능력을 말한다. 따라서 일정한 농도의 황산을 주입하면서 결정하게 되는데 이때 주입된 산의 양을 CaCO3값으로 환산된 것을 말한다. 자연수의 알칼리도는 일반적으로 탄산수소염(토양의 염기성 물질과 이산화탄소와의 반응에 의해 상당한 양이 생성)이며, 탄산염, 수산화물을 함유하는 일은 적다.
그밖에 약한 산의 염들, 즉 붕산염, 규산염, 인산염 등이 소량 존재하기도 한다. 생물학적 산화가 대단히 어려운 몇가지 유기산. 예를 들어 부식산(humic acid)과 같은 것들은 자연수에 알칼리도를 나타내게 하는 염을 생성한다. 오염된 물이나 혐기성 상태의 물에서는 아세트산. 프로히온산. 황화수소와 같은 약한 산의 염들이 생성될 수 있으며. 이들은 알칼리도를 증가시킨다. 경우에 따라서는 암모니아나 수산화물들이 물의 전 알칼리도를 나타내는 경우도 있다.
알칼리도 이론
알칼리도란 수중에 수산화물(OH-), 탄산염(CO3--), 중탄산염의 형으로 함유되어 있는 알카리분을(대이온은 Ca++, Mg++, NH4+ 등) 이에 대응하는 탄산칼슘(CaCO3) 1ℓ중의 ㎎량, 즉 ppm으로 나타낸 것으로 수산화물로 된 알카리도를 수산기 알칼리도(Hydroxide Alkalinity), 탄산염에 인한 알칼리도를 탄산알카리도(carbonate alkalinity), 중탄산염으로부터의 알칼리도를 중탄산알카리도(bicarbonate alkalinity)라 한다.
따라서 메틸오렌지(pH 약 4.5) 또는 폐놀프탈레인(pH 약 8.4)을 써서 종말점을 구한다. 전자로서 얻은 값을 메틸오렌지 알칼리도 또는 총알칼리도, 후자에 의한 측정치를 폐놀프탈레인 알칼리도라 부른다.
알칼리도 PH 측정값이 침출수가 보은하수보다 농도가 높게 나왔습니다. 침출수에 유기물질이 많은것을 알게 되었습니다. 저희조에서 침출수 실험을 할 때 첫 번째 실험에서는 0.02N황산 용액을 500ml를 넘게 넣어도 pH값이 6정도 나왔습니다. 다시 조교에게 다시 침출수를 받아서 할 때는 약 17ml를 넣으니 4.5 정도의 pH값이 나왔습니다. 그렇게 까지 값이 틀리게 나온 이유를 알고 싶습니다. 시료는 반드시 폴리에틸렌(PE)병에 보관해야 한다는 것이 산성법(담수) 실험 시약 과망간산칼륨 용액을 갈색병에 담는것과 같은 이유인지를 알고 싶습니다.
50-90
90-130
130-210
210-330
330-445
445-
5.5
5.1
5.0
4.9
4.8
4.7
4.6
4.5
50
100
50
100
50
50
50
25
0.001
0.002
0.002
0.02
0.02
0.02
0.02
0.02
④보다 낮은 알칼리도를 위해 필요한 만큼 적정액을 희석한다. 희석시킨 적정액을 위해 새로운 뷰렛을 사용한다.
2)알칼리도
①여과하지 않은 시료 100ml을 측정하여 비이커로 옮긴다. 알칼리도가 높고 적정량이 25ml이상이 사용된다면, 100ml미만의 시료를 사용한다. 자석바와 pH전극을 비이커에 넣고 자석교반기의 가동시킨다.
다른 방법으로 색 지시약을 사용할 수 있다.
②초기 pH, 시료량 그리고 시료의 온도를 기록한다.
③초기 pH가 8.3이상이면 0.02N 황산용액으로 적정하고 적정량을 기록한다. 이는 페놀프탈레인 종말점이 된다.
④pH가 4.5가될 때까지 적정하고 적정량을 기록한다. 이는 총알칼리도의 종말점이다.
5.농도 계산
여기서 A : 시료를 위해 사용된 표준 황산 용액 (ml)
B : 바탕실험을 위해 사용된 표준 황산 용액 (ml)
N : 황산의 노르말 농도
결과
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
보은하수
6.68
6.42
6.26
6.12
5.96
5.84
5.69
5.56
5.39
5.19
4.92
4.5
침출수
6.82
6.65
6.58
6.51
6.41
6.31
6.16
6.06
5.97
5.86
5.74
5.63
5.49
5.32
5.15
4.96
4.75
4.54
pH가 4.5 될 때 까지의 0.02N황산 용액의 적정량 (도표)
보은하수의 알칼리도
A : 11ml
B : l
N : 0.02N
보은 하수의 알칼리도 :
즉
침출수의 알칼리도
A : 17ml
B :
N : 0.02N
침출수의 알칼리도 :
즉
토론
알칼리도정의
수중에 함유 돼 있는 알칼리분을 탄산칼슘(CaCO3)으로 환산하여 1L중의 mg량으로 표시한 것이다. 알칼리분이란 용존하는 탄산염류(CO3), 탄산수소염류(HCO3), 수산화물류(OH) 등을 말한다.
즉, 산을 중화시키는데 필요한 능력을 말한다. 따라서 일정한 농도의 황산을 주입하면서 결정하게 되는데 이때 주입된 산의 양을 CaCO3값으로 환산된 것을 말한다. 자연수의 알칼리도는 일반적으로 탄산수소염(토양의 염기성 물질과 이산화탄소와의 반응에 의해 상당한 양이 생성)이며, 탄산염, 수산화물을 함유하는 일은 적다.
그밖에 약한 산의 염들, 즉 붕산염, 규산염, 인산염 등이 소량 존재하기도 한다. 생물학적 산화가 대단히 어려운 몇가지 유기산. 예를 들어 부식산(humic acid)과 같은 것들은 자연수에 알칼리도를 나타내게 하는 염을 생성한다. 오염된 물이나 혐기성 상태의 물에서는 아세트산. 프로히온산. 황화수소와 같은 약한 산의 염들이 생성될 수 있으며. 이들은 알칼리도를 증가시킨다. 경우에 따라서는 암모니아나 수산화물들이 물의 전 알칼리도를 나타내는 경우도 있다.
알칼리도 이론
알칼리도란 수중에 수산화물(OH-), 탄산염(CO3--), 중탄산염의 형으로 함유되어 있는 알카리분을(대이온은 Ca++, Mg++, NH4+ 등) 이에 대응하는 탄산칼슘(CaCO3) 1ℓ중의 ㎎량, 즉 ppm으로 나타낸 것으로 수산화물로 된 알카리도를 수산기 알칼리도(Hydroxide Alkalinity), 탄산염에 인한 알칼리도를 탄산알카리도(carbonate alkalinity), 중탄산염으로부터의 알칼리도를 중탄산알카리도(bicarbonate alkalinity)라 한다.
따라서 메틸오렌지(pH 약 4.5) 또는 폐놀프탈레인(pH 약 8.4)을 써서 종말점을 구한다. 전자로서 얻은 값을 메틸오렌지 알칼리도 또는 총알칼리도, 후자에 의한 측정치를 폐놀프탈레인 알칼리도라 부른다.
알칼리도 PH 측정값이 침출수가 보은하수보다 농도가 높게 나왔습니다. 침출수에 유기물질이 많은것을 알게 되었습니다. 저희조에서 침출수 실험을 할 때 첫 번째 실험에서는 0.02N황산 용액을 500ml를 넘게 넣어도 pH값이 6정도 나왔습니다. 다시 조교에게 다시 침출수를 받아서 할 때는 약 17ml를 넣으니 4.5 정도의 pH값이 나왔습니다. 그렇게 까지 값이 틀리게 나온 이유를 알고 싶습니다. 시료는 반드시 폴리에틸렌(PE)병에 보관해야 한다는 것이 산성법(담수) 실험 시약 과망간산칼륨 용액을 갈색병에 담는것과 같은 이유인지를 알고 싶습니다.





























소개글