목차
LIST OF CONTENTS
LIST OF TABLES
LIST OF FIGURES
1. ABSTRACT
2. INTRODUCTION
2.1 실험목적
2.2 실험이론
2.3 실험주의사항
2.4 시약의 특성
3. EXPERIMENTAL
3.1 기구 및 시약
3.2 실험절차
4. RESULTS
4.1 Raw data
4.2 Results
5. DISCUSSION
6. REFERENCE
LIST OF TABLES
LIST OF FIGURES
1. ABSTRACT
2. INTRODUCTION
2.1 실험목적
2.2 실험이론
2.3 실험주의사항
2.4 시약의 특성
3. EXPERIMENTAL
3.1 기구 및 시약
3.2 실험절차
4. RESULTS
4.1 Raw data
4.2 Results
5. DISCUSSION
6. REFERENCE
본문내용
넣어주고 파라필름으로 입구를 막아주었다. 위의 용액들이 평형에 도달하도록 충분한 시간동안 방치한 후 EP튜브에 넣고 13000rpm의 속도로 5분 동안 원심분리 하였다. 원심분리 후 용액의 중층부를 재취하여 용기에 넣었다.
UV측정에서는 처음에 석영큐벳에 증류수를 넣어 기준을 잡아주었다. 그 다음 준비한 표준용액들을 석영큐벳에 담아 UV측정기에 넣어 흡광도를 측정하였다. 이 때 그래프가 완만하게 그려지지 않거나 측정범위를 경우 다시 측정하거나 용액을 희석시켜 측정하였다. 매 측정마다 석영큐벳을 세척하며 활성탄을 넣은 용액도 같은 방법으로 측정하였다. 측정이 완료되면 표준용액의 농도에 따른 흡광도 그래프를 그린 다음 그래프의 방정식을 구해 활성탄을 넣은 염료의 농도를 구하였다.
4. RESULTS
4.1 Raw data
Table 2. 표준용액 농도 vs 흡광도
표준용액(ppm)
흡광도
5
0.380554
10
0.7828
25
1.79341
50
4.25336
100
7.50048
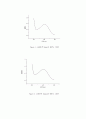
Figure 1. 표준용액 5ppm의 흡광도 그래프
Figure 2. 표준용액 10ppm의 흡광도 그래프
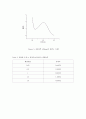
Figure 3. 표준용액 25ppm의 흡광도 그래프
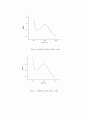
Figure 4. 표준용액 50ppm의 흡광도 그래프
Figure 5. 표준용액 100ppm의 흡광도 그래프
Table 3. 활성탄 무게 vs 흡광도(1/10희석)-샘플용액
활성탄(g)
흡광도
0.25
0.94079
0.5
1.06938
1
0.99915
1.2
1.10402
1.6
0.98972
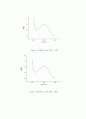
Figure 6. 샘플용액 0.25g의 흡광도 그래프
Figure 7. 샘플용액 0.5g의 흡광도 그래프
Figure 8. 샘플용액 1g의 흡광도 그래프
Figure 9. 샘플용액 1.2g의 흡광도 그래프
Figure 10. 샘플용액 1.6g의 흡광도 그래프
4.2 Results
4.2.1 염료 용액의 농도
Table 2.로부터 농도에 대한 흡광도 그래프를 그린 후 방정식을 세운다.
Figure 11. 표준용액의 농도 vs 흡광도 그래프
y = ax + b
Intercept(절편) 0.05413
Slope(기울기) 0.076
따라서 y=(0.076)x+0.05413 이다.
이 방정식으로부터 샘플용액의 농도를 구한다.
1/10배로 희석했으므로 구한 농도에 10배를 해준다.
(x : 농도, y : 흡광도)
Table 4. 활성탄 무게 vs 염료용액의 농도
활성탄(g)
농도(ppm)
0.25
116.666
0.5
133.586
1
124.345
1.2
138.143
1.6
123.104
계산과정 예)
Figure 12. 활성탄 무게 vs 염료용액의 농도 그래프
4.2.2 염료용액의 흡착량
q : 흡착량(mg/g), Co : 염료용액의 처음 농도(ppm), Cf : 염료용액의 평형농도(ppm),
V : 염료 용액의 부피(L), M : 활성탄의 무게(g)
Table 5. 활성탄 무게 대 염료용액의 흡착량
활성탄(g)
흡착량(mg/g)
0.25
6.6668
0.5
1.6414
1
1.2828
1.2
0.4940
1.6
0.8405
계산과정 예)
Figure 13. 활성탄 무게 vs 흡착량 그래프
5. DISCUSSION
이번 ‘흡착 평형’이라는 실험은 일정한 온도에서 염료의 활성탄 표면에서의 흡착 성질을 알아보기 위한 것이다.
실험 결과 표준 용액의 농도 vs 흡광도 그래프를 fitting하여 y=ax+b의 방정식을 얻었다. 여기서 기울기는 a는 0.076, y 절편 b는 0.05413이다. 그리고 이 방정식에 샘플용액의 흡광도 측정값을 대입하여 샘플용액의 농도를 구하였다. 대입결과 활성탄 0.25g의 경우에 염료 용액의 농도는 116.666ppm이고, 0.5g, 1.0g, 1.2g, 1.6g경우 각각 133.586ppm, 124.345ppm, 138.143ppm, 123.104ppm이다. 마지막으로 이 데이터 값을 mass balance하면 각각의 활성탄 양에 대한 흡착량은 6.6668mg/g, 1.6414mg/g, 1.2828mg/g, 0.4940mg/g, 0.8405mg/g이었다.
데이터 처리 결과 활성탄의 무게가 증가함에 따라 염료의 농도가 감소해야 하는데 그러지 못하였다. 또한 흡착량은 증가해야하는데 대체로 감소하는 경향을 보여 매우 큰 오차가 발생하였다.
오차의 원인에는 마이크로피펫 사용을 잘못 사용한 경우가 있다. 마이크로피펫을 사용하기 전에 사용법을 충분히 익혀야 한다. 그리고 마이크로피펫을 사용할 때 너무 세게 누르면 용액이 더 많이 취해지게 되는데 이를 주의해야 한다. 또 원심분리액을 취할 때 산소를 취해 기포가 발생하지 않도록 해야 한다.
또한 용액이 충분히 평형상태에 도달하지 않은 경우에도 오차가 발생한다. 약 14시간 정도 용액을 평형에 도달하도록 하였는데 염료용액이 활성탄 표면에 충분히 흡착되어 평형에 이르도록 일주일 정도 충분히 시간을 두어야 한다. 이번 실험의 오차의 대부분은 용액이 평형에 도달하지 못해 생긴 것 같다.
석영큐벳을 이용하여 UV를 측정할 때는 석영큐벳에 지문이나 먼지가 묻지 않도록 해야 하며, 큐벳 안에 넣은 용액에 불순물이 섞이지 않도록 주의해야 한다. 이 실험은 미세한 양에 의해 데이터 값이 변하므로 염료 용액이나 증류수에 불순물이 섞이지 않도록 해야 한다. 활성탄을 넣은 염료 용액을 원심분리하여 중층액을 얻을 때 특히 주의해야 한다. 하층부에 활성탄가루가 약간 가라앉게 되는데 이를 취하지 않아야 한다. 그리고 매 측정마다 석영큐벳을 세척하여 사용해야 한다. 또한 석영 큐벳의 경우 UV측정하는 부분에 지문이나 먼지를 묻히지 않아야 한다.
이 실험을 통해서 흡착의 개념과 농도의 변화에 따른 염료의 활성탄 표면에서의 흡착 성질을 이해할 수 있었다. 하지만 데이터가 올바르게 나오지 않아 아쉬웠다.
6. REFERENCE
1. H.S.Shin. \"Fundamental Chemical Engineering Laboratory Manual\"
2. Gilbert W. Castellan. \"Physical Chemistry\", 3rd. ed., Addison-Wesley. New York, 1983.
UV측정에서는 처음에 석영큐벳에 증류수를 넣어 기준을 잡아주었다. 그 다음 준비한 표준용액들을 석영큐벳에 담아 UV측정기에 넣어 흡광도를 측정하였다. 이 때 그래프가 완만하게 그려지지 않거나 측정범위를 경우 다시 측정하거나 용액을 희석시켜 측정하였다. 매 측정마다 석영큐벳을 세척하며 활성탄을 넣은 용액도 같은 방법으로 측정하였다. 측정이 완료되면 표준용액의 농도에 따른 흡광도 그래프를 그린 다음 그래프의 방정식을 구해 활성탄을 넣은 염료의 농도를 구하였다.
4. RESULTS
4.1 Raw data
Table 2. 표준용액 농도 vs 흡광도
표준용액(ppm)
흡광도
5
0.380554
10
0.7828
25
1.79341
50
4.25336
100
7.50048
Figure 1. 표준용액 5ppm의 흡광도 그래프
Figure 2. 표준용액 10ppm의 흡광도 그래프
Figure 3. 표준용액 25ppm의 흡광도 그래프
Figure 4. 표준용액 50ppm의 흡광도 그래프
Figure 5. 표준용액 100ppm의 흡광도 그래프
Table 3. 활성탄 무게 vs 흡광도(1/10희석)-샘플용액
활성탄(g)
흡광도
0.25
0.94079
0.5
1.06938
1
0.99915
1.2
1.10402
1.6
0.98972
Figure 6. 샘플용액 0.25g의 흡광도 그래프
Figure 7. 샘플용액 0.5g의 흡광도 그래프
Figure 8. 샘플용액 1g의 흡광도 그래프
Figure 9. 샘플용액 1.2g의 흡광도 그래프
Figure 10. 샘플용액 1.6g의 흡광도 그래프
4.2 Results
4.2.1 염료 용액의 농도
Table 2.로부터 농도에 대한 흡광도 그래프를 그린 후 방정식을 세운다.
Figure 11. 표준용액의 농도 vs 흡광도 그래프
y = ax + b
Intercept(절편) 0.05413
Slope(기울기) 0.076
따라서 y=(0.076)x+0.05413 이다.
이 방정식으로부터 샘플용액의 농도를 구한다.
1/10배로 희석했으므로 구한 농도에 10배를 해준다.
(x : 농도, y : 흡광도)
Table 4. 활성탄 무게 vs 염료용액의 농도
활성탄(g)
농도(ppm)
0.25
116.666
0.5
133.586
1
124.345
1.2
138.143
1.6
123.104
계산과정 예)
Figure 12. 활성탄 무게 vs 염료용액의 농도 그래프
4.2.2 염료용액의 흡착량
q : 흡착량(mg/g), Co : 염료용액의 처음 농도(ppm), Cf : 염료용액의 평형농도(ppm),
V : 염료 용액의 부피(L), M : 활성탄의 무게(g)
Table 5. 활성탄 무게 대 염료용액의 흡착량
활성탄(g)
흡착량(mg/g)
0.25
6.6668
0.5
1.6414
1
1.2828
1.2
0.4940
1.6
0.8405
계산과정 예)
Figure 13. 활성탄 무게 vs 흡착량 그래프
5. DISCUSSION
이번 ‘흡착 평형’이라는 실험은 일정한 온도에서 염료의 활성탄 표면에서의 흡착 성질을 알아보기 위한 것이다.
실험 결과 표준 용액의 농도 vs 흡광도 그래프를 fitting하여 y=ax+b의 방정식을 얻었다. 여기서 기울기는 a는 0.076, y 절편 b는 0.05413이다. 그리고 이 방정식에 샘플용액의 흡광도 측정값을 대입하여 샘플용액의 농도를 구하였다. 대입결과 활성탄 0.25g의 경우에 염료 용액의 농도는 116.666ppm이고, 0.5g, 1.0g, 1.2g, 1.6g경우 각각 133.586ppm, 124.345ppm, 138.143ppm, 123.104ppm이다. 마지막으로 이 데이터 값을 mass balance하면 각각의 활성탄 양에 대한 흡착량은 6.6668mg/g, 1.6414mg/g, 1.2828mg/g, 0.4940mg/g, 0.8405mg/g이었다.
데이터 처리 결과 활성탄의 무게가 증가함에 따라 염료의 농도가 감소해야 하는데 그러지 못하였다. 또한 흡착량은 증가해야하는데 대체로 감소하는 경향을 보여 매우 큰 오차가 발생하였다.
오차의 원인에는 마이크로피펫 사용을 잘못 사용한 경우가 있다. 마이크로피펫을 사용하기 전에 사용법을 충분히 익혀야 한다. 그리고 마이크로피펫을 사용할 때 너무 세게 누르면 용액이 더 많이 취해지게 되는데 이를 주의해야 한다. 또 원심분리액을 취할 때 산소를 취해 기포가 발생하지 않도록 해야 한다.
또한 용액이 충분히 평형상태에 도달하지 않은 경우에도 오차가 발생한다. 약 14시간 정도 용액을 평형에 도달하도록 하였는데 염료용액이 활성탄 표면에 충분히 흡착되어 평형에 이르도록 일주일 정도 충분히 시간을 두어야 한다. 이번 실험의 오차의 대부분은 용액이 평형에 도달하지 못해 생긴 것 같다.
석영큐벳을 이용하여 UV를 측정할 때는 석영큐벳에 지문이나 먼지가 묻지 않도록 해야 하며, 큐벳 안에 넣은 용액에 불순물이 섞이지 않도록 주의해야 한다. 이 실험은 미세한 양에 의해 데이터 값이 변하므로 염료 용액이나 증류수에 불순물이 섞이지 않도록 해야 한다. 활성탄을 넣은 염료 용액을 원심분리하여 중층액을 얻을 때 특히 주의해야 한다. 하층부에 활성탄가루가 약간 가라앉게 되는데 이를 취하지 않아야 한다. 그리고 매 측정마다 석영큐벳을 세척하여 사용해야 한다. 또한 석영 큐벳의 경우 UV측정하는 부분에 지문이나 먼지를 묻히지 않아야 한다.
이 실험을 통해서 흡착의 개념과 농도의 변화에 따른 염료의 활성탄 표면에서의 흡착 성질을 이해할 수 있었다. 하지만 데이터가 올바르게 나오지 않아 아쉬웠다.
6. REFERENCE
1. H.S.Shin. \"Fundamental Chemical Engineering Laboratory Manual\"
2. Gilbert W. Castellan. \"Physical Chemistry\", 3rd. ed., Addison-Wesley. New York, 1983.
추천자료
 [일반화학실험1] 산 해리 평형(pH meter로 측정)
[일반화학실험1] 산 해리 평형(pH meter로 측정) 힘과 토크의 평형 실험 report
힘과 토크의 평형 실험 report [대학물리학] 회전운동 실험 (토크의 평형)
[대학물리학] 회전운동 실험 (토크의 평형) 토크의 평형 실험
토크의 평형 실험 [일반 물리학 실험] 힘의 평형 (예비 + 결과)
[일반 물리학 실험] 힘의 평형 (예비 + 결과) (생명화공실험)다시마를 이용한 흡착,탈착(예비+결과)
(생명화공실험)다시마를 이용한 흡착,탈착(예비+결과) [체온조절][체온][체열평형]체온조절과 체열평형, 체온조절과 조절기전, 체온조절과 피부온 ...
[체온조절][체온][체열평형]체온조절과 체열평형, 체온조절과 조절기전, 체온조절과 피부온 ... [화학공학기초실험] (예비+결과) 평형분배
[화학공학기초실험] (예비+결과) 평형분배 [일반화학실험]산-해리 평형 [예비와 결과 보고서]
[일반화학실험]산-해리 평형 [예비와 결과 보고서] 물리화학 실험 - 상평형 실험
물리화학 실험 - 상평형 실험 물리 및 실험 보고서 -힘의 평형
물리 및 실험 보고서 -힘의 평형 [화공실험] 액-액 추출 실험 예비 및 결과 : 연속상인 아세트산 수용액과 분산상인 벤젠을 왕...
[화공실험] 액-액 추출 실험 예비 및 결과 : 연속상인 아세트산 수용액과 분산상인 벤젠을 왕... 힘의 평형 실험
힘의 평형 실험 [물리화학 실험] (예비 레포트) 용매 사이의 용질의 분배 : 섞이지 않는 두 용매 사이의 평형...
[물리화학 실험] (예비 레포트) 용매 사이의 용질의 분배 : 섞이지 않는 두 용매 사이의 평형...
































소개글