
|
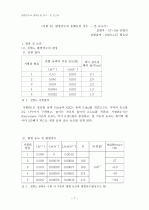
농도가 적은 것이 용해도곱 상수가 더 컸다. NaOH의 농도가 0.05M일때의 용해도곱 상수는 0.000000032이고 0.025M일 때는 0.000000032였다. 특히 용해도곱 상수는 온도에 따라서 변하기 때문에 온도를 주의해야했다. 일반화학 실험 - 용해상수의 결정
|
- 페이지 3페이지
- 가격 1,000원
- 등록일 2015.04.03
- 파일종류 한글(hwp)
- 참고문헌 없음
- 최근 2주 판매 이력 없음
|

|
화학 기초실험(2) 실험서
②응용화공 기초실험(1) 실험서
③Brady and Holum 일반화학 - 자유아카데미 출판사-
④고등학교 화학 교과서 (서정선, 홍창표, 이범흥, 전영협 저) - 지학사 출판- Ⅰ.서론
a. 실험 목적
b. 이론
Ⅱ. 실험
1.실험
|
- 페이지 5페이지
- 가격 1,300원
- 등록일 2014.06.05
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
화학회. 천문각.
두산 세계 대백과.
일반 화학. 탐구당. 인하대 화학 교재 편찬회 역.
분석화학, Daniel. C. Harris , 자유 아카데미. Ⅰ. 서 론 ----------------------------------------ⅲ
1. 크로마토그래피실험 연구의 목적
2. 크로마토그래피의
|
- 페이지 10페이지
- 가격 2,000원
- 등록일 2015.03.13
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
실험을 행하고 통과 시간을 각각 측정한다.
(7) 비중병을 이용하여 각 시료의 밀도를 측정한다.
5. 참고 문헌
[1] 3학년 1학기 ‘단위조작 및 실험‘ 실험노트
[2] 안전보건공단 화학물질정보 MSDS - 에틸렌글리콜
[3] Yunas A.cengel 외 1명, <유체역
|
- 페이지 10페이지
- 가격 1,500원
- 등록일 2020.05.13
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
화학실험법, 대학화학실험법편찬회, 단국대학교출판부, p.165~p.173.
[2] https://ko.wikipedia.org/wiki/%EC%A4%91%ED%99%94_%EB%B0%98%EC%9D%91 Ⅰ. 실험목적
Ⅱ. 실험원리
1. 알칼리
2. 완충 용액
3. 산-염기 적정 곡선
4. 중화 적정의 원리
5. 중화
|
- 페이지 7페이지
- 가격 1,700원
- 등록일 2021.01.18
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|
|
1 January 1998 Journal of Chemical Education에서 평형상수값 발췌
[2]. http://en.wikipedia.org/wiki/Solubility_equilibrium 에서 용해도곱 상수 발췌
표준 일반화학 실험 제6개정판 실험22. 평형상수와 용해도 곱 상수 측정 1. 결과 및 논의
2. 결론
3. reference
|
- 페이지 7페이지
- 가격 1,200원
- 등록일 2009.10.09
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
화학물질정보 MSDS
[2] 위키백과- 용존산소량, 윙클리 아지드화 나트륨 변법
[3] 조창선, 2005.01.15, 해양용어사전, 일진사
[4] 노재식 외 (2016). 《토목기사 대비 상하수도 공학》. 한솔아카데미. 68쪽. 1. 실험 목적
2. 바탕 이론
3. 실험 기기 및
|
- 페이지 12페이지
- 가격 1,500원
- 등록일 2020.05.13
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
2000,pp45~54
이은부,임무창,김재호『화학분석 기사』,성안당,2006,pp4-94~4-98
인권식, 손무정, 이장욱, 『분석화학 원리 및 실험』, 동화기술, 2003, pp.177~229
D.Kealey&P.J Haines『분석화학』,자유아카데미,2008,pp113~120
네이버 지식백과,(시약 및 기구) *
|
- 페이지 5페이지
- 가격 1,500원
- 등록일 2015.05.19
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
2+과 Mg2+ 이온은 EDTA와 착화합물을 형성한다. 용액에 있는 모든 Ca2+과 Mg2+ 이온이 착화합물을 형성할 수 있도록 충분한 EDTA가 첨가되면 용액의 색은 붉은색에서 파란색으로 변하는데, 이때의 점이 적정의 종말점이다. 01. 실험 제목
02. 실험
|
- 페이지 9페이지
- 가격 2,500원
- 등록일 2024.08.13
- 파일종류 워드(doc)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
질산칼륨, 질산칼륨
https://terms.naver.com/entry.nhn?docId=1145100&cid=40942&categoryId=32269
안전보건공단 화학물질정보, 질산구리, 질산구리,
https://msds.kosha.or.kr/kcic/msdsdetail.do 1. 서론
2. 실험이론
3. 실험기구 및 시약
4. 참고문헌
|
- 페이지 16페이지
- 가격 1,500원
- 등록일 2022.03.15
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|