목차
□목적
□이론
※Beer's Law
※Single/Double Beam system
※Absorbing Species
※Transition
※Solvent Effect
※LOL, LOQ
□실험 방법
□결과의 예측
□실험결과
□토의
□이론
※Beer's Law
※Single/Double Beam system
※Absorbing Species
※Transition
※Solvent Effect
※LOL, LOQ
□실험 방법
□결과의 예측
□실험결과
□토의
본문내용
도로 나타날 것이다.
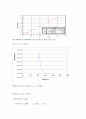
*미지용액의 흡광도를 측정하면 그림중 하나의 그래프로 나타날 것이다. 그리고 농도가 다른 용액들의 흡광도를 표시하면 그림과 같이 나타날 것이다.
*
`_{ max }
에서 흡광도의 값을 농도에 대하여 도식하면 다음과 같은 Calibration curve를 얻을 수 있다. 미지용액의 흡광도에 대응되는 용액의 농도를 그래프에서 구할 수 있다.
□실험결과
scan 200~500 nm, bandwidth 2 nm, NIR 20 nm, Data pitch 2 nm
측정치: max = 218 nm
Calibration curve ( max = 218 nm)
농도( 10-2 mM)
흡광도
0.5
0.0915
1.0
0.1948
2.5
0.4675
5.0
1.0363
8.0
1.6589
10.0
2.0398
15.0
2.7012
20.0
2.7807
샘플의 농도 구하기
샘플의 흡광도:1.9648
y = 207.47x - 0.0188 (y: 흡광도, x: 농도)
x =
{ 1.9648+0.0018 } over { 207.47 }
= 0.0095609 = 0.97 10-2 mM
□토의
이번 실험은 Ultraviolet/Visible and Near-Infrared Absorption Spectroscopy를 이용하여 미지 시료의 농도를 결정하는 실험 이었다. 용액의 농도가 빛의 흡광도에 비례한다는 Beer의 법칙을 이용하여 표준용액의 농도에 따른 흡광도를 측정하고 일정 파장의 흡광도를 이용하여 Calibration curve를 그렸다. 그리고 미지시료의 흡광도를 측정하여 Calibration curve를 이용하여 농도를 알아 낼 수 있었다.
Base line은 기계자체의 흡수나 여러 가지 noise에 의한 오차를 없애주기 위해서 잡는다.
reference cell과 sample cell에 물을 넣고 흡광도 전 영역(200~2500nm)에서 측정한다. 이는 물이 파장을 흡수하는 영역을 제외한 나머지의 유용한 영역을 알아내기 위해서이다. 측정결과 200~500nm 영역에서 물의 흡수가 없는 유용한 영역을 얻었다.
물만을 넣고 다시 scan 하여 흡광도가 0.005 미만이 나와 이 값을 이용하였다. 스펙트럼의 그래프를 보면 처음에는 흡광도가 0으로 일정하다. 이것은 물이 2500nm 부근에서 빛을 대부분 흡수하기 때문에 기계에 도달하는 빛이 너무 약해서 기계가 인식하지 못한다. 그리고 그래프가 갑자기 변하는 부분이 있는데 이는 source나 grating이 바뀌기 때문이다. 처음 1mM의 미지 용액의 스펙트럼을 찍었을 때 하나의 경사 모양을 나타냈다. 용액의 농도가 너무 높아 이런 결과가 나타나며 용액의 농도가 5*10
`^{ -5 }
M부터 산모양의 가우스 분포를 나타 냈다.
우선 시료의 흡수 스펙트럼을 조사하여 최대흡수파장 ( max=218nm)를 결정한다. 최대흡수파장에서 흡광도를 측정하면 농도 변화에 다른 흡광도의 변화가 크지 않기고, 감도가 크고 높은 정확도를 가지게 된다.
흡광도가 가우스 분포는 나타내는 5*10
`^{ -5 }
M부터 농도를 낮춰가며 흡광도를 측정했다. 5*10
`^{ -5 }
M까지 측정한 후 미지시료의 흡광도를 측정해보니 1.9648이었다. 처음 시작한 5*10
`^{ -5 }
M의 흡광도가 1.0363으로 미지시료보다 더 작았으므로, 농도를 높여서 다시 측정하였다. 0.01mM까지는 흡광도가 linear하게 증가하였으나, 그 뒤로 흡광도가 예상 값에서 벗어났다. 그래서 0.01mM을 LOL로 잡고 이 측정값까지를 사용하여 Calibration curve를 그렸다. 그래프의 식은 Y = 207.47X - 0.018이며, y는 흡광도 x는 농도를 나타낸다.
측정된 직선의 식을 통해 미지 시료의 흡광도에 대응하는 농도를 구하면 0.97 10-2 mM이 나온다.
이번실험의 결과 값이 주어지지 실험을 통해 구한 농도가 정확히 구해졌는지 알 수 없다. 그리고 실험을 한번만 했기 때문에 실험이 제대로 실행되었는지 판단하기 어렵다. 다만 농도에 따라 흡광도가 Linear 하게 나오는 구간이 뚜렷하게 나타나 Beer의 법칙을 만족한다.
오차가 생길 수 있는 요인으로는 일정 농도의 용액을 만들 때, cell을 세척할 때 남아있을 수 있는 이전 농도의 용액, 그리고 세척 시 cell 겉 표면에 이물질이 묻어 다른 흡수를 나타내어 오차가 발생할 수 있다. 실제로 측정한 흡광도 값이 너무 이상하여 그 값을 다시 측정하기도 했다.
*미지용액의 흡광도를 측정하면 그림중 하나의 그래프로 나타날 것이다. 그리고 농도가 다른 용액들의 흡광도를 표시하면 그림과 같이 나타날 것이다.
*
`_{ max }
에서 흡광도의 값을 농도에 대하여 도식하면 다음과 같은 Calibration curve를 얻을 수 있다. 미지용액의 흡광도에 대응되는 용액의 농도를 그래프에서 구할 수 있다.
□실험결과
scan 200~500 nm, bandwidth 2 nm, NIR 20 nm, Data pitch 2 nm
측정치: max = 218 nm
Calibration curve ( max = 218 nm)
농도( 10-2 mM)
흡광도
0.5
0.0915
1.0
0.1948
2.5
0.4675
5.0
1.0363
8.0
1.6589
10.0
2.0398
15.0
2.7012
20.0
2.7807
샘플의 농도 구하기
샘플의 흡광도:1.9648
y = 207.47x - 0.0188 (y: 흡광도, x: 농도)
x =
{ 1.9648+0.0018 } over { 207.47 }
= 0.0095609 = 0.97 10-2 mM
□토의
이번 실험은 Ultraviolet/Visible and Near-Infrared Absorption Spectroscopy를 이용하여 미지 시료의 농도를 결정하는 실험 이었다. 용액의 농도가 빛의 흡광도에 비례한다는 Beer의 법칙을 이용하여 표준용액의 농도에 따른 흡광도를 측정하고 일정 파장의 흡광도를 이용하여 Calibration curve를 그렸다. 그리고 미지시료의 흡광도를 측정하여 Calibration curve를 이용하여 농도를 알아 낼 수 있었다.
Base line은 기계자체의 흡수나 여러 가지 noise에 의한 오차를 없애주기 위해서 잡는다.
reference cell과 sample cell에 물을 넣고 흡광도 전 영역(200~2500nm)에서 측정한다. 이는 물이 파장을 흡수하는 영역을 제외한 나머지의 유용한 영역을 알아내기 위해서이다. 측정결과 200~500nm 영역에서 물의 흡수가 없는 유용한 영역을 얻었다.
물만을 넣고 다시 scan 하여 흡광도가 0.005 미만이 나와 이 값을 이용하였다. 스펙트럼의 그래프를 보면 처음에는 흡광도가 0으로 일정하다. 이것은 물이 2500nm 부근에서 빛을 대부분 흡수하기 때문에 기계에 도달하는 빛이 너무 약해서 기계가 인식하지 못한다. 그리고 그래프가 갑자기 변하는 부분이 있는데 이는 source나 grating이 바뀌기 때문이다. 처음 1mM의 미지 용액의 스펙트럼을 찍었을 때 하나의 경사 모양을 나타냈다. 용액의 농도가 너무 높아 이런 결과가 나타나며 용액의 농도가 5*10
`^{ -5 }
M부터 산모양의 가우스 분포를 나타 냈다.
우선 시료의 흡수 스펙트럼을 조사하여 최대흡수파장 ( max=218nm)를 결정한다. 최대흡수파장에서 흡광도를 측정하면 농도 변화에 다른 흡광도의 변화가 크지 않기고, 감도가 크고 높은 정확도를 가지게 된다.
흡광도가 가우스 분포는 나타내는 5*10
`^{ -5 }
M부터 농도를 낮춰가며 흡광도를 측정했다. 5*10
`^{ -5 }
M까지 측정한 후 미지시료의 흡광도를 측정해보니 1.9648이었다. 처음 시작한 5*10
`^{ -5 }
M의 흡광도가 1.0363으로 미지시료보다 더 작았으므로, 농도를 높여서 다시 측정하였다. 0.01mM까지는 흡광도가 linear하게 증가하였으나, 그 뒤로 흡광도가 예상 값에서 벗어났다. 그래서 0.01mM을 LOL로 잡고 이 측정값까지를 사용하여 Calibration curve를 그렸다. 그래프의 식은 Y = 207.47X - 0.018이며, y는 흡광도 x는 농도를 나타낸다.
측정된 직선의 식을 통해 미지 시료의 흡광도에 대응하는 농도를 구하면 0.97 10-2 mM이 나온다.
이번실험의 결과 값이 주어지지 실험을 통해 구한 농도가 정확히 구해졌는지 알 수 없다. 그리고 실험을 한번만 했기 때문에 실험이 제대로 실행되었는지 판단하기 어렵다. 다만 농도에 따라 흡광도가 Linear 하게 나오는 구간이 뚜렷하게 나타나 Beer의 법칙을 만족한다.
오차가 생길 수 있는 요인으로는 일정 농도의 용액을 만들 때, cell을 세척할 때 남아있을 수 있는 이전 농도의 용액, 그리고 세척 시 cell 겉 표면에 이물질이 묻어 다른 흡수를 나타내어 오차가 발생할 수 있다. 실제로 측정한 흡광도 값이 너무 이상하여 그 값을 다시 측정하기도 했다.






























소개글