목차
1. 결과 및 논의
2. 결론
3. reference
2. 결론
3. reference
본문내용
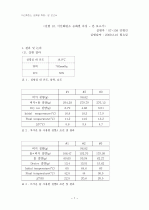
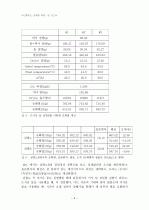
엔탈피로 승화에만 필요한 열을 구하려면 기체 팽창에 의한 일을 빼주어야 한다. 이 일은 로 n_g는 기체 몰 수이고 m은 드라이아이스 질량, M_w는 이산화탄소의 분자량인 44g/mol이 된다. 차가운 물 실험1에서 승화열2 값을 보정해 준다고 하면 드라이아이스 질량이 6.79g 이므로 일은 이므로 순수 승화열2는 595.35-249.5= 345.9J이 된다.
2. 결론
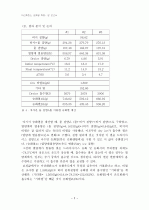
본 실험에서는 차가운 물과 뜨거운 물을 사용하는 두 가지 실험 방법으로 이산화탄소의 승화열을 측정하였고, 실험 결과로 얻은 승화열(승화엔탈피)이 얼마나 잘 구하여졌는지 정밀도와 정확도 및 오차를 계산, 분석하였다. 가능한 오차원인 중 중요한 것은 외부와의 열교환, 기계적 오차, 물 냉각시 얼음 생성, 부정확한 열용량, 이산화탄소 기체의 온도 상승시의 열 흡수 등이 있다.
3. 참고문헌
표준 일반화학 실험 제6개정판 실험10. 이산화탄소의 승화열 측정
이산화탄소의 승화열 참값 : http://kin.naver.com/detail/detail.php?d1id=11&dir_id=110204&eid=pU2JiTsNj4eX4Jdn73fftVjeQYmcasaJ&qb=7J207IKw7ZmU7YOE7IaMIOyKue2ZlOyXtA==&enc=utf8&pid=fN79gdoi5TNssaWuqGlsss--051788&sid=ScL83bvOwkkAABNoMrw
이산화탄소 비열 : Perry's Chemical Engineer's Handbook-6th edition(1984)
유리, 물 비열 : en.wikipedia.org/wiki/specific_heat
2. 결론
본 실험에서는 차가운 물과 뜨거운 물을 사용하는 두 가지 실험 방법으로 이산화탄소의 승화열을 측정하였고, 실험 결과로 얻은 승화열(승화엔탈피)이 얼마나 잘 구하여졌는지 정밀도와 정확도 및 오차를 계산, 분석하였다. 가능한 오차원인 중 중요한 것은 외부와의 열교환, 기계적 오차, 물 냉각시 얼음 생성, 부정확한 열용량, 이산화탄소 기체의 온도 상승시의 열 흡수 등이 있다.
3. 참고문헌
표준 일반화학 실험 제6개정판 실험10. 이산화탄소의 승화열 측정
이산화탄소의 승화열 참값 : http://kin.naver.com/detail/detail.php?d1id=11&dir_id=110204&eid=pU2JiTsNj4eX4Jdn73fftVjeQYmcasaJ&qb=7J207IKw7ZmU7YOE7IaMIOyKue2ZlOyXtA==&enc=utf8&pid=fN79gdoi5TNssaWuqGlsss--051788&sid=ScL83bvOwkkAABNoMrw
이산화탄소 비열 : Perry's Chemical Engineer's Handbook-6th edition(1984)
유리, 물 비열 : en.wikipedia.org/wiki/specific_heat
추천자료
 [일반화학실험] 나일론과 헤어젤 합성
[일반화학실험] 나일론과 헤어젤 합성 6. 일반화학실험 엔탈피 enthalpy - 엔탈피 측정
6. 일반화학실험 엔탈피 enthalpy - 엔탈피 측정 [일반화학실험] 글리신산구리의 합성 - 9-3. 글리신산 구리(ll) 및 벤조산의 합성
[일반화학실험] 글리신산구리의 합성 - 9-3. 글리신산 구리(ll) 및 벤조산의 합성 [일반화학실험] 용해열 구하기
[일반화학실험] 용해열 구하기 [일반화학실험] 르 샤틀리에의 원리
[일반화학실험] 르 샤틀리에의 원리 [일반화학실험] 엔탈피 측정 : 산과 염기의 중화반응을 이용해서 엔탈피가 상태함수임을 확인...
[일반화학실험] 엔탈피 측정 : 산과 염기의 중화반응을 이용해서 엔탈피가 상태함수임을 확인... [일반화학실험] 몰질량의 측정 : 이상기체 상태방정식을 이용하여 쉽게 증발하는 기체의 물질...
[일반화학실험] 몰질량의 측정 : 이상기체 상태방정식을 이용하여 쉽게 증발하는 기체의 물질... [일반화학실험] 재결정과 거르기 : 산 염기의 성질에 대하여 알아보고 그것을 이용하여 용해...
[일반화학실험] 재결정과 거르기 : 산 염기의 성질에 대하여 알아보고 그것을 이용하여 용해... 일반화학실험 - 아스피린의 제조
일반화학실험 - 아스피린의 제조 일반화학실험 비누만들기(비누의 합성) 레포트
일반화학실험 비누만들기(비누의 합성) 레포트 일반화학실험/ 엔탈피측정
일반화학실험/ 엔탈피측정 일반화학실험 - 비누화반응
일반화학실험 - 비누화반응
























소개글