목차
1. 실험 제목
2. 실험 목적
3. 실험 재료
4. 실험 이론 및 원리
5. 실험 방법
6. 실험 결과
7. 고찰
8. 참고문헌 및 출처
2. 실험 목적
3. 실험 재료
4. 실험 이론 및 원리
5. 실험 방법
6. 실험 결과
7. 고찰
8. 참고문헌 및 출처
본문내용
ris 50㎖
9.8
HCl 5㎖ 추가
8.72
HCl 5㎖ 추가
8.42
HCl 5㎖ 추가
8.25
HCl 5㎖ 추가
8.11
HCl 4.4㎖ 추가
8
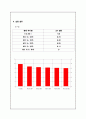
⑤ 0.05M의 tris buffer을 이용하여 HCl 첨가에 따른 buffer의 pH 변화를 알아보자.
(Buffer 용액이 만들어지면 1M HCl 용액을 피펫으로 1㎖ 씩 넣으며 pH 변화를
확인 후 그래프로 그려본다.)
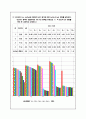
조
Buffer
pH
HCl (1M)
1㎖
2㎖
3㎖
4㎖
5㎖
6㎖
7㎖
8㎖
9㎖
10㎖
1
인산
6.5
6.48
6.35
6.23
6.09
5.90
5.72
5.37
4.61
3.67
3.14
2
인산
7.0
6.98
6.86
6.75
6.65
6.53
6.42
6.31
6.18
6.04
5.89
3
Tris
7.2
6.94
6.84
6.75
6.34
1.71
1.43
1.30
1.22
1.16
1.12
4
Tris
8.0
7.81
7.6
7.36
7.04
5.99
2.22
2.05
1.94
1.87
1.86
교수님
증류수
5.8
2.4
2.3
2.2
2.1
2.0
2.0
2.0
2.0
1.9
1.9
순서대로 1㎖, 2㎖, 3㎖, 4㎖, 5㎖~ 이다.
7. 고찰
이번 실험은 좀 까다롭고 어려웠다. 몰 용액도 만들어야 되고 pH 측정도 해야 되고,
측정할 때 용액의 양도 정확히 맞추어야 되서 진땀이 났다.
그래도 재미있는 실험이었다.
8. 참고문헌 및 출처
관상원예기초실험 교재 - Plant Physiology Laboratory Manual
관상원예기초실험 수업 필기
네이버 검색
네이버 백과사전 - pH meter, 완충용액
9.8
HCl 5㎖ 추가
8.72
HCl 5㎖ 추가
8.42
HCl 5㎖ 추가
8.25
HCl 5㎖ 추가
8.11
HCl 4.4㎖ 추가
8
⑤ 0.05M의 tris buffer을 이용하여 HCl 첨가에 따른 buffer의 pH 변화를 알아보자.
(Buffer 용액이 만들어지면 1M HCl 용액을 피펫으로 1㎖ 씩 넣으며 pH 변화를
확인 후 그래프로 그려본다.)
조
Buffer
pH
HCl (1M)
1㎖
2㎖
3㎖
4㎖
5㎖
6㎖
7㎖
8㎖
9㎖
10㎖
1
인산
6.5
6.48
6.35
6.23
6.09
5.90
5.72
5.37
4.61
3.67
3.14
2
인산
7.0
6.98
6.86
6.75
6.65
6.53
6.42
6.31
6.18
6.04
5.89
3
Tris
7.2
6.94
6.84
6.75
6.34
1.71
1.43
1.30
1.22
1.16
1.12
4
Tris
8.0
7.81
7.6
7.36
7.04
5.99
2.22
2.05
1.94
1.87
1.86
교수님
증류수
5.8
2.4
2.3
2.2
2.1
2.0
2.0
2.0
2.0
1.9
1.9
순서대로 1㎖, 2㎖, 3㎖, 4㎖, 5㎖~ 이다.
7. 고찰
이번 실험은 좀 까다롭고 어려웠다. 몰 용액도 만들어야 되고 pH 측정도 해야 되고,
측정할 때 용액의 양도 정확히 맞추어야 되서 진땀이 났다.
그래도 재미있는 실험이었다.
8. 참고문헌 및 출처
관상원예기초실험 교재 - Plant Physiology Laboratory Manual
관상원예기초실험 수업 필기
네이버 검색
네이버 백과사전 - pH meter, 완충용액
키워드
추천자료
 디지털논리회로실험1-8
디지털논리회로실험1-8 컴퓨터 그래픽 시스템
컴퓨터 그래픽 시스템 수용성 단백질 정량(Bradford Method) 실험 보고서
수용성 단백질 정량(Bradford Method) 실험 보고서 오라클데이타베이스구조
오라클데이타베이스구조 <실험레포트> Michaelis-Menten Kinetics
<실험레포트> Michaelis-Menten Kinetics 오라클 백업 복구
오라클 백업 복구 infix를 postfix로 전환 <파일입력을 통해서>
infix를 postfix로 전환 <파일입력을 통해서> [생화학 실험] PCR-mediated mutagenesis
[생화학 실험] PCR-mediated mutagenesis  [컴파일러, Compiler] Lex & Yacc 를 이용한 계산기 Report
[컴파일러, Compiler] Lex & Yacc 를 이용한 계산기 Report 생화학
생화학 [데이터 통신] Packet Sniffer의 구현
[데이터 통신] Packet Sniffer의 구현 [아주대-생물학실험] (결과) DNA의 구조 및 추출 & DNA 전기영동
[아주대-생물학실험] (결과) DNA의 구조 및 추출 & DNA 전기영동 [분석화학실험] Analysis of acid and base Titration Curve
[분석화학실험] Analysis of acid and base Titration Curve TIMER 교안
TIMER 교안
























소개글