목차
없음
본문내용
부피인 당량점에서의 부피와, 실제 실험을
통해 얻은 부피인 종말점에서의 부피의 차이로 인해 생기는 오차이다. 적정
오차를 줄이기 위해서는 먼저 지시약의 색깔, 반응물 또는 생성물의 광학
흡광도, pH와 같은 적당한 물리적 특성의 변화를 지표로 삼아야 한다. 또
다른 방법은 바탕 적정(blank titration)을 통해 보정할 수 있다. 바탕 적정은,
분석물질만 배고 똑같은 적정과정을 실행하는 것으로, 본 실험에서는
아스코르브산을 녹인 증류수만을 갖고 적정을 수행하는 것을 의미한다. 이
과정에서 소모된 아이오딘산 용액의 부피를 아스코르브산 용액 적정에 소모된
아이오딘산 용액 부피에서 뺀 값을 최종적인 적정 부피로 생각하면 된다.
(2) 온도와 녹말 착물간의 관계
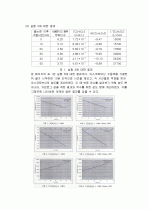
녹말-아이오딘 착물은 온도에 따라 변한다. 50℃에서 착물의 색깔은 25℃에서의
색깔의 세기에 비하여 정도밖에 되지 본 실험에서와 같이 100℃ 이상의
높은 온도로 가열한 아스코르브산 용액을 바로 적정에 사용하는 경우, 요오드-녹말
착물의 색이 확실하게 눈에 띠지 않기 때문에 적정오차는 더욱 커질 수 있다.
따라서 적정을 시작하기 전에 찬 물에 식히는 것이다. 만약 최대 감도가
요구된다면 얼음물에서의 냉각이 바람직하다.
온도가 증가함에 따라 착물의 색이 감소하는 이유는 착물의 구조에 있다.
녹말-요오드 착물은 나선형의 녹말분자 속으로 막대 형태의 요오드가 끼어들어간
형태를 취하고 있다. 그러나 온도가 증가하게 되면 녹말의 나선형구조가
안정화되지 않고 풀어지게 되며, 이로 인해 녹말-요오드 착물은 안정성을
잃게 되고 더 이상 색을 띠지 못한다. 온도가 증가할수록 안정성을 잃은 착물의
비율이 증가하게 되고 색은 점차 옅어지게 되는 것이다.
(3) I2를 직접 사용하지 않고 KIO3를 사용한 이유
I2를 이용함으로 인해 생기는 단점 중 하나는 I2의 승화성에 있다. I2는 일차
표준 물질이 될 정도로 충분히 순수하지만 승화성이 있기 때문에 무게를 정확히
측정하는 것은 사실상 불가능하다. 따라서 I2는 표준물질로는 거의 사용하지
않는다. 그 대신 I2의 무게를 대강 재고, 이로써 형성된 I3-용액을 정량하고자
하는 분석물질의 순수한 표준시료를 이용해 적정한다. 이러한 방법을
iodometry라 한다.
두 번째 이유는 I2의 용해도에 있다. I2는 무극성분자이기 때문에 극성 용매인
물에 잘 녹지 않는다. 실제로 요오드의 반응식 I2+H2OH++I-+HIO의 평형
상수는 k=2.0×10-13로 매우 용해도가 낮음을 알 수 있다. 그러나 IO-의 경우
3IO-→2I-+IO3-의 평형상수가 k=1020으로 굉장히 크다. 따라서 I2를 쓰는 것 보다
IO-를 써서 I-이온을 형성하는 것이 더욱 효율적임을 알 수 있다.
결과적으로, I2의 승화성과 무에 대한 낮은 용해도로 인해 실험에서는 KIO3를
사용한 것이다.
4. Reference
Daniel C. Harris, 김강진 등 역, 분석화학, 7thed, 자유아카데미, 2007,
p. 150~151, 412, 418~423
통해 얻은 부피인 종말점에서의 부피의 차이로 인해 생기는 오차이다. 적정
오차를 줄이기 위해서는 먼저 지시약의 색깔, 반응물 또는 생성물의 광학
흡광도, pH와 같은 적당한 물리적 특성의 변화를 지표로 삼아야 한다. 또
다른 방법은 바탕 적정(blank titration)을 통해 보정할 수 있다. 바탕 적정은,
분석물질만 배고 똑같은 적정과정을 실행하는 것으로, 본 실험에서는
아스코르브산을 녹인 증류수만을 갖고 적정을 수행하는 것을 의미한다. 이
과정에서 소모된 아이오딘산 용액의 부피를 아스코르브산 용액 적정에 소모된
아이오딘산 용액 부피에서 뺀 값을 최종적인 적정 부피로 생각하면 된다.
(2) 온도와 녹말 착물간의 관계
녹말-아이오딘 착물은 온도에 따라 변한다. 50℃에서 착물의 색깔은 25℃에서의
색깔의 세기에 비하여 정도밖에 되지 본 실험에서와 같이 100℃ 이상의
높은 온도로 가열한 아스코르브산 용액을 바로 적정에 사용하는 경우, 요오드-녹말
착물의 색이 확실하게 눈에 띠지 않기 때문에 적정오차는 더욱 커질 수 있다.
따라서 적정을 시작하기 전에 찬 물에 식히는 것이다. 만약 최대 감도가
요구된다면 얼음물에서의 냉각이 바람직하다.
온도가 증가함에 따라 착물의 색이 감소하는 이유는 착물의 구조에 있다.
녹말-요오드 착물은 나선형의 녹말분자 속으로 막대 형태의 요오드가 끼어들어간
형태를 취하고 있다. 그러나 온도가 증가하게 되면 녹말의 나선형구조가
안정화되지 않고 풀어지게 되며, 이로 인해 녹말-요오드 착물은 안정성을
잃게 되고 더 이상 색을 띠지 못한다. 온도가 증가할수록 안정성을 잃은 착물의
비율이 증가하게 되고 색은 점차 옅어지게 되는 것이다.
(3) I2를 직접 사용하지 않고 KIO3를 사용한 이유
I2를 이용함으로 인해 생기는 단점 중 하나는 I2의 승화성에 있다. I2는 일차
표준 물질이 될 정도로 충분히 순수하지만 승화성이 있기 때문에 무게를 정확히
측정하는 것은 사실상 불가능하다. 따라서 I2는 표준물질로는 거의 사용하지
않는다. 그 대신 I2의 무게를 대강 재고, 이로써 형성된 I3-용액을 정량하고자
하는 분석물질의 순수한 표준시료를 이용해 적정한다. 이러한 방법을
iodometry라 한다.
두 번째 이유는 I2의 용해도에 있다. I2는 무극성분자이기 때문에 극성 용매인
물에 잘 녹지 않는다. 실제로 요오드의 반응식 I2+H2OH++I-+HIO의 평형
상수는 k=2.0×10-13로 매우 용해도가 낮음을 알 수 있다. 그러나 IO-의 경우
3IO-→2I-+IO3-의 평형상수가 k=1020으로 굉장히 크다. 따라서 I2를 쓰는 것 보다
IO-를 써서 I-이온을 형성하는 것이 더욱 효율적임을 알 수 있다.
결과적으로, I2의 승화성과 무에 대한 낮은 용해도로 인해 실험에서는 KIO3를
사용한 것이다.
4. Reference
Daniel C. Harris, 김강진 등 역, 분석화학, 7thed, 자유아카데미, 2007,
p. 150~151, 412, 418~423
추천자료
 흡연이 혈장의 비타민 C 함량과 지질과산화 및 지질의 농도 변화에 미치는
흡연이 혈장의 비타민 C 함량과 지질과산화 및 지질의 농도 변화에 미치는 비타민 C 섭취 적으면 뇌졸중 위험 증가
비타민 C 섭취 적으면 뇌졸중 위험 증가  [화학실험1] Ascorbic Acid(비타민C)과 설탕의 분자량 측정
[화학실험1] Ascorbic Acid(비타민C)과 설탕의 분자량 측정 비타민에 관하여
비타민에 관하여 비타민 C의 역할
비타민 C의 역할 식품화학-비타민
식품화학-비타민 [활성산소][활성산소 종류][활성산소 제거][SOD][비타민C][토코페롤][만병의 근원]만병의 근...
[활성산소][활성산소 종류][활성산소 제거][SOD][비타민C][토코페롤][만병의 근원]만병의 근... FTA 대처를 위한 고급육 생산을 위한 비타민 C 급여 기술(사료 내 비타민 C 첨가)
FTA 대처를 위한 고급육 생산을 위한 비타민 C 급여 기술(사료 내 비타민 C 첨가) [비타민과건강] 영양제 및 시판 음료에 함유된 비타민 함량 조사
[비타민과건강] 영양제 및 시판 음료에 함유된 비타민 함량 조사 비타민 C와 당뇨병
비타민 C와 당뇨병  피부와 비타민 (피부미용)
피부와 비타민 (피부미용) 분석화학실험 - 비타민C의 요오드 적정
분석화학실험 - 비타민C의 요오드 적정 지용성 비타민과 수용성 비타민
지용성 비타민과 수용성 비타민 [서울대학교 화학실험] 요오드 적정에 의한 비타민 C 분석
[서울대학교 화학실험] 요오드 적정에 의한 비타민 C 분석