목차
1. 실험이론
(1) 물의 전리와 수소 이온 농도
(2) pH 미터
(3) 유리 전극과 pH미터의 원리 및 구조
(4) pH 미터의 용도
(5) 완충 용액
2. 실험방법
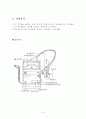
3. 실험장치
4. 결과 및 고찰
1) 실험계산 및 결과
(1) pH 측정결과
(2) 측정결과 그래프
(3) 각 pH 구간에 사용될 수 있는 pH 지시약
2) 결과고찰
5. 참고문헌
(1) 물의 전리와 수소 이온 농도
(2) pH 미터
(3) 유리 전극과 pH미터의 원리 및 구조
(4) pH 미터의 용도
(5) 완충 용액
2. 실험방법
3. 실험장치
4. 결과 및 고찰
1) 실험계산 및 결과
(1) pH 측정결과
(2) 측정결과 그래프
(3) 각 pH 구간에 사용될 수 있는 pH 지시약
2) 결과고찰
5. 참고문헌
본문내용
0.1N NaOH 적가할양
(ml)
1회
2회
3회
평균
실제적가량
HCl용액의pH
실제적가량
HCl용액의pH
실제적가량
HCl용액의pH
실제적가량
HCl용액의pH
0.00
1.97
2.04
2.02
2.01
10.00
2.22
2.23
2.22
2.22
20.00
2.78
2.70
2.72
2.73
21.00
2.93
2.82
2.88
2.87
22.00
3.14
2.98
3.10
3.07
23.00
3.75
3.25
3.62
3.54
24.00
5.29
4.32
6.19
5.26
24.50
7.15
5.69
7.64
6.82
24.90
10.89
0.1
9.62
10.20
10.23
25.00
10.96
10.06
10.39
10.47
25.10
11.06
10.41
10.51
10.66
25.50
11.26
11.07
10.92
11.08
26.00
11.43
11.30
11.21
11.31
28.00
11.75
11.70
11.66
11.70
30.00
11.90
11.86
11.83
11.86
(1) pH 측정결과
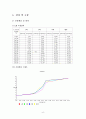
(2) 측정결과 그래프
■ 1회 ■ 2회 ■ 3회 ■ 평균
(3) 각 pH 구간에 사용될 수 있는 pH 지시약
지시약
pH 범위
Methyl violet
0.5 ~ 1.5
Thymol blue
1.2 ~ 2.8
Methyl yellow
2.9 ~ 4.0
Methyl orange
3.1 ~ 4.4
Bromomphenol blue
3.0 ~ 4.6
Bromocresol green
3.8 ~ 5.4
Methyl red
4.2 ~ 6.3
Chlorophenol red
4.8 ~ 6.4
Bromothymol blue
6.0 ~ 7.6
Paranitrophenol
6.2 ~ 7.5
Phenol red
6.4 ~ 8.0
Cresol red
7.2 ~ 8.8
Thymol blue
8.0 ~ 9.6
Phenolphthalein
8.0 ~ 9.8
Thymolphthalein
9.3 ~ 10.5
Alizarin yellow R
10.1 ~12.0
2) 결과고찰
이번 실험은 pH미터를 이용한 pH 측정 실험이었는데 pH 측정기의 원리를 습득 할 수 있었다.
3회까지의 pH의 측정값은 거의 비슷했다. 실험은 그다지 어렵지는 않았지만 실험에 의해 측정된 pH와 이론적 pH는 약간의 차이를 보였는데 오차가 생기는 원인으로는 정확한 농도의 NaOH를 조제 할 수가 없고, 기계 상의 오차도 발생하기 때문이라고 생각한다.
그리고 pH미터의 전극 검출부를 증류수로 3회 이상 씻고 깨끗한 거름종이나 탈지면으로 닦아야 하는데 그냥 수돗물을 받아놓고 사용하였다. 물의 pH는 항상 유지하는 것은 아니고 안의 녹아있는 CO2의 양과 온도 등의 상태에 따라서 pH가 변하게 된다. 이것도 pH 측정 결과 값에 약간의 영향을 준 것 같다.
5. 참고문헌
- http://www.nces.go.kr/R_Study/mpaqec/theory/handing/hydrogen/phmeter.htm
- 인터넷 사이트 두산동아대백과사전 & 브리태니커 백과사전
(ml)
1회
2회
3회
평균
실제적가량
HCl용액의pH
실제적가량
HCl용액의pH
실제적가량
HCl용액의pH
실제적가량
HCl용액의pH
0.00
1.97
2.04
2.02
2.01
10.00
2.22
2.23
2.22
2.22
20.00
2.78
2.70
2.72
2.73
21.00
2.93
2.82
2.88
2.87
22.00
3.14
2.98
3.10
3.07
23.00
3.75
3.25
3.62
3.54
24.00
5.29
4.32
6.19
5.26
24.50
7.15
5.69
7.64
6.82
24.90
10.89
0.1
9.62
10.20
10.23
25.00
10.96
10.06
10.39
10.47
25.10
11.06
10.41
10.51
10.66
25.50
11.26
11.07
10.92
11.08
26.00
11.43
11.30
11.21
11.31
28.00
11.75
11.70
11.66
11.70
30.00
11.90
11.86
11.83
11.86
(1) pH 측정결과
(2) 측정결과 그래프
■ 1회 ■ 2회 ■ 3회 ■ 평균
(3) 각 pH 구간에 사용될 수 있는 pH 지시약
지시약
pH 범위
Methyl violet
0.5 ~ 1.5
Thymol blue
1.2 ~ 2.8
Methyl yellow
2.9 ~ 4.0
Methyl orange
3.1 ~ 4.4
Bromomphenol blue
3.0 ~ 4.6
Bromocresol green
3.8 ~ 5.4
Methyl red
4.2 ~ 6.3
Chlorophenol red
4.8 ~ 6.4
Bromothymol blue
6.0 ~ 7.6
Paranitrophenol
6.2 ~ 7.5
Phenol red
6.4 ~ 8.0
Cresol red
7.2 ~ 8.8
Thymol blue
8.0 ~ 9.6
Phenolphthalein
8.0 ~ 9.8
Thymolphthalein
9.3 ~ 10.5
Alizarin yellow R
10.1 ~12.0
2) 결과고찰
이번 실험은 pH미터를 이용한 pH 측정 실험이었는데 pH 측정기의 원리를 습득 할 수 있었다.
3회까지의 pH의 측정값은 거의 비슷했다. 실험은 그다지 어렵지는 않았지만 실험에 의해 측정된 pH와 이론적 pH는 약간의 차이를 보였는데 오차가 생기는 원인으로는 정확한 농도의 NaOH를 조제 할 수가 없고, 기계 상의 오차도 발생하기 때문이라고 생각한다.
그리고 pH미터의 전극 검출부를 증류수로 3회 이상 씻고 깨끗한 거름종이나 탈지면으로 닦아야 하는데 그냥 수돗물을 받아놓고 사용하였다. 물의 pH는 항상 유지하는 것은 아니고 안의 녹아있는 CO2의 양과 온도 등의 상태에 따라서 pH가 변하게 된다. 이것도 pH 측정 결과 값에 약간의 영향을 준 것 같다.
5. 참고문헌
- http://www.nces.go.kr/R_Study/mpaqec/theory/handing/hydrogen/phmeter.htm
- 인터넷 사이트 두산동아대백과사전 & 브리태니커 백과사전
추천자료
 양이온정성분석
양이온정성분석 실험4. 아스피린의 합성
실험4. 아스피린의 합성 실험3. 밀도의 측정
실험3. 밀도의 측정 실험5. 흡광광도 분석
실험5. 흡광광도 분석 실험6. 빛의 편광 특성
실험6. 빛의 편광 특성 화학실험-화학전지와 전기화학적 서열
화학실험-화학전지와 전기화학적 서열 [식품미생물학실험]그람염색&카탈라아제테스트(gram staining & catalase test)
[식품미생물학실험]그람염색&카탈라아제테스트(gram staining & catalase test) 지시약의 이온화 상수
지시약의 이온화 상수 병원미생물학실험_report_3_(단순염색 및 그람염색)
병원미생물학실험_report_3_(단순염색 및 그람염색) 양이온 피피티
양이온 피피티 물리화학실험(설탕반전반응)[1][1]
물리화학실험(설탕반전반응)[1][1] 화학실험 - 화학전지[원소들간의 산화 환원 정도 차이를 이용하여 화학 전지의 원리에 대하여]
화학실험 - 화학전지[원소들간의 산화 환원 정도 차이를 이용하여 화학 전지의 원리에 대하여] [실험보고서] PH meter(미터) 실험
[실험보고서] PH meter(미터) 실험 일반화학실험-산 염기 적정 A+레포트
일반화학실험-산 염기 적정 A+레포트