본문내용
4
12.06
37.4
12.08
43.4
12.16
44.4
12.17
2. 결과 및 토의
B-1. NaOH 표준용액의 적정
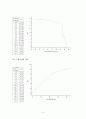
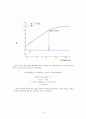
0.5M 옥살산 용액을 농도를 알 수 없는 NaOH 용액에 일정량씩 떨어뜨리며 pH를 측정하였다. 떨어뜨린 옥살산 용액의 양에 대한 pH의 변화를 그래프로 그려서 당량점을 찾았다. 변곡점(당량점)을 찾기 위해 그래프(B)를 2차 미분하였다. 2계 도함수(파란색)가 0인 지점에서 그래프 B의 부호가 바뀌므로 변곡점은 A점과 B점 두 개의 변곡점이 나온다. A와 B의 중간 값 C를 읽으면 옥살산 13.51mL에 pH는 9.09이고, pOH=4.91이다.
옥살산 용액과 NaOH 용액의 반응은 다음과 같다.
산과 염기의 수용액이 중화할 경우에는 다음이 성립하므로
(염기의 OH-)=(산의 H+)
B-2. 식용 식초의 적정
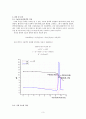
실험 B-1처럼 2계 도함수(파란색)의 부호가 바뀌는 점이 당량점이므로 식용 식초의 적정에서는 NaOH 용액 22.81mL가 사용되었다.
(염기의 OH-)=(산의 H+)
실험 A와 B를 비교해 보면 실험 A에서의 아세트산의 몰농도는 0.23M 이였고 실험 B에서의 아세트산의 몰농도는 0.21M로 오차는 8.70%이다.
12.06
37.4
12.08
43.4
12.16
44.4
12.17
2. 결과 및 토의
B-1. NaOH 표준용액의 적정
0.5M 옥살산 용액을 농도를 알 수 없는 NaOH 용액에 일정량씩 떨어뜨리며 pH를 측정하였다. 떨어뜨린 옥살산 용액의 양에 대한 pH의 변화를 그래프로 그려서 당량점을 찾았다. 변곡점(당량점)을 찾기 위해 그래프(B)를 2차 미분하였다. 2계 도함수(파란색)가 0인 지점에서 그래프 B의 부호가 바뀌므로 변곡점은 A점과 B점 두 개의 변곡점이 나온다. A와 B의 중간 값 C를 읽으면 옥살산 13.51mL에 pH는 9.09이고, pOH=4.91이다.
옥살산 용액과 NaOH 용액의 반응은 다음과 같다.
산과 염기의 수용액이 중화할 경우에는 다음이 성립하므로
(염기의 OH-)=(산의 H+)
B-2. 식용 식초의 적정
실험 B-1처럼 2계 도함수(파란색)의 부호가 바뀌는 점이 당량점이므로 식용 식초의 적정에서는 NaOH 용액 22.81mL가 사용되었다.
(염기의 OH-)=(산의 H+)
실험 A와 B를 비교해 보면 실험 A에서의 아세트산의 몰농도는 0.23M 이였고 실험 B에서의 아세트산의 몰농도는 0.21M로 오차는 8.70%이다.























소개글