
|
용해도곱을 비교하여보니 비슷하였고 , 대학화학책 뒷면에 나와 있는 이론적 용해도곱상수는 7.9*10 인데 이에도 비슷한 결과가 나왔다.
결론
용해도곱에서 오차가 있는 이유를 생각해 보았는데 오차의 원인은 HCl , NaOH용액 농도가 확실하였는
|
- 페이지 2페이지
- 가격 800원
- 등록일 2009.06.03
- 파일종류 한글(hwp)
- 참고문헌 없음
- 최근 2주 판매 이력 없음
|

|
용해도곱상수를 측정하는 방법과 르샤틀리에의 원리도 이해할 수 있는 실험이었다.
6.참고문헌
1)일반화학[자유아카데미, 제5판, p.A-25, Table C.5]
(Ksp)
2)https://en.wikipedia.org/wiki/Calcium_hydroxide
(Calcium hydroxide) 1.실험제목
2.실험목적
3.실험결과
|
- 페이지 3페이지
- 가격 2,000원
- 등록일 2016.05.27
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
=11200%이다.
5. log[Ca2+] 대 log[OH-]를 그래프로 그리고 Ksp를 구하여라.
Ksp=[Ca2+][OH-]2
logKsp=log[Ca2+][OH-]2
logKsp=log[Ca2+]+2[OH-]
log[Ca2+]=logKsp-2log[OH-]
y =logKsp- x
순수한물 log[ca2+]=log0.0325=-1.488 log[OH-]=log0.065=-1.187
0.1M NaOH log[ca2+]=log0.01=-2 log[OH-]=log0.02=-1.699
0.05M
|
- 페이지 3페이지
- 가격 13,860원
- 등록일 2013.05.20
- 파일종류 한글(hwp)
- 참고문헌 없음
- 최근 2주 판매 이력 없음
|

|
* 불포화용액
- 용매가 녹일 수 있는 양보다 적은 양의 용질이 녹아 있어 용질을 더 녹일 수 있는 용액으로 용해도는 온도에 따라 바뀌기 때문에 포화용액의 온도를 변화시켜 불포화용액으로 만들 수 있다.
* 포화용액
- 일정 온도에서 일정량
|
- 페이지 3페이지
- 가격 500원
- 등록일 2015.11.27
- 파일종류 한글(hwp)
- 참고문헌 없음
- 최근 2주 판매 이력 없음
|

|
상수를 구할 때 분모에 [SCN-]이 있지만, ②의 반응식에서 평형상수를 구할 때, 분모에 [SCN-]2 이다. 그러므로 색을 띤 화학종이 FeSCN2+일 때보다, Fe(SCN)2+일 때의 평형상수값이 더 작다.
5. 실험결과 및 검토
농도를 구하는 방법에는 분광광도계와
|
- 페이지 3페이지
- 가격 9,660원
- 등록일 2013.12.15
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|
|
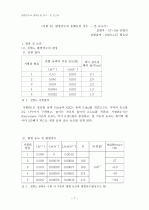
서 칼슘이온이 침전되는 역반응이 일어난다. 결과적으로 농도가 더 높은 수산화나트륨 용액일 수록 더 적은 칼슘 이온 농도를 보였다.
3). 각 용액에서의 용해도곱을 비교하고, 용해도곱이 상수임을 알아보자. 실험에서 얻은 값과 문헌에서 조
|
- 페이지 7페이지
- 가격 1,200원
- 등록일 2009.10.09
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
표준용액 약 100 mL
Ca(OH)2
페놀프탈레인 지시약
실험결과 3. 용해도곱 상수의 결정
학번 : 이름 : 조 :
1.실험결과
각 관찰값과 계산 값을 쓰시오.
순수한 물
0.025M
NaOH용액
0.050M
NaOH용액
0.100M
NaOH용액
온도 (℃)
21
21.5
22
23
0.10M
Hcl의 부피 (ml)
10.5
14.3
|
- 페이지 7페이지
- 가격 1,200원
- 등록일 2005.12.05
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
같은 평형이 이루어진다.
Ca(OH)2(s) ? Ca2+(aq) + 2OH-(aq)
이 반응의 평형상수인 용해도곱 상수는 다음과 같이 표현된다.
Ksp = [Ca2+][OH-]2
*************(이하생략)*********** 1.실험목적
2.이론적 고찰
3.실험결과 및 고찰
4.결과 및 종합의견
|
- 페이지 3페이지
- 가격 800원
- 등록일 2023.11.28
- 파일종류 워드(doc)
- 참고문헌 없음
- 최근 2주 판매 이력 없음
|

|
상수를 용해도 곱 상수(Solubility product)라고 부르며, 포화용액에서 염을 구성하는 양이온과 음이온의 농도를 곱하여 구한 다. 표기는 보통 로 표시한다. 고체의 경우, 그 농도는 계산에서 1로 정의한다. (1) 서론
(2) 이론
(3) 실험
(4) 결과
|
- 페이지 5페이지
- 가격 2,500원
- 등록일 2024.02.09
- 파일종류 아크로벳(pdf)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|

|
4. 실험이론
4-1. 평형상수의 결정
4-2. 용해도곱상수의 결정
5. 실험기구 및 시약
5-1. 실험기구
5-2. 시약
6. 실험방법
7. 실험결과
8. 고찰
8-1. 오차의 원인 분석
8-2. 오차를 줄이기 위한 방안
8-3. 생각해야 할 사항
9. 참고문헌 및 사이트
|
- 페이지 6페이지
- 가격 1,300원
- 등록일 2013.10.04
- 파일종류 한글(hwp)
- 참고문헌 있음
- 최근 2주 판매 이력 없음
|