목차
1. 실험 목적
2. 이론
3. 실험 시약 및 기구
4. 실험 방법
2. 이론
3. 실험 시약 및 기구
4. 실험 방법
본문내용
혼합한 이 순간부터 시간을 기록한다.
⑥ 시간에 따른 (3,6,9,12,15,........ ) 선광도를 측정하여 기록한다.
이때, 더 이상 편광계의 값이 변화가 없는 시간, 즉 반응이 종료되었을 때의 값을 라 한다.
⑦ 같은 방법으로 30 에서의 값을 측정하여 기록한다.
⑧ 실험 Data를 가지고 자당용액의 반응속도상수(k)와 활성화 에너지(Ea)를 구한다.
3) Data
(1) 반응속도 상수(k)
- { da} over {dt } = ka
(1차 반응식), 양변을 적분하면,
INT _{ 0}^{t } { -1} over { a} {da} over {dt} = INT _{0 }^{t } k
되고,
비 선광도 식
LEFT [ alpha RIGHT ] `_{D} ^{t} = {100 alpha } over ~C
에서 농도(C)와 선광도( )는 비례하므로, 정리하면
ln{ { a}_{0 }} over {{a}_{t}} = kt
가 된다.
(2) 계산결과
< 20 에서의 선광도 측정 data값 >
Time
(min)
{a}_{t}
(at 20 )
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }}
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }} = kt
으로부터 구한 k(min-1)
o
14.7
-
-
3
3.5
0.99
0.330
6
2.05
1.24
0.206
10
1.25
1.41
0.141
15
1.1
1.44
0.096
20
0.6
1.57
0.079
25
0.52
1.59
0.064
30
-0.9
2.09
0.069
35
-1.7
2.54
0.073
40
-2.2
2.98
0.075
45
-2.75
3.92
0.087
50
-2.8
4.08
0.082
55
-2.9
4.49
0.075
60
-3.1
5.87
0.098
24h
-3.15
-
k값의 산술평균 : 0.1135 min-1
36h
-3.15
-
48h
-3.15
-
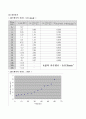
< 20 에서의 선광도 그래프 >
< 30 에서의 선광도 측정 data값 >
Time
(min)
{a}_{t}
(at 30 )
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }}
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }} = kt
으로부터 구한 k(min-1)
o
11.85
-
-
3
5.35
0.810
0.270
6
5.2
0.840
0.140
10
4.75
0.933
0.093
15
2.65
1.543
0.102
20
1.7
2.021
0.101
25
1.05
2.565
0.103
30
0.85
2.816
0.094
35
0.6
3.250
0.093
40
0.5
3.509
0.088
45
0.3
4.357
0.097
50
0.2
5.455
0.110
55
0.15
-
k값의 산술평균 : 0.1172 min-1
60
0.15
-
24h
0.15
-
36h
0.15
-
48h
0.15
-
< 30 에서의 선광도 그래프 >
(3) 활성화 에너지 (Ea)
온도 T1에서, ki는 아레늬우스 식에 의해 구할 수 있다.
{ k}_{ i} = A {e }^{ { { -E}_{ a} } over {R {T }_{i } } }
자연대수를 취하고, 온도 T2,
ln{k}_{1}= ln{} A - {{E}_{a}over{R}}·{1}over{{T}_{1}}
ln{k}_{2} = ln{} A - {{E}_{a}over{R}}·{1}over{{T}_{2}}
ln{k}_{1}
을
ln{k}_{2}
로 빼주면,
ln{{k}_{1}over{k}_{2}} = {}-{} {{E}_{a}over{R}}·({1}over{{T}_{1}}-{1}over{{T}_{2}})
{E}_{a}{}{}{}={}{}{} {R{}·{}ln{{k}_{1}}over{{k}_{2}}}over{{1}over{{T}_{2}}{}-{}{1}over{{T}_{1}}}
위 식으로부터 활성화 에너지를 구해 보면,
k1 = 0.1135 min-1 ( at 20 ) , k2 = 0.1172 min-1 ( at 30 )
{E}_{a}{}{}{}={}{}{} {8.314{}[{J}over{㏖·K}]{}·{}ln{{0.1135}}over{{0.1175}}}over{{1}over{{303.15K}}{}-{}{1}over{{293.15K}}}
= {}{}2.559{} TIMES {}{10}^{3}{} {J}over{mol}
5. 고찰
⑥ 시간에 따른 (3,6,9,12,15,........ ) 선광도를 측정하여 기록한다.
이때, 더 이상 편광계의 값이 변화가 없는 시간, 즉 반응이 종료되었을 때의 값을 라 한다.
⑦ 같은 방법으로 30 에서의 값을 측정하여 기록한다.
⑧ 실험 Data를 가지고 자당용액의 반응속도상수(k)와 활성화 에너지(Ea)를 구한다.
3) Data
(1) 반응속도 상수(k)
- { da} over {dt } = ka
(1차 반응식), 양변을 적분하면,
INT _{ 0}^{t } { -1} over { a} {da} over {dt} = INT _{0 }^{t } k
되고,
비 선광도 식
LEFT [ alpha RIGHT ] `_{D} ^{t} = {100 alpha } over ~C
에서 농도(C)와 선광도( )는 비례하므로, 정리하면
ln{ { a}_{0 }} over {{a}_{t}} = kt
가 된다.
(2) 계산결과
< 20 에서의 선광도 측정 data값 >
Time
(min)
{a}_{t}
(at 20 )
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }}
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }} = kt
으로부터 구한 k(min-1)
o
14.7
-
-
3
3.5
0.99
0.330
6
2.05
1.24
0.206
10
1.25
1.41
0.141
15
1.1
1.44
0.096
20
0.6
1.57
0.079
25
0.52
1.59
0.064
30
-0.9
2.09
0.069
35
-1.7
2.54
0.073
40
-2.2
2.98
0.075
45
-2.75
3.92
0.087
50
-2.8
4.08
0.082
55
-2.9
4.49
0.075
60
-3.1
5.87
0.098
24h
-3.15
-
k값의 산술평균 : 0.1135 min-1
36h
-3.15
-
48h
-3.15
-
< 20 에서의 선광도 그래프 >
< 30 에서의 선광도 측정 data값 >
Time
(min)
{a}_{t}
(at 30 )
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }}
ln {{a}_{0} - {a}_{ }}over {{a}_{t} - {a}_{ }} = kt
으로부터 구한 k(min-1)
o
11.85
-
-
3
5.35
0.810
0.270
6
5.2
0.840
0.140
10
4.75
0.933
0.093
15
2.65
1.543
0.102
20
1.7
2.021
0.101
25
1.05
2.565
0.103
30
0.85
2.816
0.094
35
0.6
3.250
0.093
40
0.5
3.509
0.088
45
0.3
4.357
0.097
50
0.2
5.455
0.110
55
0.15
-
k값의 산술평균 : 0.1172 min-1
60
0.15
-
24h
0.15
-
36h
0.15
-
48h
0.15
-
< 30 에서의 선광도 그래프 >
(3) 활성화 에너지 (Ea)
온도 T1에서, ki는 아레늬우스 식에 의해 구할 수 있다.
{ k}_{ i} = A {e }^{ { { -E}_{ a} } over {R {T }_{i } } }
자연대수를 취하고, 온도 T2,
ln{k}_{1}= ln{} A - {{E}_{a}over{R}}·{1}over{{T}_{1}}
ln{k}_{2} = ln{} A - {{E}_{a}over{R}}·{1}over{{T}_{2}}
ln{k}_{1}
을
ln{k}_{2}
로 빼주면,
ln{{k}_{1}over{k}_{2}} = {}-{} {{E}_{a}over{R}}·({1}over{{T}_{1}}-{1}over{{T}_{2}})
{E}_{a}{}{}{}={}{}{} {R{}·{}ln{{k}_{1}}over{{k}_{2}}}over{{1}over{{T}_{2}}{}-{}{1}over{{T}_{1}}}
위 식으로부터 활성화 에너지를 구해 보면,
k1 = 0.1135 min-1 ( at 20 ) , k2 = 0.1172 min-1 ( at 30 )
{E}_{a}{}{}{}={}{}{} {8.314{}[{J}over{㏖·K}]{}·{}ln{{0.1135}}over{{0.1175}}}over{{1}over{{303.15K}}{}-{}{1}over{{293.15K}}}
= {}{}2.559{} TIMES {}{10}^{3}{} {J}over{mol}
5. 고찰
추천자료
 화학양론-구리반응
화학양론-구리반응 [일반화학실험] 평형상수의 결정
[일반화학실험] 평형상수의 결정 [일반화학및실험] 평형상수와 용해도곱 상수의 결정
[일반화학및실험] 평형상수와 용해도곱 상수의 결정  [일반화학및실험] 시계반응
[일반화학및실험] 시계반응 화학실험 사례(에멀젼합성, 산소요구량), 화학실험 사례(평형상수결정), 화학실험 사례(밀크,...
화학실험 사례(에멀젼합성, 산소요구량), 화학실험 사례(평형상수결정), 화학실험 사례(밀크,... 화학 - 에스테르화 반응
화학 - 에스테르화 반응 화학공정실험 시계반응
화학공정실험 시계반응  전기분해와 도금 - 전기에너지를 이용하여 일어나는 화학반응에 대하여 알아본다
전기분해와 도금 - 전기에너지를 이용하여 일어나는 화학반응에 대하여 알아본다 [물리화학] 깁스 프리 에너지와 평형상수와의 관계
[물리화학] 깁스 프리 에너지와 평형상수와의 관계 [일반화학실험] 결과보고서-평형상수의 결정
[일반화학실험] 결과보고서-평형상수의 결정 화학공학실험 - 기액평형 실험(기-액 평형 실험)
화학공학실험 - 기액평형 실험(기-액 평형 실험) [일반화학실험] 평형 상수와 용해도곱 결정
[일반화학실험] 평형 상수와 용해도곱 결정 [일반화학실험] 전기분해와 도금 : 전기에너지를 이용하여 일어나는 화학반응에 대하여 알아...
[일반화학실험] 전기분해와 도금 : 전기에너지를 이용하여 일어나는 화학반응에 대하여 알아... 화학반응열의 측정과 Hess의 법칙(결과레포트)
화학반응열의 측정과 Hess의 법칙(결과레포트)






























소개글